Clear Sky Science · de
Verminderte Expression von BIRC2 und BIRC3 verbunden mit längerer Überlebenszeit bei pädiatrischen hochgradigen Gliomen
Warum bei Hirntumoren von Kindern neue Hinweise nötig sind
Pädiatrische hochgradige Gliome gehören zu den tödlichsten kindlichen Hirntumoren; Operation, Bestrahlung und Chemotherapie helfen derzeit nur einer kleinen Minderheit der Patient:innen. Diese Studie stellt eine einfache, aber entscheidende Frage: Gibt es molekulare „Überlebensschalter“ in diesen Tumoren, die Krebszellen davor bewahren zu sterben, und können diese Schalter erklären, warum einige Kinder länger leben als andere?
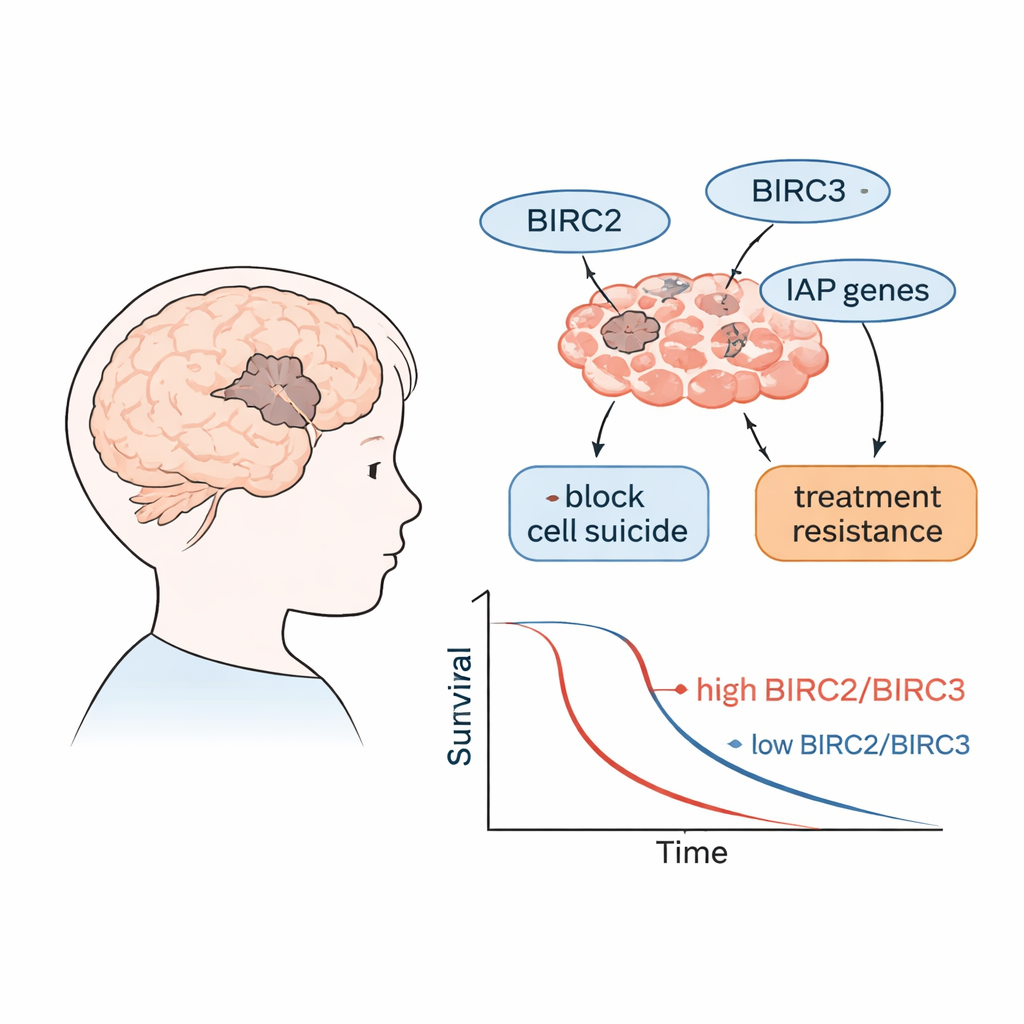
Proteine, die Krebszellen am Sterben hindern
Unsere Zellen verfügen über ein eingebautes Selbstzerstörungsprogramm, oft als programmierter Zelltod oder Apoptose bezeichnet, das beschädigte oder gefährliche Zellen entfernt. Eine Proteinfamilie, die als IAPs (Inhibitoren der Apoptoseproteine) bekannt ist, kann diese Selbstzerstörungsmaschinerie blockieren. Die Gene, die diese Proteine codieren, heißen BIRC‑Gene. In vielen Krebsarten sind IAPs überexprimiert und helfen den Tumorzellen, Todessignale zu ignorieren und weiter zu wachsen. Die Forschenden konzentrierten sich auf mehrere Mitglieder dieser Familie, darunter BIRC2 und BIRC3, sowie auf verwandte Gene, die den Zelltod fördern oder hemmen, um zu untersuchen, wie aktiv sie in aggressiven Hirntumoren bei Kindern sind.
Untersuchung echter Tumoren von jungen Patient:innen
Das Team analysierte Tumorproben von 26 jungen Menschen, alle behandelt an einem pädiatrischen Neuro‑Onkologie‑Zentrum und alle mit der aggressivsten Form des Glioms diagnostiziert. Aus konserviertem Gewebe, das während der Operation entnommen worden war, maßen sie die Aktivität mehrerer Gene, die mit Zellüberleben und ‑tod verbunden sind, etwa BIRC2, BIRC3, BIRC5, BIRC6, BIRC7, NAIP, XIAP, DIABLO, XAF1, CASP3 und CASP9. Zudem verglichen sie diese molekularen Befunde mit klinischen Merkmalen: wie lange jede Patient:in lebte, wie lange die Krankheit stabil blieb, bevor sie sich verschlechterte, und dem Vorhandensein gängiger Tumormarker wie Ki‑67 (ein Wachstumsindikator), PD‑1 (ein Immun‑Checkpoint), Olig2, p53, GFAP und einem kleinen regulatorischen RNA‑Molekül namens miR‑155‑5p.
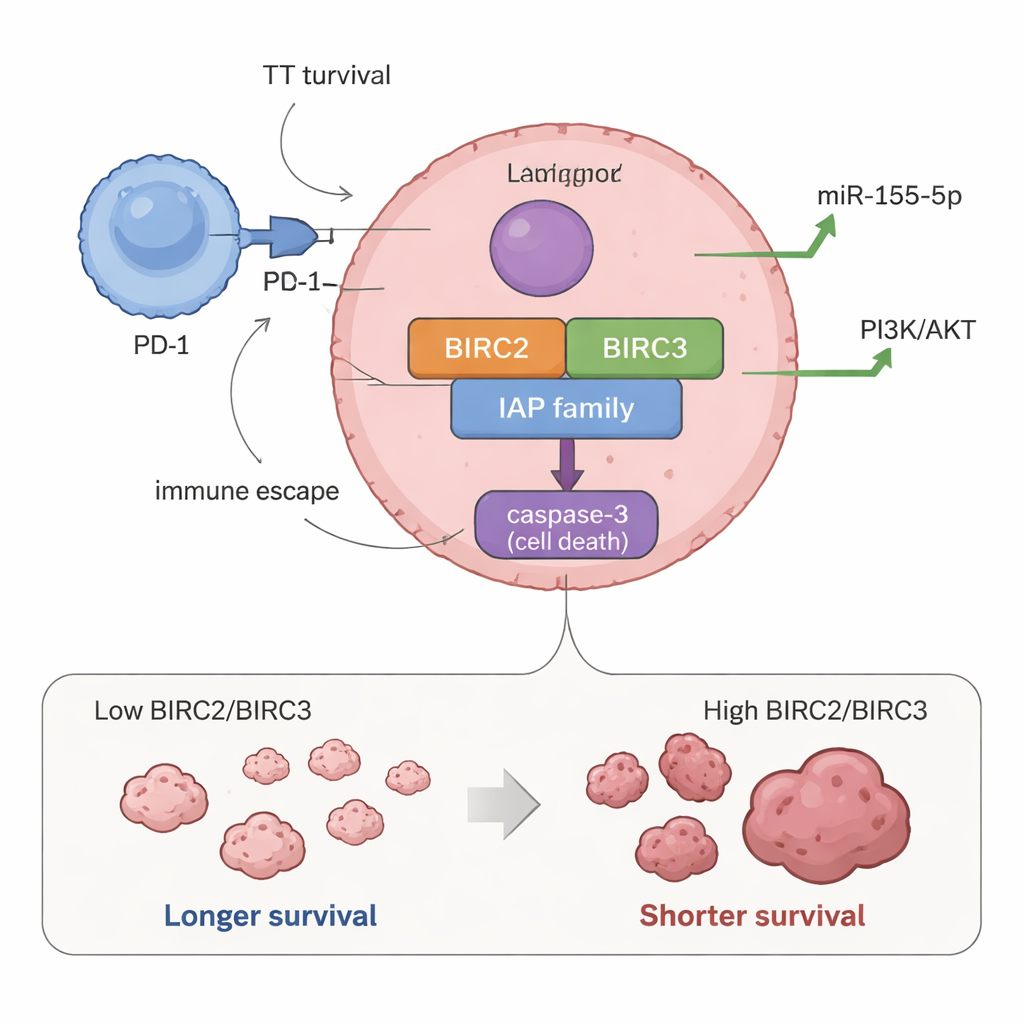
Überlebensschalter, die mit kürzerem Leben verbunden sind
Beim Vergleich der Genaktivität mit den Patientenergebnissen traten zwei Gene besonders hervor. Kinder, deren Tumoren höhere Werte von BIRC2 und BIRC3 aufwiesen, hatten tendenziell eine kürzere Gesamtüberlebenszeit und kürzere Zeitspannen ohne Tumorprogression. Anders ausgedrückt: Wenn diese „Nicht‑Sterben“‑Schalter stärker eingeschaltet waren, verhielt sich die Erkrankung aggressiver. Tumoren mit hohem BIRC2‑ und BIRC3‑Spiegel standen außerdem im Zusammenhang mit erhöhten Werten von miR‑155‑5p, einer kleinen RNA, die zuvor gezeigt wurde, dass sie Zellen zum Wachstum treibt und vom Zelltod weglenkt — was darauf hindeutet, dass diese Moleküle gemeinsam Tumoren gegen Therapien widerstandsfähiger machen könnten.
Verbindungen zu Tumorwachstum und Immunflucht
Die Studie untersuchte auch, wie diese Überlebensschalter in das breitere Tumorumfeld eingebettet sind. Überraschenderweise waren einige Gene, die den Zelltod fördern oder regulieren können, wie NAIP, BIRC3 und XAF1, in Tumoren mit fehlendem Proliferationsmarker Ki‑67 stärker aktiv, was auf ein komplexes Gleichgewicht zwischen Wachstums‑ und Todes‑Signalen hinweist. Höhere BIRC3‑ und XAF1‑Werte traten tendenziell in Tumoren mit mehr PD‑1 auf, einem wichtigen immunologischen „Bremsmechanismus“, der dem Krebs hilft, sich vor der Abwehr des Körpers zu verbergen. Außerdem war eine erhöhte Aktivität von CASP3, einem zentralen Vollstrecker des Zelltods, stark mit PD‑1‑Expression assoziiert, was nahelegt, dass Wechselwirkungen zwischen Krebs‑ und Immunzellen die Nutzung oder Blockade der Todesmechanik innerhalb des Tumors umgestalten könnten.
Was das für künftige Behandlungen bedeuten könnte
Für Familien und Kliniker:innen, die sich pädiatrischen hochgradigen Gliomen gegenübersehen, ändern diese Befunde die Therapie noch nicht, liefern aber wichtige Hinweise. Die Arbeit legt nahe, dass insbesondere eine hohe Aktivität des Gens BIRC2, möglicherweise auch von BIRC3, Tumoren kennzeichnet, die widerstandsfähiger sind und eher schnell zurückkehren — was diese Gene zu potenziellen Warnzeichen für eine ungünstige Prognose macht. Da IAP‑Proteine bereits als Wirkstoffziele bei Krebserkrankungen Erwachsener untersucht werden, werfen die neuen Ergebnisse die Möglichkeit auf, dass Medikamente, die diese Überlebensschalter ausschalten, eines Tages mit bestehenden Hirntumortherapien oder mit Immuntherapien gegen PD‑1 kombiniert werden könnten. Die Studie ist klein und explorativ, daher müssen die Schlussfolgerungen in größeren Kohorten und auf Proteinebene bestätigt werden, aber sie weist in Richtung einer Zukunft, in der Tumoren von Kindern auf diese Schlüsselschalter profiliert werden könnten, um Prognosen zu verbessern und schließlich individuellere und wirksamere Therapien zu steuern.
Zitation: Petniak, A., Gil-Kulik, P., Zarychta, J. et al. Reduced expression of BIRC2 and BIRC3 associated with longer survival in pediatric high-grade gliomas. Sci Rep 16, 6665 (2026). https://doi.org/10.1038/s41598-026-35887-7
Schlüsselwörter: pädiatrischer Hirntumor, Gliom, Apoptose, BIRC2 BIRC3, Immuntherapie