Clear Sky Science · de
KIN17 fördert den Beginn und das Fortschreiten von Nierentumoren über den PI3K‑AKT‑mTOR‑Signalweg
Warum diese Nierenkrebsstudie wichtig ist
Nierenkrebs wird zunehmend häufiger entdeckt, doch für viele Patientinnen und Patienten bleibt die Krankheit schwer beherrschbar, sobald sie streut. Diese Studie blickt mit Mikroskopie auf die Ebene einzelner Moleküle in Krebszellen, um zu verstehen, was das Wachstum und die Invasion von Nierentumoren antreibt und ob ein experimenteller Wirkstoff diesen Prozess bremsen kann. Die Ergebnisse lenken die Aufmerksamkeit auf ein wenig bekanntes Protein, KIN17, als neuen Übeltäter beim Nierenkrebs und deuten einen Weg an, es indirekt mit einer Tablettenbehandlung anzugreifen.
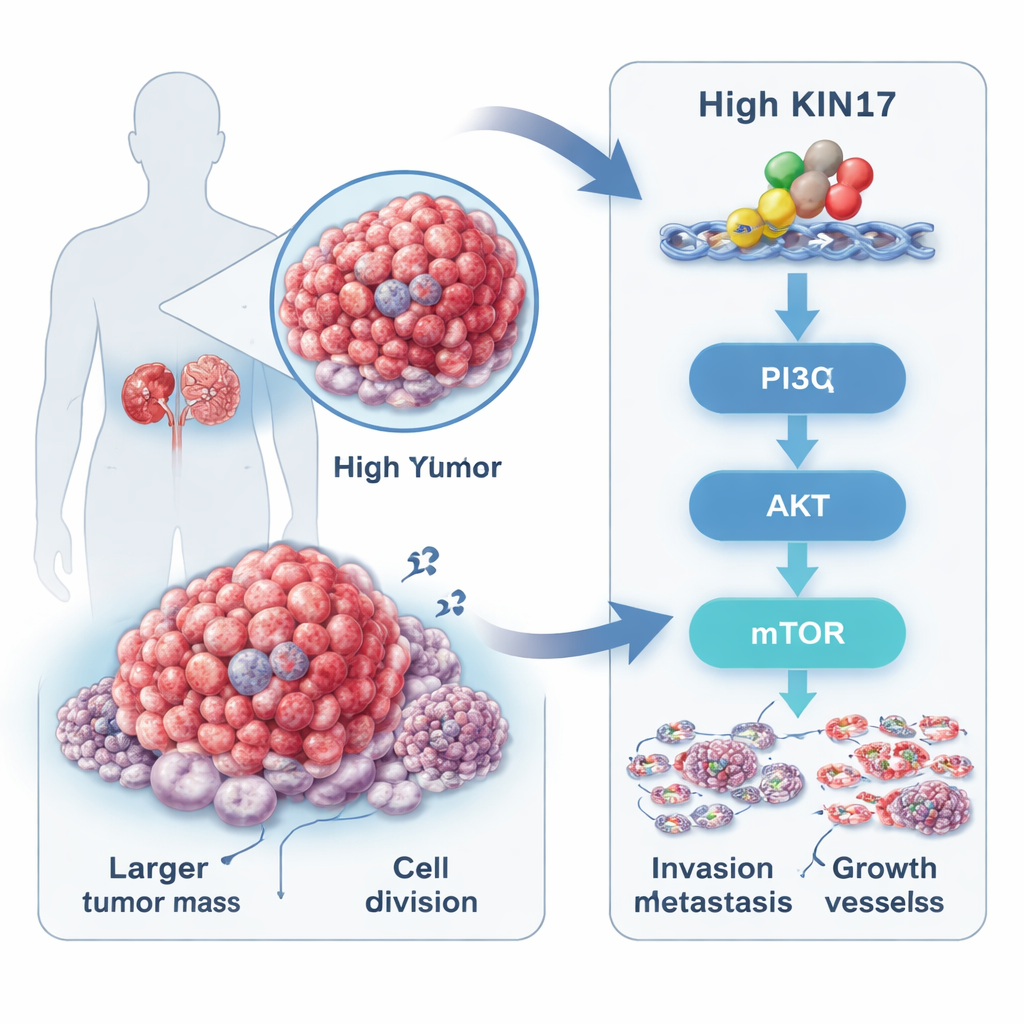
Ein verborgener Treiber in Nierentumoren
Das Nierenzellkarzinom, die häufigste Form von Nierenkrebs, beginnt oft ohne Symptome und wird häufig spät entdeckt. Die Forscherinnen und Forscher konzentrierten sich auf ein Protein namens KIN17, das lange für seine Rolle beim Schutz und bei der Replikation von DNA bekannt war, aber erst kürzlich mit mehreren anderen Krebsarten in Verbindung gebracht wurde. Durch die Analyse öffentlicher Krebsdatenbanken und Tumorproben von 88 Patientinnen und Patienten stellten sie fest, dass die KIN17‑Spiegel in Nierentumoren deutlich höher waren als im umliegenden nicht‑tumorösen Gewebe. Patientinnen und Patienten mit höherem KIN17 in ihren Tumoren hatten tendenziell größere Tumoren, höhergradige Erkrankungen, fortgeschrittenere Stadien und mehr Fernmetastasen und überlebten kürzer als solche mit niedrigem KIN17. Dieses Muster deutete darauf hin, dass KIN17 nicht nur ein Zuschauer ist, sondern eng mit der Aggressivität eines Tumors verknüpft ist.
KIN17 an Krebszellen getestet
Um herauszufinden, was KIN17 tatsächlich in Nierenkrebszellen bewirkt, veränderte das Team Laborzelllinien so, dass KIN17 entweder heruntergeregelt oder überexprimiert wurde. Bei Reduktion von KIN17 teilten sich die Zellen langsamer, bildeten weniger Kolonien und waren weniger beweglich und invasiv durch künstliche Membranen. Mehr dieser Zellen blieben in der Ruhephase des Zellzyklus stecken und gingen vermehrt zugrunde; es wurden höhere Werte programmierter Zellsterblichkeit festgestellt. Das Gegenteil zeigte sich bei Überproduktion von KIN17: Die Zellen vermehrten sich schneller, kopierten ihre DNA aktiver, schlossen kratzartige Lücken in Zellschichten schneller und drangen aggressiver vor. Diese Experimente zeigten, dass KIN17 wie ein Gaspedal für Wachstum und Ausbreitung von Nierenkrebszellen wirkt.
Ein Wachstumsweg wird auf frischer Tat ertappt
Die Forscherinnen und Forscher fragten als Nächstes, wie KIN17 diese Wirkung ausübt. Ihre Genaktivitätsanalysen und Proteinuntersuchungen wiesen auf ein bekanntes Netzwerk für Wachstum und Überleben in Zellen hin: den PI3K–AKT–mTOR‑Signalweg. Dieser Weg wird oft mit einem zentralen Steuerzentrum verglichen, das Zellen sagt, wann sie wachsen, sich teilen und dem Tod entgehen sollen. Nierenkrebszellen mit hohem KIN17 zeigten stärkere „An“-Signale — chemische Markierungen, sogenannte Phosphatgruppen — an Schlüsselkomponenten dieses Weges, obwohl die Gesamtmenge dieser Proteine unverändert blieb. Bei Herunterregulierung von KIN17 fielen diese Aktivierungsmarkierungen ab, und auch Moleküle, die mit Zellbewegung und Invasion verbunden sind, veränderten sich. In Mäuseexperimenten wuchsen aus KIN17‑reichen Zellen erzeugte Tumoren größer und schneller, und Gewebefärbungen zeigten, dass derselbe Wachstumsweg in diesen Tumoren stark aktiviert war.
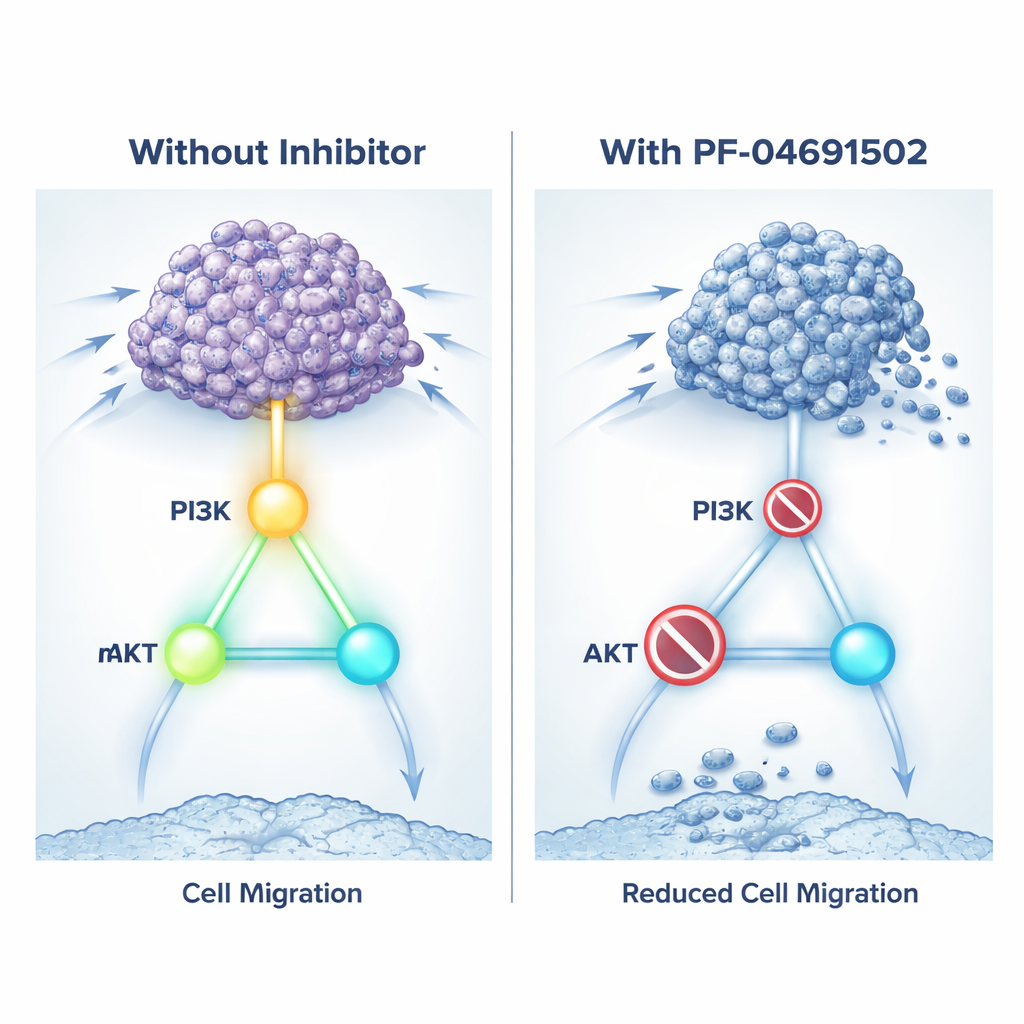
Das Signal mit einem Dual‑Wirkstoff dämpfen
Da eine direkte Blockade von KIN17 mit bestehenden Medikamenten noch nicht möglich ist, testete das Team einen anderen Ansatz: das Abschalten des Wachstumswegs, den KIN17 offenbar steuert. Sie verwendeten PF‑04691502, einen experimentellen Wirkstoff, der sowohl PI3K als auch mTOR hemmt — zwei zentrale Schalter des Weges. In Zellkulturen verlangsamte die Behandlung KIN17‑reicher Nierenkrebszellen deren Wachstum, reduzierte ihre Wanderfähigkeit und Koloniebildung und trieb mehr Zellen in den Tod. Der Wirkstoff verringerte zudem die Aktivierungsmarkierungen auf PI3K, AKT und mTOR und senkte die Spiegel invasionsassoziierter Proteine. Bei Mäusen mit Nierentumoren verkleinerte eine tägliche Gabe von PF‑04691502 Tumoren mit KIN17‑Überproduktion und reduzierte Marker der Zellteilung, während Signale des Zellsterbens zunahmen. Im Wesentlichen konnte der Wirkstoff die schädlichen Effekte von KIN17 abschwächen, indem er dessen bevorzugten Wachstumsweg stilllegte.
Was das für Patientinnen und Patienten bedeuten könnte
Für Menschen mit Nierenkrebs legen diese Befunde zwei hoffnungsvolle Ideen nahe. Erstens könnte die Messung von KIN17 in Tumorproben Ärzten helfen einzuschätzen, wie aggressiv ein Tumor ist und wie wahrscheinlich eine Streuung ist. Zweitens könnten Tumoren, die stark von KIN17 abhängig sind, besonders anfällig für Wirkstoffe sein, die den PI3K–AKT–mTOR‑Weg treffen, wie PF‑04691502 oder ähnliche Dual‑Inhibitoren, die bereits in klinischen Studien für andere Krebsarten untersucht werden. Obwohl noch viel Arbeit nötig ist, bevor eine neue Therapie in die Klinik gelangt, zeichnet diese Studie eine klare Ereigniskette nach — von KIN17 über einen Schlüssel‑Wachstumsweg bis hin zur unkontrollierten Tumorausbreitung — und zeigt, dass das Durchbrechen dieser Kette Nierenkrebs im Labor und in Tiermodellen verlangsamen kann.
Zitation: Wen, Y., Lyu, L., Zhang, H. et al. KIN17 facilitates the initiation and progression of renal tumor progression through the PI3K-AKT-mTOR pathway. Sci Rep 16, 5721 (2026). https://doi.org/10.1038/s41598-026-35851-5
Schlüsselwörter: Nierenzellkarzinom, KIN17, PI3K AKT mTOR, zielgerichtete Therapie, PF-04691502