Clear Sky Science · de
Proteinbestand von extrazellulären Vesikeln von Patient*innen mit fortgeschrittenem Melanom verändert sich beim Fortschreiten unter Anti‑PD1‑Therapie
Warum winzige Boten im Blut den Erfolg einer Krebsbehandlung vorhersagen könnten
Bei Menschen mit fortgeschrittenem Melanom können leistungsfähige neue Immuntherapien manchmal dazu führen, dass Tumoren zurückgehen – in vielen Fällen jedoch wehrt sich der Krebs schnell. In dieser Studie werden mikroskopische "Pakete", die Tumoren ins Blut abgeben, untersucht, um zu prüfen, ob sie frühzeitig und ohne Biopsie verraten können, wer von einer Anti‑PD1‑Behandlung profitieren wird und wer eine andere Strategie benötigen könnte.
Kleine Bläschen mit großen Hinweisen
Unser Blut enthält zahllose nanoskalige Bläschen, so genannte extrazelluläre Vesikel. Dabei handelt es sich um winzige, membranumhüllte Päckchen, die Zellen nutzen, um molekulare Botschaften zu verschicken. Krebszellen schleudern diese Vesikel ebenfalls aus und füllen sie mit Proteinen, die widerspiegeln, was im Tumor und seiner Umgebung vor sich geht. Da diese Vesikel frei zirkulieren, lassen sie sich aus einer einfachen Blutprobe fischen, statt in einen Tumor hineinschneiden zu müssen. Die Forschenden fragten, ob die Proteinfracht dieser Vesikel bei Patient*innen mit fortgeschrittenem Melanom bereits im Vorfeld anzeigen könnte, wie gut jemand auf die Anti‑PD1‑Immuntherapie reagieren würde – eine weit verbreitete Wirkstoffklasse, die die "Bremsen" der Immunzellen löst.
Patient*innen während der Behandlung verfolgen
Das Team untersuchte neun Personen mit fortgeschrittenem Melanom, die alle Anti‑PD1‑Präparate erhielten. Blutproben wurden zu drei Zeitpunkten entnommen: vor Beginn der Behandlung, kurz nach der ersten Dosis und entweder bei Krankheitsprogression oder neun Monate später, falls keine Progression eingetreten war. Aus jeder Probe isolierten die Wissenschaftler*innen extrazelluläre Vesikel und verwendeten hochauflösende Massenspektrometrie, um deren Proteingehalt zu katalogisieren. Nach sorgfältiger Datenfilterung konzentrierten sie sich auf 969 zuverlässig gemessene Proteine. Diese Proteine gruppierten sie dann in Netzwerke, die wichtige biologische Prozesse repräsentieren – etwa Immunaktivität, Zell‑Adhäsion, Blutgerinnung und Energiestoffwechsel – und untersuchten, wie sich diese Muster zwischen Patient*innen mit kontrollierter Erkrankung und solchen mit weiter wachsendem Tumor unterschieden.
Frühe Hinweise auf Ansprechen in Proteinmustern verborgen
Bereits vor Behandlungsbeginn unterschieden sich die Vesikel in späteren Ansprechern von denen der Nicht‑Ansprecher. Patient*innen, denen es später besser ging, hatten tendenziell Vesikel, die angereichert waren an Proteinen, die mit Zell‑zu‑Zell‑Kontakten und bestimmten schützenden Reaktionen auf UV‑Licht zusammenhängen – ein entscheidender Faktor bei Hautkrebs. Im Gegensatz dazu waren einige immunbezogene Proteine und Entzündungsmarker bei jenen häufiger, die später eine Progression zeigten, was darauf hindeutet, dass eine "heiße, aber fehlgeleitete" Immunumgebung den Nutzen der Therapie mindern könnte. Indem sie einzelne Moleküle betrachteten, entwickelten die Forschenden eine Signatur aus acht Proteinen – im Wesentlichen eine gewichtete Kombination von Proteinniveaus –, die Patient*innen in Hoch‑ und Niedrigrisiko‑Gruppen für ein früheres Fortschreiten einteilte. In dieser kleinen Kohorte konnte diese Signatur die Gruppen mit vielversprechender Genauigkeit unterscheiden.
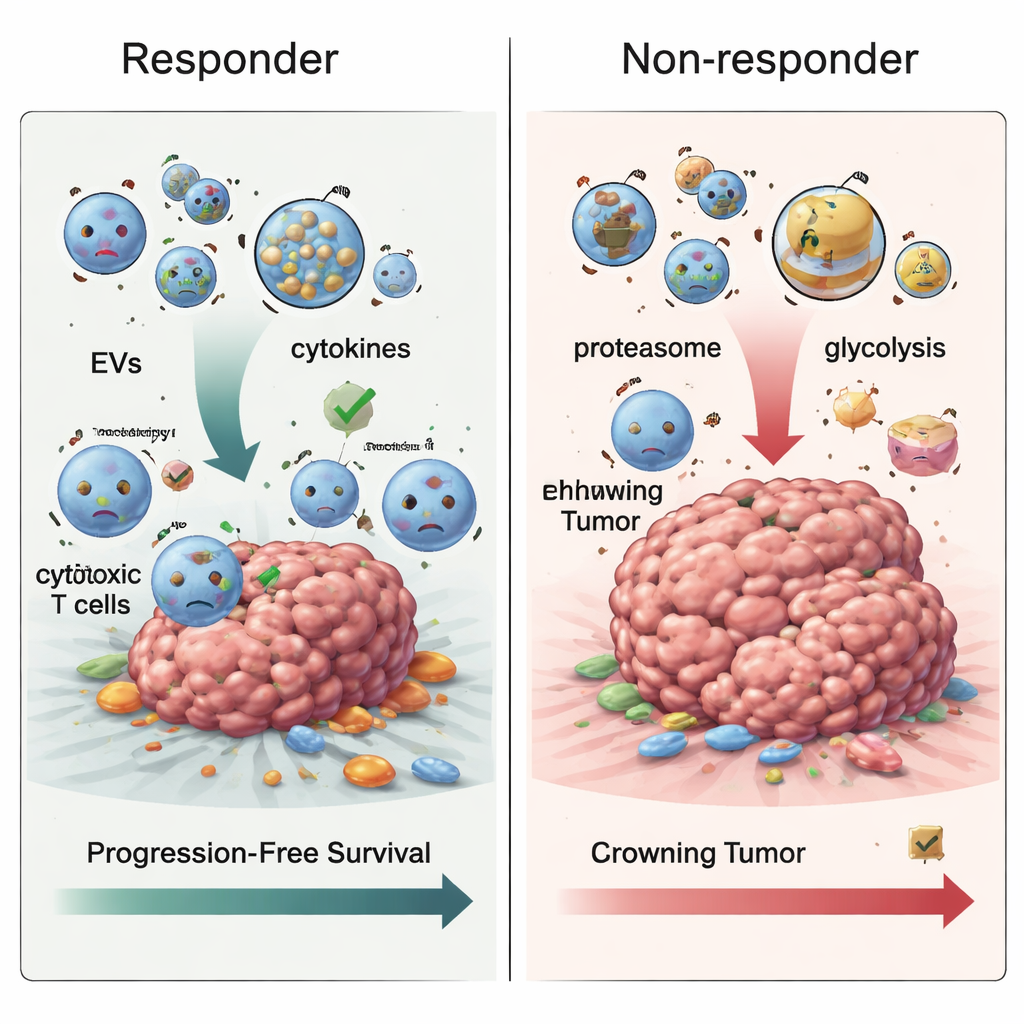
Wie sich Resistenz im Laufe der Zeit entwickeln könnte
Als das Team Proben untersuchte, die nach Beginn der Behandlung entnommen wurden, zeigte sich ein weiteres Muster. Bei Patient*innen mit progressivem Melanom reicherte sich in den extrazellulären Vesikeln vermehrt Proteinmaterial an, das zur zellulären Abfallentsorgung gehört – dem Proteasom – sowie Proteine aus energieerzeugenden Wegen wie der Glykolyse, dem Zuckerabbauprozess, auf den viele Tumoren angewiesen sind. Diese Veränderungen passen zu der Idee, dass resistente Tumoren ihren Stoffwechsel und die Proteinverarbeitung umstellen, um dem Immunangriff zu widerstehen. Betrachte man alle drei Zeitpunkte zusammen, beobachteten die Forschenden außerdem, dass Proteine, die mit der Blutgerinnung verknüpft sind, bei Nicht‑Ansprechern im Zeitverlauf tendenziell abnahmen, während Proteine, die an der Präsentation von Tumorfragmenten an das Immunsystem beteiligt sind, zunahmen – paradoxerweise mündete dies jedoch nicht in einer besseren Tumorkontrolle, was darauf hindeutet, dass die Art und Weise, wie diese Signale in Vesikeln verpackt sind, die effektive Immunabwehr behindern könnte.
Was das für Patient*innen bedeuten könnte
Einfach ausgedrückt deutet die Studie darauf hin, dass winzige Bläschen im Blutstrom einen detaillierten molekularen Fingerabdruck darüber tragen, wie Melanomtumoren und das Immunsystem unter Anti‑PD1‑Therapie interagieren. Bestimmte Proteinmuster in diesen Vesikeln – gemessen vor und während der Behandlung – könnten Ärzten helfen vorherzusagen, wer voraussichtlich länger eine Krankheitskontrolle hat und wer möglicherweise eine durch Entzündung und veränderten Stoffwechsel getriebene Resistenz entwickelt. Obwohl die Arbeit nur auf neun Patient*innen beruht und in größeren Kohorten bestätigt werden muss, weist sie auf eine Zukunft hin, in der eine routinemäßige Blutentnahme die Immuntherapie beim Melanom steuern und anpassen könnte, damit diese starken Medikamente präziser und wirksamer eingesetzt werden.
Zitation: Trilla-Fuertes, L., Gámez-Pozo, A., Laso-García, F. et al. Protein content of extracellular vesicles from patients with advanced melanoma changes upon progression to anti-PD1 therapy. Sci Rep 16, 5891 (2026). https://doi.org/10.1038/s41598-026-35848-0
Schlüsselwörter: Melanom‑Immuntherapie, extrazelluläre Vesikel, Blut‑Biomarker, Anti‑PD1‑Resistenz, Proteomik