Clear Sky Science · de
Erkennung der Sichelzellenanämie unter ressourcenarmen Bedingungen mit Transfer-Learning und Contrastive-Learning gekoppelt mit XAI
Warum intelligentere Bluttests wichtig sind
Die Sichelzellenanämie ist eine lebenslange Bluterkrankung, die starke Schmerzen, Infektionen und vorzeitigen Tod verursachen kann, insbesondere in Teilen Afrikas und Indiens, wo medizinische Ressourcen knapp sind. Eine frühe Diagnose kann Leben retten, doch traditionelle Tests erfordern geschultes Personal, spezialisierte Geräte und Zeit, die vielen Kliniken schlicht fehlt. Diese Arbeit untersucht, wie künstliche Intelligenz (KI) einfache Mikroskopbilder von Blut in schnelle, verlässliche Screening-Tools verwandeln kann, sodass sich die Sichelzellenanämie auch in ressourcenarmen Umgebungen leichter erkennen lässt.
Ein genauerer Blick auf eine gefährliche Bluterkrankung
Bei der Sichelzellenanämie führt eine kleine Veränderung im Gen für Hämoglobin—the Protein, das Sauerstoff transportiert—dazu, dass rote Blutkörperchen zu steifen, sichel- oder halbmondförmigen Formen verformen, statt weich und rund zu bleiben. Diese verformten Zellen können winzige Blutgefäße verstopfen, den Blutfluss blockieren und Organe schädigen. 
Von überlasteten Laboren zu KI-Helfern
Traditionelle Methoden zur Bestätigung der Sichelzellenanämie — wie Hämoglobinelektrophorese oder genetische Tests — sind zwar genau, aber oft teuer, geräteintensiv und langsam. Demgegenüber verfügen viele Kliniken bereits über einfache Mikroskope, und moderne Kameras können hochaufgelöste Bilder von Blutausstrichen aufnehmen. Die Autoren bauen auf dieser Realität auf: Anstatt die Blutentnahme zu ändern, verändern sie die Bildanalyse. Sie geben digitalisierte Blutausstrichbilder in KI-Modelle, die bereits aus Millionen von Alltagsfotografien Muster gelernt haben, und feinabstimmen diese Modelle anschließend darauf, normale rote Blutkörperchen von sichelförmigen zu unterscheiden. Diese Wiederverwendung von Vorwissen, Transfer-Learning genannt, ist entscheidend, wenn nur wenige hundert medizinische Bilder für das Training zur Verfügung stehen.
Maschinen das Unterscheiden feiner Formen beibringen
Nicht alle KI-Trainingsmethoden sind gleich, besonders bei begrenzten Daten. Die Forscher vergleichen drei populäre Bildvernetzungsarchitekturen — ResNet-50, DenseNet-121 und EfficientNet-B0 — und drei Trainingsansätze. Zwei der Trainingsmethoden behandeln das Problem als einfache Ja‑/Nein‑Frage (Sichelzelle oder nicht) und versuchen, die rohe Klassifikationsgenauigkeit zu verbessern. Die dritte, Triplet Loss genannt, bringt dem Netzwerk stattdessen bei, Bilder in einem „Formraum“ anzuordnen, in dem Bilder von Sichelzellen zusammenclustern und sich von Bildern normaler Zellen abgrenzen. Dieses kontrastorientierte Training macht das Modell zu einem Spezialisten für kleine, formbasierte Unterschiede — genau das, was in der Sichelzellenmikroskopie zählt.
Den Entscheidungsprozess sichtbar machen
Ärztinnen, Ärzte und Laborpersonal müssen einem automatisierten System vertrauen können, das die Patientenversorgung beeinflusst. Um die KI-„Blackbox“ zu öffnen, verwenden die Autoren eine erklärbare-KI-Methode namens Grad-CAM, die eine Heatmap über das originale Mikroskopbild legt, um zu zeigen, welche Bereiche die Entscheidung am stärksten beeinflusst haben. 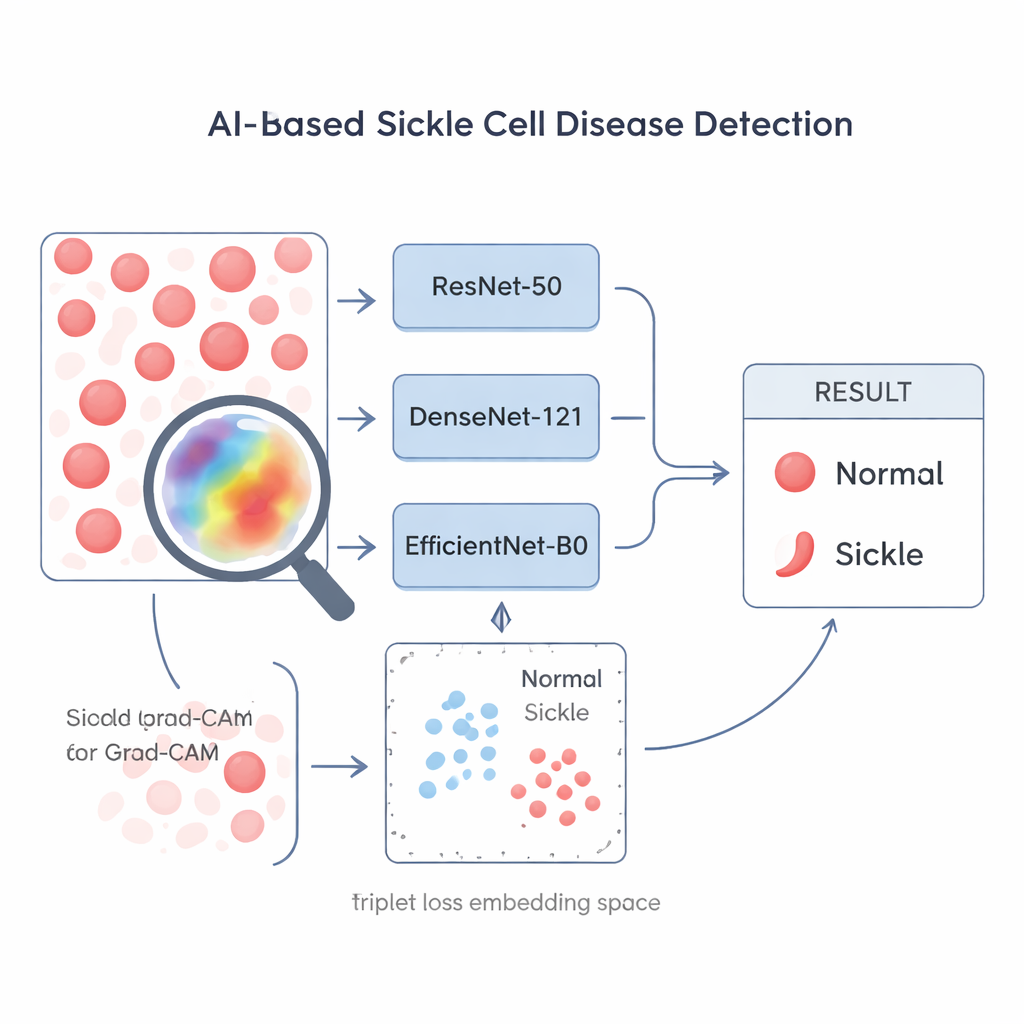
Von der Forschung in die reale Klinik
Die Studie kommt zu dem Schluss, dass die intelligente Wiederverwendung vorhandener Bilderkennungsnetzwerke, kombiniert mit Triplet-Loss-Training und visuellen Erklärungen, eine genaue und transparente Erkennung der Sichelzellenanämie aus relativ wenigen Bildern ermöglichen kann. Kurz gesagt: Ein Standardmikroskop plus Kamera und Laptop könnte Erstlinieneinrichtungen dabei helfen, Patienten, die wahrscheinlich an Sichelzellenanämie leiden, schnell zu identifizieren — auch ohne umfassende Labortests. Größere und vielfältigere Datensätze werden zwar weiterhin nötig sein, bevor solche Werkzeuge breit eingesetzt werden, doch diese Arbeit zeigt einen klaren Weg zu kostengünstigem, KI-gestütztem Screening, das insbesondere in Regionen mit hoher Krankheitslast und begrenzten Diagnose-Ressourcen einen echten Unterschied machen könnte.
Zitation: Patel, J., Muralikrishna, H., Chadaga, K. et al. Sickle cell disease detection in low-resource conditions using transfer-learning and contrastive-learning coupled with XAI. Sci Rep 16, 6104 (2026). https://doi.org/10.1038/s41598-026-35831-9
Schlüsselwörter: Sichelzellenanämie, medizinische Bildgebung, Deep Learning, Diagnostik in ressourcenarmen Umgebungen, erklärbare KI