Clear Sky Science · de
Integratives Einzelzell- und Machine-Learning-Framework offenbart prognostische Fibroblasten-Subtypen und erstellt eine fibroblastenbezogene Risikosignatur beim Lungenadenokarzinom
Warum die „helfenden“ Zellen rund um Lungen tumoren wichtig sind
Das Lungenadenokarzinom ist eine der häufigsten und tödlichsten Formen von Lungenkrebs, doch Patienten mit scheinbar ähnlichen Tumoren können sehr unterschiedliche Verläufe und Therapieansprechen zeigen. Diese Studie blickt über die Krebszellen hinaus und konzentriert sich auf die umgebenden „helfenden“ Zellen, die Fibroblasten genannt werden und am Aufbau sowie an der Umgestaltung von Gewebe beteiligt sind. Indem die Forschenden diese Zellen einzeln analysieren und anschließend moderne Rechenmodelle einsetzen, zeigen sie, dass Fibroblasten in unterschiedliche Ausprägungen vorkommen, die vorhersagen können, wie Patientinnen und Patienten abschneiden und wie ihre Tumoren auf moderne Immuntherapien reagieren könnten.
Blick in die Nachbarschaft des Tumors
Mithilfe modernster Einzelzell-RNA-Sequenzierung analysierte das Team mehr als 140.000 einzelne Zellen aus unbehandelten Proben von Lungenadenokarzinomen. Diese Methode erfasst, welche Gene in jeder Zelle aktiv sind, und ermöglicht es den Autoren, den Tumor in seine wichtigsten Bewohner zu unterteilen: Immunzellen, Krebszellen, Gefäßzellen und Fibroblasten. Sie fanden heraus, dass Tumoren stark darin variieren, wie viel von jedem Zelltyp sie enthalten. Manche Tumoren sind mit Immunzellen durchsetzt, andere werden von Fibroblasten und strukturellem Gewebe dominiert. Folgestudien zeigten, dass jeder dieser Zelltypen spezialisierte Aufgaben erfüllt, von der Organisation immunologischer Angriffe bis zum Aufbau des strukturellen Gerüsts des Tumors.
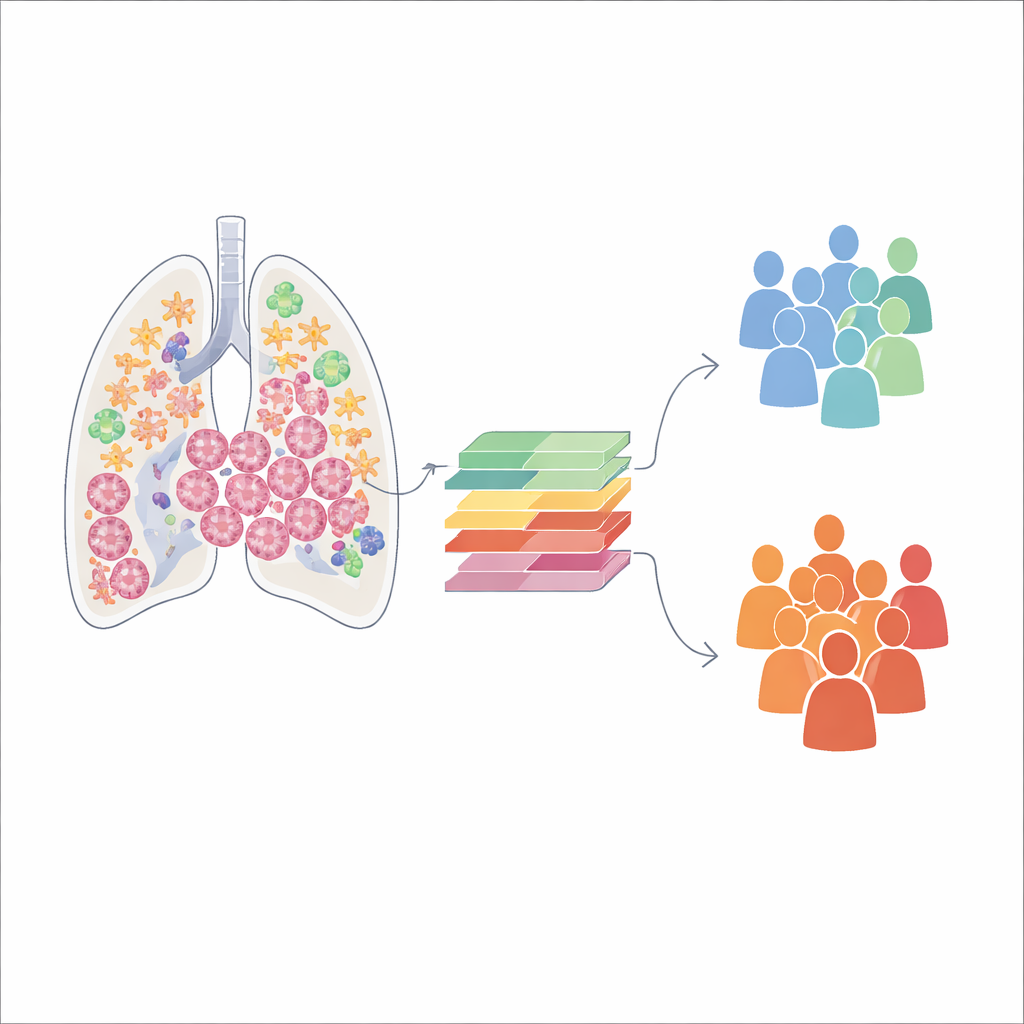
Nicht alle Fibroblasten sind gleich
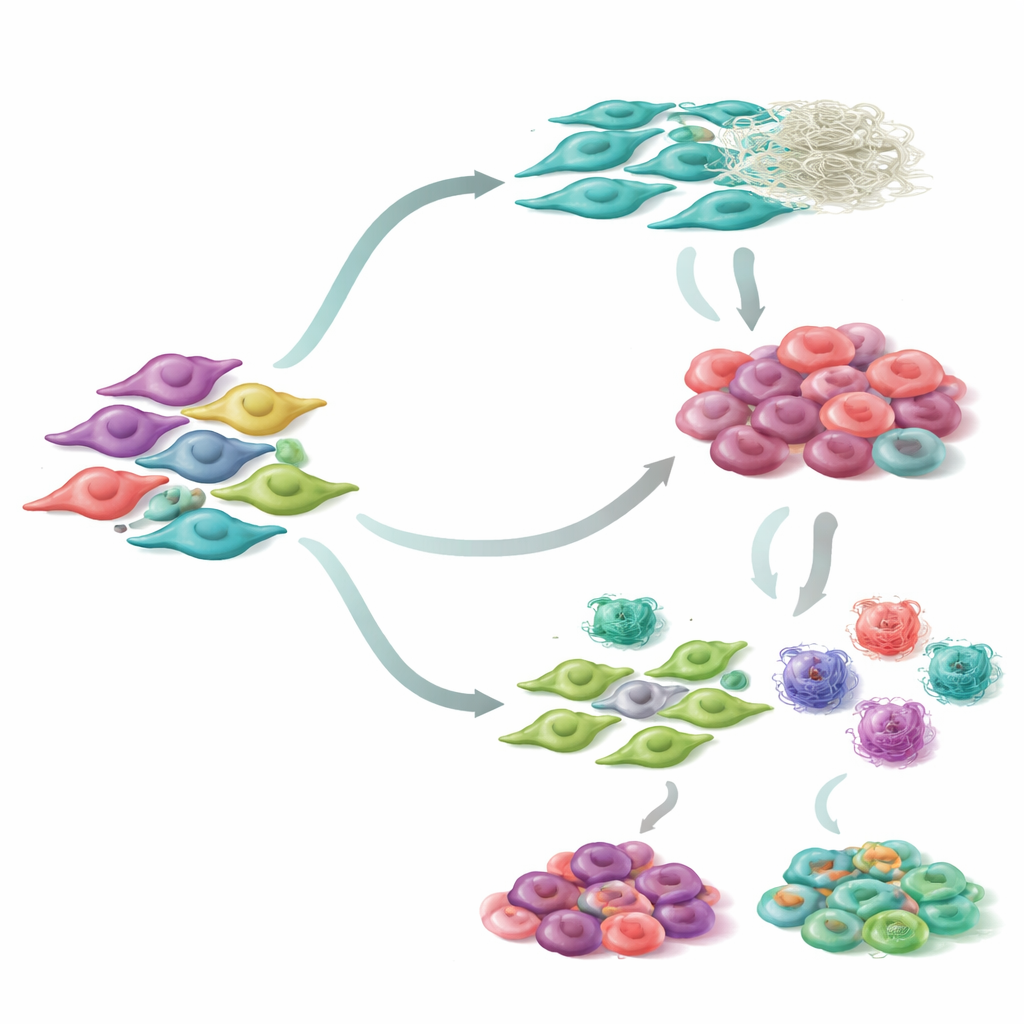
Als sich die Forschenden speziell auf Fibroblasten konzentrierten, entdeckten sie sieben unterschiedliche Fibroblasten-Untergruppen innerhalb von Lungentumoren. Durch die Rekonstruktion, wie sich diese Zellen im Zeitverlauf verändern, identifizierten sie zwei Hauptentwicklungspfade. Entlang des einen Pfads nehmen Fibroblasten schrittweise Merkmale kontraktiler, das Gewebe versteifender Zellen an, die die Umgebung des Tumors umgestalten. Entlang des anderen Pfads engagieren sich Fibroblasten stärker in der Interaktion mit dem Immunsystem, indem sie Immunzellen entweder anlocken oder dämpfen. Jede Untergruppe zeigte charakteristische Muster der Genaktivität und war mit unterschiedlichen biologischen Aufgaben verknüpft, etwa muskelähnlicher Kontraktion, Bewegung oder Immunregulation. Wichtig ist, dass Patientinnen und Patienten, deren Tumoren für bestimmte Fibroblasten-Subtypen angereichert waren, tendenziell länger lebten — das Gemisch der Fibroblasten-Zustände ist also nicht nur eine kuriose Beobachtung, sondern steht in Verbindung mit tatsächlichen klinischen Ergebnissen.
Erstellung eines Risikoscores aus Fibroblasten-Signalen
Um diese biologischen Erkenntnisse in etwas Klinisch Nützliches zu überführen, kombinierten die Forschenden Fibroblasten-Marker aus Einzelzell-Daten mit Bulk-Tumordaten von Hunderten Patientinnen und Patienten aus großen öffentlichen Datenbanken. Anschließend setzten sie zehn verschiedene Machine-Learning-Verfahren ein und testeten 101 Modellkombinationen, um herauszufinden, welche Kombination fibroblastenbezogener Gene das Patientenüberleben am besten vorhersagt. Das erfolgreichste Modell, genannt fibroblastenbezogene Signatur (FRS), verwendet 29 Gene, um jeder Person einen Risikoscore zuzuweisen. In der Hauptdatenmenge und in sechs unabhängigen Kohorten hatten Personen mit hohen FRS-Werten durchweg eine schlechtere Überlebensprognose als solche mit niedrigen Werten. Der FRS blieb zudem ein starker Prädiktor, selbst wenn Alter, Geschlecht und Tumorstadium berücksichtigt wurden, und er verbesserte die Vorhersage, wenn er mit dem standardmäßigen TNM-Staging kombiniert wurde.
Hinweise auf Immunflucht und Therapieansprechen
Da viele Patientinnen und Patienten heute Immuntherapien erhalten, untersuchten die Autoren, ob der fibroblastenbasierte Score Merkmale der immunologischen Tumorumgebung erfasst. Sie fanden, dass Tumoren mit niedrigem FRS eine reichere Infiltration durch krebsbekämpfende Immunzellen wie CD8-T-Zellen und natürliche Killerzellen aufwiesen sowie eine höhere Expression von Genen, die an der Präsentation von Tumorfragmenten für das Immunsystem beteiligt sind. Im Gegensatz dazu zeigten Tumoren mit hohem FRS weniger hilfreiche Immunzellen, einen höheren Anteil an Tumorzellen, mehr genetische Instabilität und Anzeichen von Immunexklusion, das heißt, Immunzellen werden ferngehalten. Simulierte Messgrößen, die das wahrscheinliche Ansprechen auf Checkpoint-Inhibitoren vorhersagen, deuteten darauf hin, dass Patientinnen und Patienten mit niedrigem FRS eher von diesen Therapien profitieren könnten, während Hoch-FRS-Patienten möglicherweise resistenter sind.
Fokussierung auf ein vielversprechendes Zielgen
Unter den Genen, die den FRS ausmachen, hoben die Forschenden eines namens TIMP1 als besonders starken Marker für schlechte Prognose hervor. TIMP1 war in vielen Krebsarten hochreguliert und zeigte insbesondere in Lungenadenokarzinom-Gewebe deutlich erhöhte Spiegel im Vergleich zum angrenzenden normalen Lungengewebe. In Laborversuchen verringerte eine Reduktion von TIMP1 in Lungenkrebszelllinien deren Fähigkeit, durch eine Matrix zu invasieren und neue Kolonien zu bilden, was darauf hindeutet, dass TIMP1 das Tumorwachstum und die Ausbreitung fördert. Diese Ergebnisse machen TIMP1 zu einem Kandidaten für künftige Medikamente, die darauf abzielen, die strukturellen und immunmodulierenden Mechanismen des Tumors zu schwächen.
Was das für Patientinnen und Patienten bedeutet
Diese Arbeit zeigt, dass die unterstützende Zellumgebung um einen Lungentumor, insbesondere die Fibroblasten, wertvolle Informationen darüber enthält, wie sich die Krankheit verhalten wird und wie sie auf Behandlungen reagieren könnte. Durch die Kombination von Einzelzell-Messungen mit Machine Learning entwickelten die Autorinnen und Autoren einen fibroblastenbasierten Risikoscore, der Patientinnen und Patienten in höhere und niedrigere Risikogruppen einteilen und Hinweise darauf geben kann, welche Tumoren eher gegenüber Immuntherapien resistent sind. Zwar sind weitere Tests erforderlich, bevor ein solcher Score die tägliche Versorgung leiten kann, doch die Studie unterstreicht, dass eine effektive Behandlung von Lungenkrebs nicht nur das direkte Bekämpfen der Tumorzellen erfordert, sondern auch das Eindämmen der umgebenden Fibroblasten, die dem Tumor beim Wachsen und Verstecken helfen.
Zitation: Cheng, S., Zhang, H., Mu, Q. et al. Integrative single-cell and machine learning framework reveals prognostic fibroblast subtypes and constructs a fibroblast-related risk signature in lung adenocarcinoma. Sci Rep 16, 7965 (2026). https://doi.org/10.1038/s41598-026-35830-w
Schlüsselwörter: Lungenadenokarzinom, tumorassoziierte Fibroblasten, Einzelzellsequenzierung, Tumormikroumgebung, Ansprechen auf Immuntherapie