Clear Sky Science · de
Gemeinsamkeiten in Genexpressions- und Methylierungsänderungen bei zwei Rattenmodellen der erworbenen Epilepsie
Warum veränderte Gene für Anfälle wichtig sind
Epilepsie betrifft Millionen von Menschen und bei etwa einem Drittel können die verfügbaren Medikamente die Anfälle nicht vollständig kontrollieren. Die meisten Arzneien dämpfen lediglich die elektrischen Stürme im Gehirn, verhindern aber nicht, dass sich Epilepsie überhaupt entwickelt. Diese Studie untersucht, ob anhaltende chemische Markierungen auf der DNA und die Art und Weise, wie Gene ein- oder ausgeschaltet werden, erklären könnten, wie ein gesundes Gehirn epileptisch wird — und ob diese Veränderungen bei verschiedenen Formen der Erkrankung geteilt werden.
Zwei unterschiedliche Wege zur gleichen Erkrankung
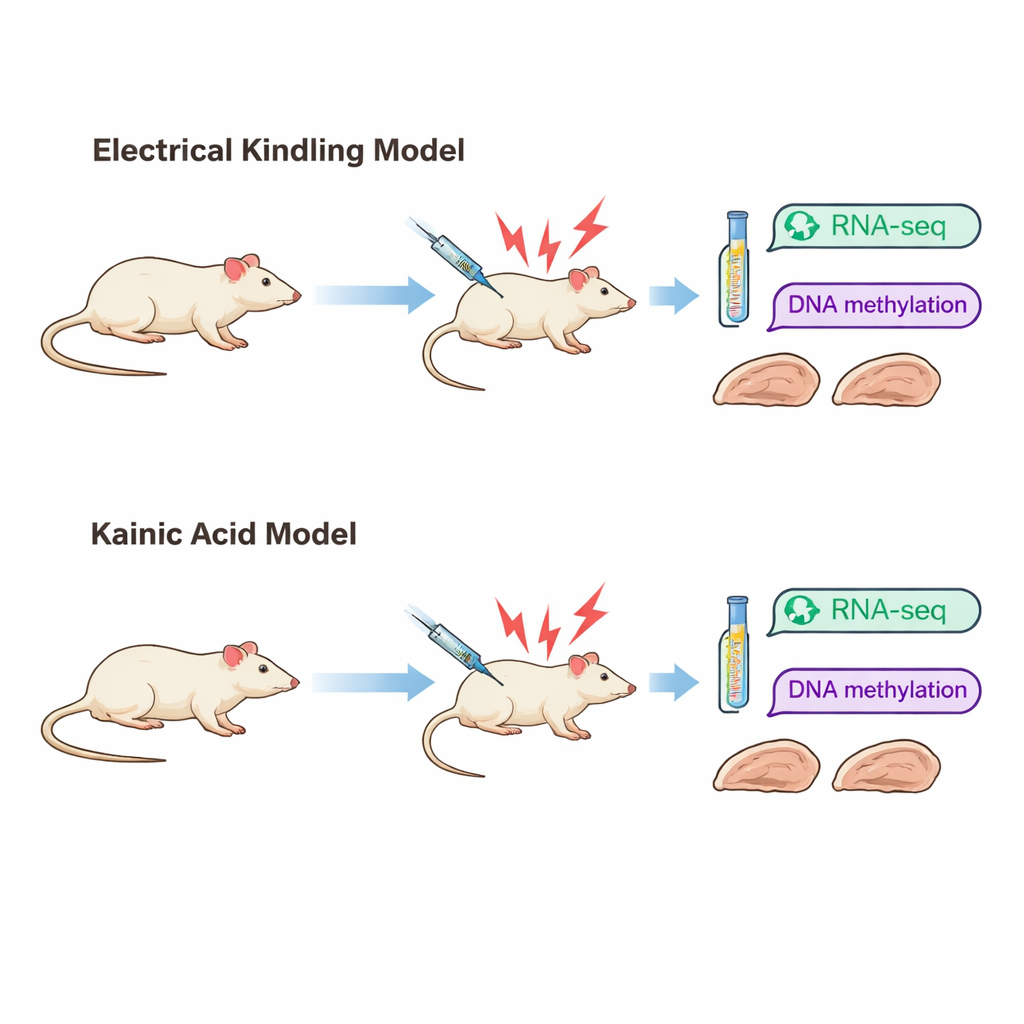
Die Forscher konzentrierten sich auf die temporale Lappenepilepsie, eine häufige Form der Erkrankung, die oft schwer behandelbar ist. Sie verwendeten zwei gut etablierte Rattenmodelle, die verschiedene Entstehungswege der Epilepsie nachbilden. Im „Kindling“-Modell werden über die Zeit kurze elektrische Impulse an einen Teil des Hippocampus abgegeben, bis Anfälle leicht auslösbar sind. Im „Kaininsäure“-Modell löst ein Chemikalikum eine heftige Anfallsphase aus, nach der später spontane Anfälle auftreten. Obwohl beide Modelle letztlich ähnliches äußeres Verhalten erzeugen — schwere krampfartige Anfälle —, sieht der Hirnschaden sehr unterschiedlich aus. Bei den kindling-behandelten Ratten ist die Gewebestruktur weitgehend erhalten, während kaininsäurebehandelte Ratten ausgeprägten Zellverlust und Vernarbung in wichtigen Hippocampusregionen zeigen.
Das genetische Aktivitätsmuster des Gehirns lesen
Um zu sehen, wie diese unterschiedlichen Wege zur Epilepsie das Gehirn auf molekularer Ebene verändern, untersuchte das Team den Hippocampus, nachdem Ratten in jedem Modell drei schwere Anfälle erlebt hatten. Sie maßen, welche Gene stärker oder schwächer aktiv waren, mittels RNA-Sequenzierung, und kartierten chemische Markierungen, sogenannte Methylgruppen auf der DNA, mit einer Methode namens reduced-representation bisulfite sequencing. Veränderungen in der Genaktivität spiegeln wider, wie Zellen reagieren und sich anpassen, während Methylierungsmarken oft als längerfristiges „Gedächtnis“ gesehen werden, das beeinflussen kann, ob Gene ein- oder ausgeschaltet sind.
Genaktivitätsänderungen übertreffen DNA-Marken
Die beiden Modelle zeigten auffallend unterschiedliche Muster der Genaktivität. Im Kindling-Modell veränderten sich mehr als zehnmal so viele Gene wie im Kaininsäure-Modell. Doch als die Forscher die beiden Listen überlappten, fanden sie trotzdem über hundert Gene, die sich in beiden Modellen veränderten, und die meisten davon bewegten sich in dieselbe Richtung. Ein Beispiel ist Mmp9, ein Gen, das mit der Umgestaltung neuronaler Verbindungen und mit anfallsbedingten Schäden in Verbindung gebracht wird; es war in beiden Modellen stark erhöht. Diese gemeinsamen Veränderungen deuten darauf hin, dass es Kernreaktionen der Genexpression bei der Epileptogenese gibt, selbst wenn der initiale Auslöser und die sichtbaren Hirnschäden unterschiedlich sind.
DNA-Marken erzählen eine andere Geschichte
Wenn das Team die DNA-Methylierung betrachtete, änderte sich das Bild. Beide Modelle zeigten viele Gene mit veränderter Methylierung, und es gab eine beträchtliche Überlappung zwischen ihnen. Allerdings zeigte nur eine überschaubare Teilmenge von Genen sowohl veränderte Methylierung als auch veränderte Aktivität innerhalb desselben Modells, und noch weniger verhielten sich so in beiden Modellen. Bei einigen dieser gemeinsamen Gene, wie Nedd9 und Ptpre, stieg die Expression in beiden Modellen, aber die Richtung der Methylierungsänderung an einzelnen Stellen konnte zwischen den Modellen entgegengesetzt sein. Insgesamt gab es keine einfache Regel, dass „mehr Methylierung weniger Genaktivität bedeutet“ oder umgekehrt. Das legt nahe, dass in diesen Epilepsiemodellen die meisten Verschiebungen in der Genaktivität nicht direkt durch umfangreiche Änderungen der DNA-Methylierung gesteuert werden.
Was das für zukünftige Therapien bedeutet
Für Menschen, die auf bessere Epilepsiebehandlungen hoffen, bringen diese Ergebnisse sowohl Vorsicht als auch Orientierung. Die Arbeit zeigt, dass die genetischen Programme, die während der Entwicklung der Epilepsie eingeschaltet werden, stark modellabhängig sein können und dass die DNA-Methylierung nur ein Teil eines größeren, komplexeren Regulationsbildes ist. Vielversprechende Genkandidaten, die in einem einzelnen Tiermodell identifiziert werden, verallgemeinern möglicherweise nicht und sollten daher in mehreren Modellen getestet werden, bevor man sie in Richtung klinischer Anwendungen beim Menschen vorantreibt. Gleichzeitig könnte die kleine Gruppe von Genen, die sowohl in Expression als auch in Methylierung modellübergreifend verändert sind, besonders robuste Ansatzpunkte für die Entwicklung krankheitsmodifizierender Therapien darstellen, die nicht nur Anfälle dämpfen, sondern verhindern wollen, dass Epilepsie sich etabliert.
Zitation: Purnell, B.S., Hur, J., Ruskin, D. et al. Commonalities in gene expression and methylation changes across two rat models of acquired epilepsy. Sci Rep 16, 5095 (2026). https://doi.org/10.1038/s41598-026-35826-6
Schlüsselwörter: Epileptogenese, DNA-Methylierung, Genexpression, temporale Lappenepilepsie, Rattenmodelle