Clear Sky Science · de
Zelluläre bioenergetische und migratorische Reaktionen humaner Gingivalfibroblasten auf Photobiomodulation mit einem 940-nm-Diodenlaser
Licht zur Unterstützung der Wundheilung im Mund
Wer schon einmal einen Zahn gezogen bekommen oder eine Zahnfleischoperation erlebt hat, weiß, wie unangenehm die Heilung im Mundbereich sein kann. Das Gewebe ist ständig Belastungen durch Kauen, Sprechen und Bakterien ausgesetzt, weshalb alles, was die Reparatur sicher beschleunigen könnte, für Zahnärzte und Patienten von großem Interesse ist. Diese Studie untersuchte, ob ein in der Zahnmedizin verbreiteter Laser, bei sehr geringer Leistung eingesetzt, die Zellen im Zahnfleisch sanft „anleiten“ kann, kräftiger zu arbeiten und sich schneller zu bewegen, während sie verletztes Gewebe wiederaufbauen — ohne sie zu verbrennen oder zu schädigen.
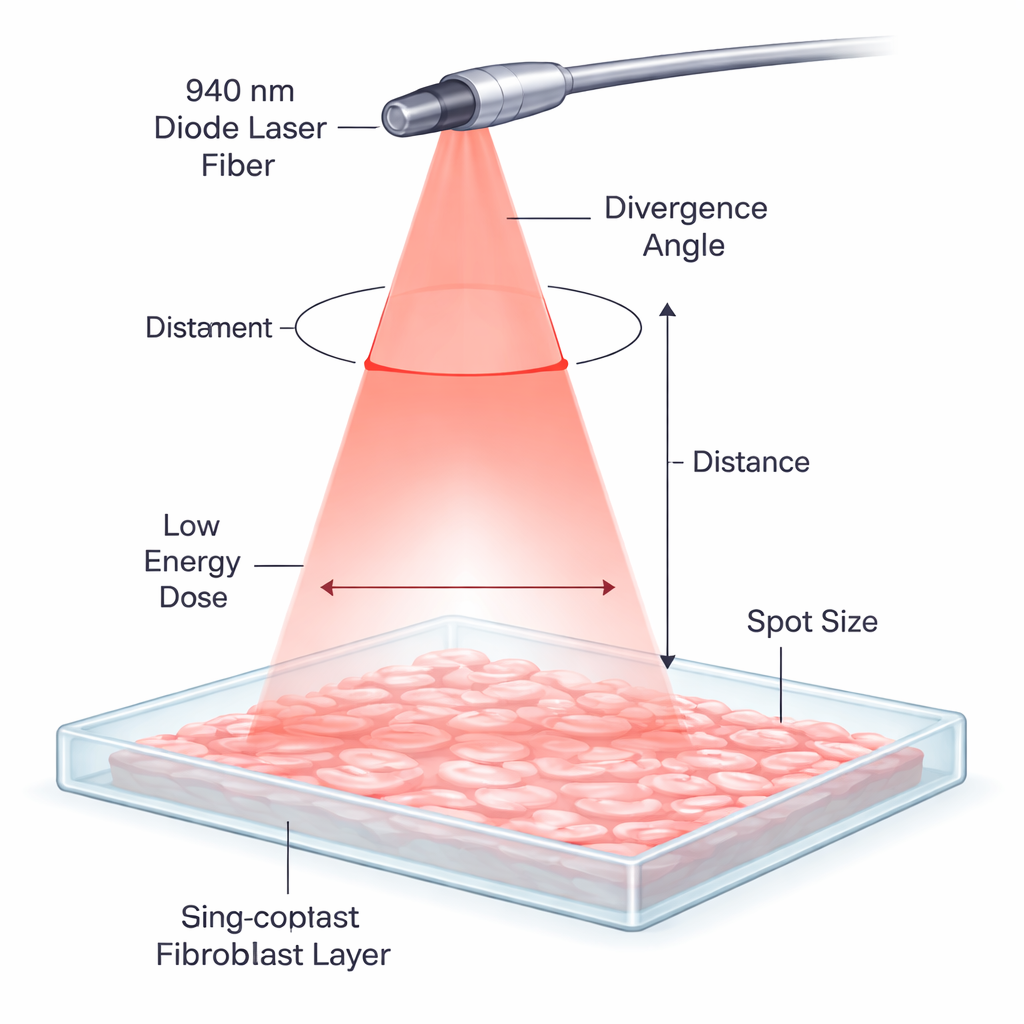
Worin sich ein sanfter Laser von einem schneidenden Laser unterscheidet
In vielen Zahnarztpraxen werden Diodenlaser routinemäßig eingesetzt, um Weichgewebe durch Erzeugung von Wärme zu schneiden oder zu formen. Hier wurde derselbe Typ eines 940-Nanometer-Lasers auf sehr niedrige Leistung eingestellt und ganz anders verwendet. Anstatt das Gewebe zu berühren und zu verbrennen, wurde das Licht für nur eine Sekunde aus kurzer Distanz abgegeben und breitete sich als weicher Kegel über einer dünnen Schicht menschlicher Gingivalzellen aus, die in einer Kulturschale gewachsen waren. Bei diesen niedrigen Dosen geht es nicht ums Schneiden, sondern darum, die interne Zellmaschinerie zu stimulieren — ein Prozess, der als Photobiomodulation bezeichnet wird — damit sie sich effizienter repariert und neu organisiert.
Prüfung von Energiezustand und Sicherheit der Gingivazellen
Die Forschenden konzentrierten sich auf Fibroblasten, die wichtigsten Arbeiterzellen, die die Fasern und die Matrix produzieren, welche dem Zahnfleisch seine Festigkeit verleihen. Kommerziell bezogene humane Gingivalfibroblasten wurden als gleichmäßige Schichten kultiviert und drei unterschiedlichen Energiedosen des 940-nm-Lasers ausgesetzt; eine vierte Gruppe erhielt kein Licht. Das Team maß mehrere Marker: wie stoffwechselaktiv die Zellen waren, ob ihre Außenmembranen beschädigt waren, wie viel zellulärer Brennstoff (ATP) sie produzierten und ob sie Stickstoffmonoxid freisetzten — ein Molekül, das mit Entzündung in Verbindung steht. Über alle Laserdosen zeigten die Zellen keine Anzeichen von Undichtheit oder Verletzung und lösten kein entzündliches Signal aus, was darauf hinweist, dass die kurzzeitige Lichtexposition unter den getesteten Bedingungen sanft und biologisch verträglich war.
Mehr zellulärer „Treibstoff“ und ein Sweet Spot für Bewegung
Obwohl die Zellen in allen Gruppen gesund blieben, änderte sich ihre Energieproduktion dosis- und zeitabhängig. Bei moderaten Lichtstärken erhöhten die Fibroblasten die ATP-Produktion, die universelle Energiewährung der Zellen, um bis zu etwa ein Viertel gegenüber unbehandelten Zellen nach 24 Stunden. Auch ihre allgemeine Stoffwechselaktivität stieg leicht an, besonders bei der höchsten Dosis. Um zu prüfen, ob diese zusätzliche Energie in ein besseres Reparaturverhalten übersetzt wurde, erzeugten die Forschenden einen geraden „Kratz“ in der Zellschicht und verwendeten digitale holographische Bildgebung, um zu beobachten, wie schnell die Zellen zur Schließung der Lücke hineinkrabbten. Sie fanden heraus, dass eine niedrigere Laserdosis die Migrationsgeschwindigkeit leicht erhöhte und zur schnellsten Verschlussrate führte, während die höchste Dosis die Bewegung tatsächlich verlangsamte und den Verschluss verzögerte, obwohl die Energielevels weiterhin erhöht waren. Dieses Muster, bei dem eine geringe Stimulation hilft, zu viel aber zu hemmen beginnt, ist als biphasische Reaktion bekannt.
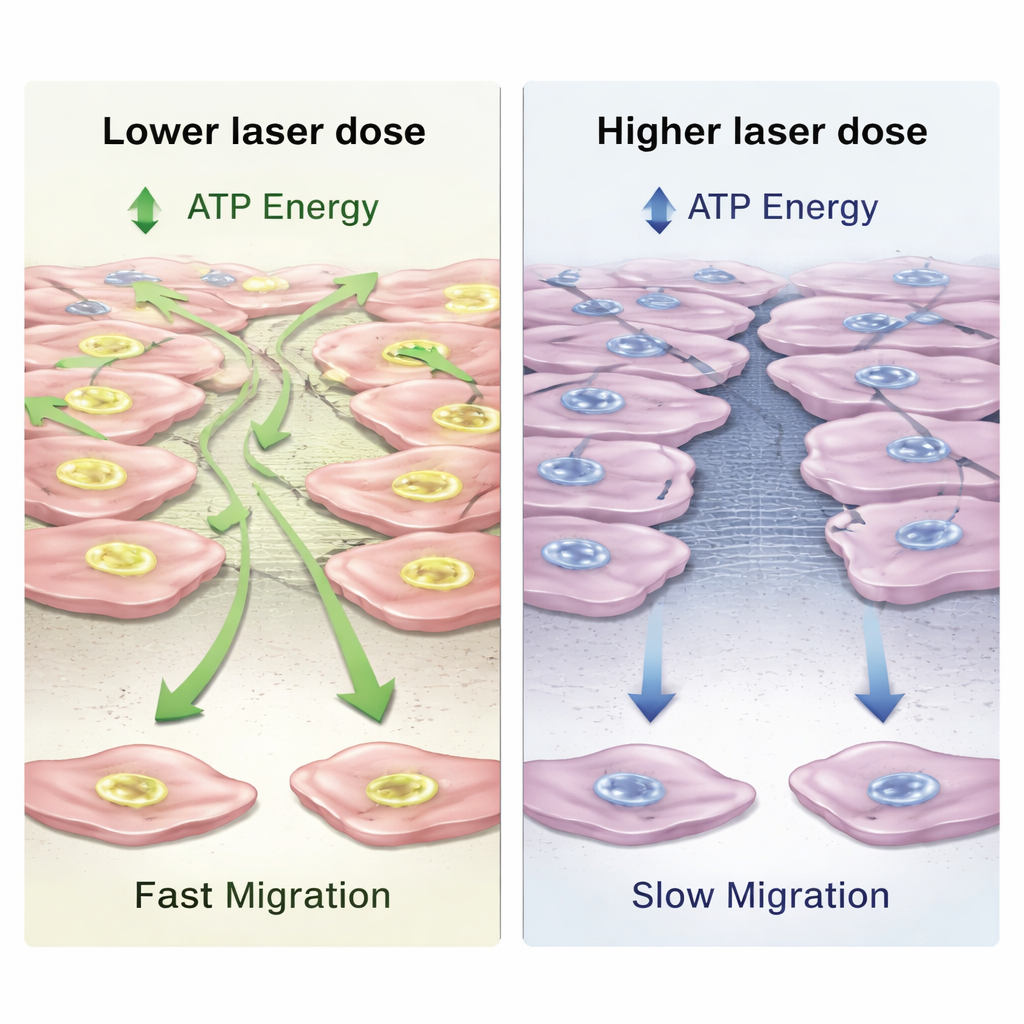
Was das für die zahnärztliche Heilung bedeuten könnte
Weil diese Experimente in einem vereinfachten Schalenmodell durchgeführt wurden, können sie die Komplexität einer heilenden Wunde in einem lebenden Mund, in dem Blutfluss, Immunzellen und Bakterien eine große Rolle spielen, nicht vollständig abbilden. Dennoch zeichnen die Ergebnisse ein vielversprechendes Dosisfenster auf, in dem ein 940-nm-Diodenlaser die Energie der Zahnfleischzellen steigern und ihre Bewegung lenken kann, ohne Schaden oder Entzündung zu verursachen. Die Arbeit zeigt außerdem, dass die Feinabstimmung der Dosis wichtig ist: Die Bedingungen, die die maximale Zellenergie bewirkten, waren nicht exakt dieselben wie diejenigen, die den schnellsten Verschluss der künstlichen Wunde erzeugten.
Fazit für Patientinnen, Patienten und Behandler
Für Nicht-Fachleute lautet die Kernbotschaft, dass niedrigenergetisches Laserlicht, sorgfältig kontrolliert, eines Tages helfen könnte, dass Zahnfleisch nach Eingriffen wie Transplantaten, Implantaten oder Extraktionen schneller und vorhersagbarer heilt. In dieser Studie förderte sehr kurze, kontaktfreie Bestrahlung mit einem 940-nm-Diodenlaser kultivierte Gingivalzellen darin, gesund zu bleiben, mehr Energie zu produzieren und — innerhalb eines bestimmten Dosisbereichs — sich schneller zu bewegen, um eine wundenähnliche Lücke zu schließen. Diese Einstellungen sind noch nicht bereit für die direkte Anwendung in der Klinik, aber sie liefern eine wissenschaftliche Grundlage für künftige Tier- und Humanstudien, die darauf abzielen, einen alltäglichen zahnärztlichen Laser in ein präzises Instrument zur Förderung natürlicher Gewebereparatur und nicht nur zum Schneiden zu verwandeln.
Zitation: Mizrahi, I.K., Neculau, C., Balasea, B.V. et al. Cellular bioenergetic and migratory responses of human gingival fibroblasts to 940 nm diode laser photobiomodulation. Sci Rep 16, 5972 (2026). https://doi.org/10.1038/s41598-026-35824-8
Schlüsselwörter: Wundheilung am Zahnfleisch, Niedrigenergiestimulation mit Laser, Erholung nach oraler Chirurgie, Photobiomodulation, Gingivalfibroblasten