Clear Sky Science · de
Mechanischer Stress fördert das Eindringen heterogener Lungenkrebszellen in enge Kanäle und untersucht das Wachstum von Tumorsphäroiden aus Zellen, die in begrenztem Raum wandern
Warum das Zusammendrücken von Krebszellen wichtig ist
Krebs breitet sich nicht im freien Raum aus. Wenn Tumorzellen ihren Ursprungsort verlassen, müssen sie sich durch winzige Spalten in Geweben, Gefäßwänden und anderen beengten Strukturen zwängen. Diese Studie stellt eine einfache, aber wirkungsvolle Frage: Welche Zellen innerhalb einer gemischten Gruppe von Lungenkrebszellen schaffen es tatsächlich durch solche engen Stellen, und welche Art von Tumoren bauen sie später auf? Die Antworten könnten erklären, warum einige Krebszellen gefährlicher sind als andere, und neue Wege zur Vorhersage oder Verlangsamung der Metastasierung aufzeigen.
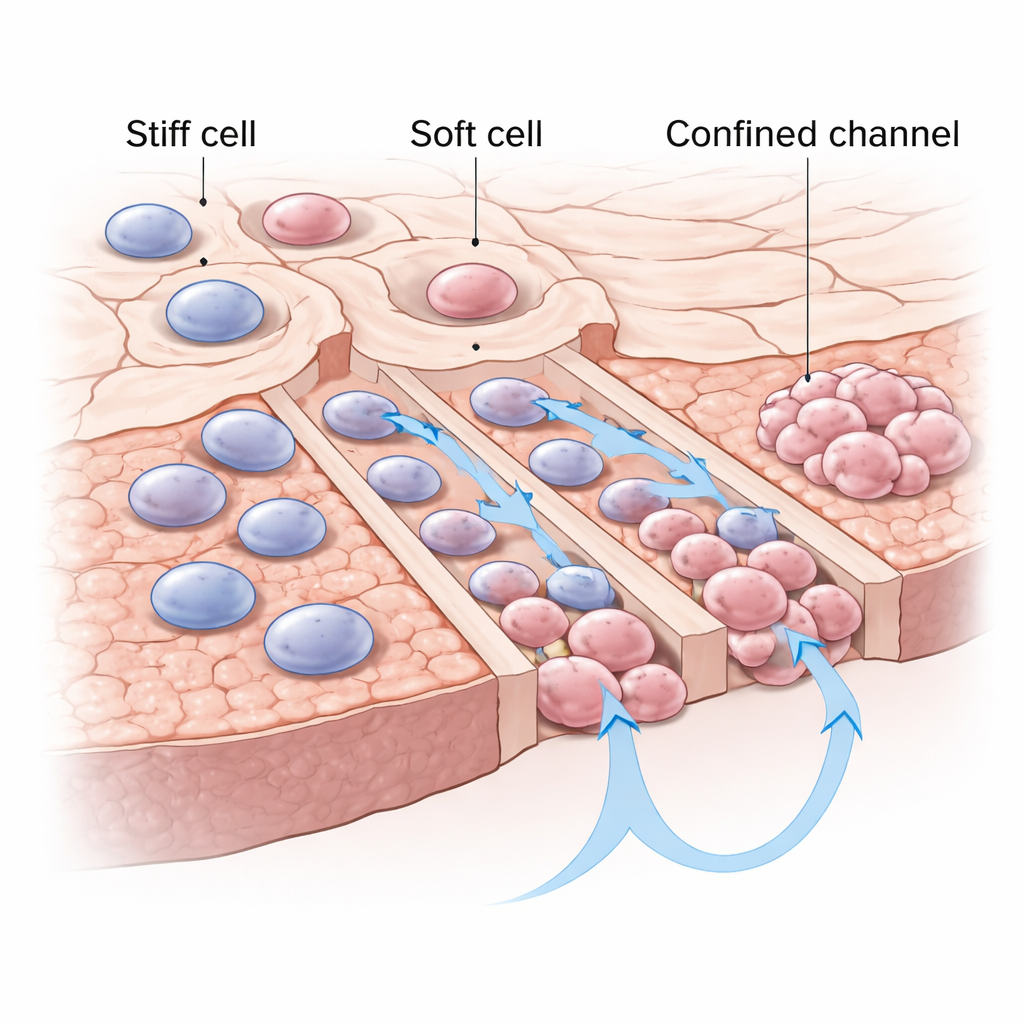
Weichere Zellen haben in engen Räumen die Nase vorn
Die Autorinnen und Autoren konzentrierten sich auf ein physikalisches Merkmal von Zellen, das den meisten Menschen unbekannt ist: die Steifigkeit. Manche Krebszellen sind relativ starr, andere dagegen weich und leicht verformbar. Mithilfe speziell entwickelter mikrofluidischer Chips – winziger Kunststoffgeräte mit Kanälen, die schmaler sind als eine typische Zelle – fingen sie einzelne Lungenkrebszellen an den Eingängen schmaler (konfineder) und hoher (unkonfineder) Kanäle ein. Nach 24 Stunden wählten und durchquerten mehr einzelne Zellen die engen, konfineden Kanäle als die offeneren, und sie bewegten sich in diesen engen Passagen schneller. Als die Forschenden die Mechanik der Zellen später mit einem Rasterkraftmikroskop (einer Art nanoskaligem „Finger“) untersuchten, stellten sie fest, dass die Reisenden in den engen Kanälen konsistent weicher waren als diejenigen, die zurückblieben oder sich in unkonfineden Kanälen bewegten.
Eine molekulare Signatur der Weichheit
Um zu verstehen, was einige Zellen weicher machte, untersuchte das Team ein Strukturprotein namens Vimentin sowie ein nukleäres Stützprotein, das vom LMNA-Gen kodiert wird. Vimentin ist Teil des inneren Gerüsts, das einer Zelle hilft, Verformungen zu widerstehen. Zellen, die durch konfinede Kanäle gedrungen waren, zeigten niedrigere Vimentin-Spiegel im Vergleich zu Zellen in geräumigen Kanälen oder in Standardkulturen. Hochauflösende Bildgebung machte deutlich, dass bei den konfineden Wanderern das Vimentin-Netzwerk sowohl um den Zellkörper als auch in der Nähe des Zellkerns lockerer angeordnet war statt dicht gebündelt. Einzelzell-Genexpressionsanalysen bestätigten, dass sowohl das Vimentin-Gen (VIM) als auch LMNA, das den Zellkern mechanisch stabilisiert, in Zellen, die enge Wege bevorzugten, herunterreguliert waren.
Zellen weicher machen fördert die Migration in engen Räumen
Die Forschenden fragten dann, ob sie Zellen gezielt aufweichen und dadurch ihr Verhalten verändern könnten. Sie nutzten zwei Ansätze: eine biochemische Behandlung (TGF-β1), die das zelluläre Skelett umgestaltet, und sanfte mechanische Kompression durch weiche Silikonschichten, die auf die Zellen drücken. Beide Methoden verringerten die Steifigkeit und senkten die Vimentin-Werte, ohne die Zellen abzutöten. Wenn diese vorweichgemachten Zellen in das mikrofluidische Gerät eingebracht wurden, wanderte ein noch größerer Anteil in die engen Kanäle im Vergleich zu unbehandelten Zellen. Das legt nahe, dass Weichheit nicht nur ein Nebeneffekt der Enge ist; sie ist eine einstellbare Eigenschaft, die stark beeinflusst, ob eine Zelle kleine Öffnungen betreten und durchqueren kann.
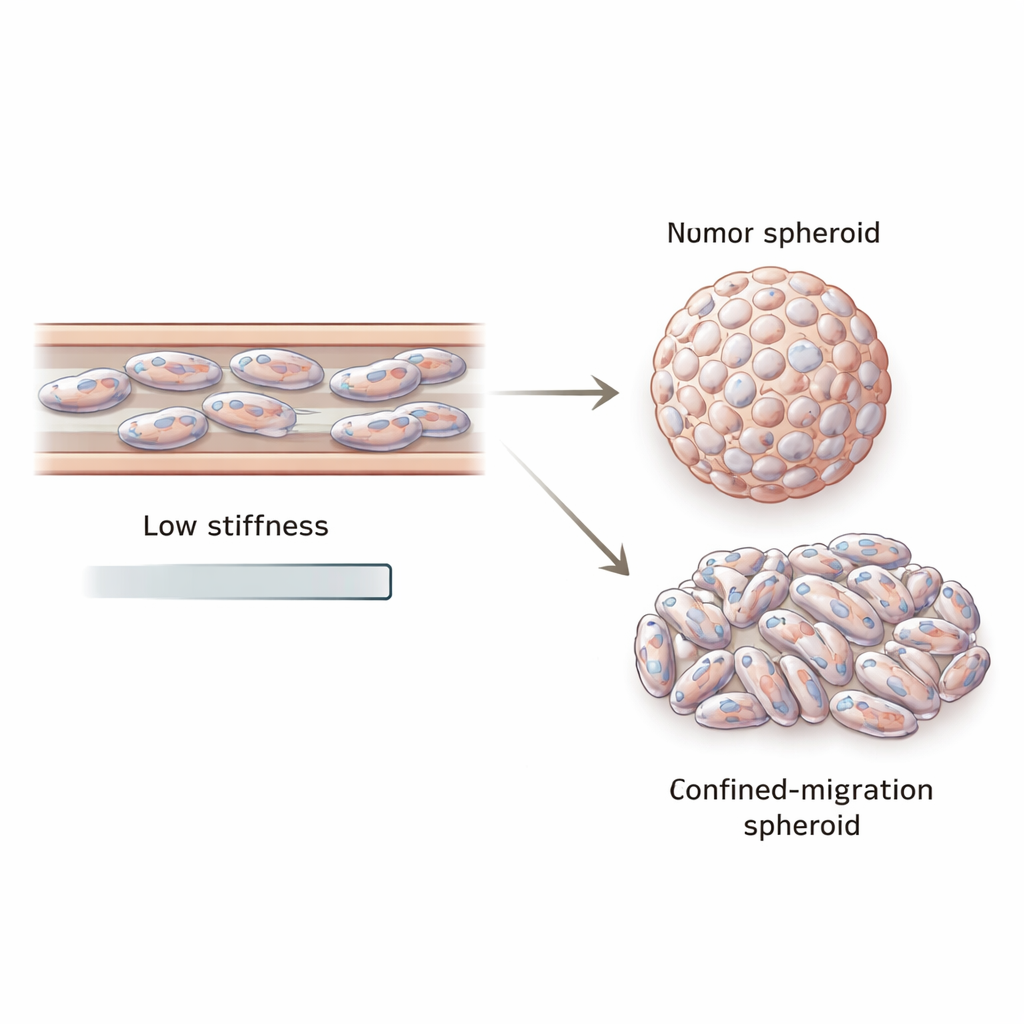
Von gequetschten Zellen zu verformten Tumorknäueln
Metastasierung betrifft jedoch nicht nur Bewegung. Entkommene Zellen müssen auch in der Lage sein, in neuen Umgebungen wieder Tumoren zu bilden. Um diesen Schritt zu imitieren, verwendete das Team ein zweites System mit Begrenzung, ein Transwell, in dem Zellen durch winzige Poren wandern, bevor sie gesammelt und in Antihaft-Kulturschalen zur Bildung dreidimensionaler Tumor-„Sphäroide“ ausgesät werden. Aus Zellen, die durch konfinede Migration gewonnen wurden, gewachsene Sphäroide waren kleiner und deutlich weniger rund als Sphäroide derselben Zelllinien ohne vorheriges Zusammendrücken. Ihre Zellkerne waren länglicher und deformierter, und diese Sphäroide zeigten weiterhin reduzierte VIM- und LMNA-Expression. Sogar innerhalb einzelner Sphäroide variierten die Vimentin-Werte vom Zentrum zum Rand, was auf mechanische und genetische Diversität in den Tochtertumoren hinweist.
Was das für das Verständnis der Metastasierung bedeutet
Kurz gesagt zeigt diese Studie, dass unter vielen Lungenkrebszellen die weicheren eher durch enge Stellen schlüpfen, die Reise überleben und später eigenartig geformte, mechanisch fragilere Tumorklumpen mit verzerrten Zellkernen bilden. Diese Zellen tragen und bewahren eine charakteristische molekulare Signatur – niedrige Spiegel wichtiger Strukturgene –, die ihr Bewegungsverhalten mit ihrem Wachstumsverhalten verknüpft. Zwar wurden die Experimente in kontrollierten Laborgeräten und nicht in Patientinnen und Patienten durchgeführt, doch bieten die Ergebnisse eine physikalische und genetische Blaupause einer „konfined-migrierenden“ Krebszelle. Langfristig könnten Messung oder gezielte Beeinflussung der Zellweichheit und ihrer molekularen Marker Teil von Strategien werden, um die invasivsten Untergruppen von Krebszellen zu verstehen, nachzuverfolgen oder schließlich zu stören.
Zitation: Alam, M.K., Ma, Y., Zhai, J. et al. Mechano-stress endorsing heterogeneous lung cancer cells migration into confined channels and investigating tumor spheroids growth of confined space migrating cells. Sci Rep 16, 6649 (2026). https://doi.org/10.1038/s41598-026-35818-6
Schlüsselwörter: Steifigkeit von Krebszellen, Migration in engen Räumen, Lungenkrebs-Sphäroide, Vimentin und LMNA, Tumormechanik