Clear Sky Science · de
Sepsis-assoziierter Skelettmuskelabbau wird durch pharmakologische Hemmung des STAT3-Signalwegs bei Mäusen gemildert
Warum schwere Infektionen Ihre Kraft rauben können
Ein lebensbedrohlicher Infekt wie Sepsis zu überleben, ist nur die halbe Miete. Viele Patientinnen und Patienten verlassen die Intensivstation so geschwächt, dass Gehen, Treppensteigen oder sogar das Heben der Arme zur Anstrengung werden. Diese Studie stellt eine einfache, aber dringliche Frage: Können wir verhindern, dass der Körper während einer Sepsis seine eigenen Muskeln abbaut, und wenn ja, wie? An Hand von Mäusen, Muskelzellen im Reagenzglas und Beobachtungen an Menschen auf einer Intensivstation verfolgen die Forschenden einen zentralen Signalweg, der den Muskelschwund antreibt — und zeigen, dass ein gezieltes Medikament den Schaden teilweise blockieren kann.
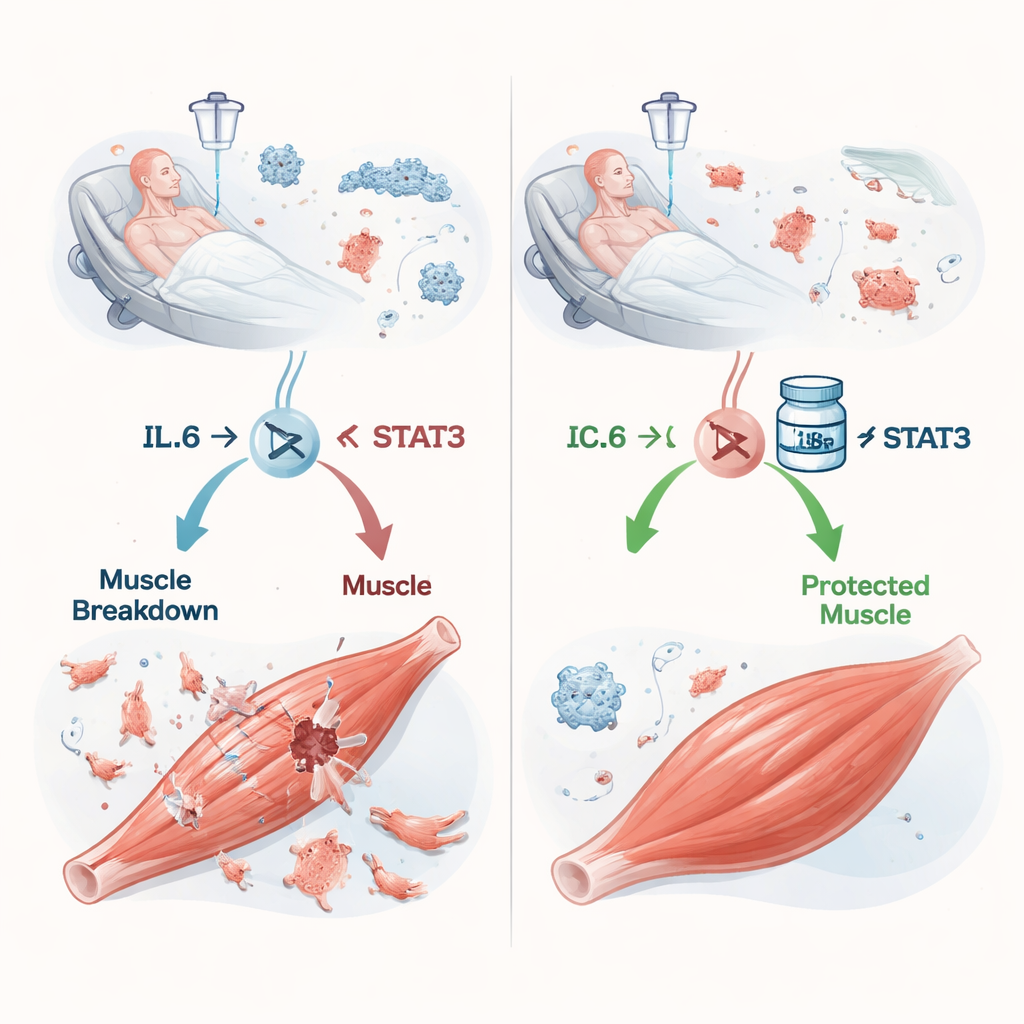
Eine Kettenreaktion von Infektion zum Muskelschwund
Sepsis entsteht, wenn die Abwehrreaktion des Körpers auf eine Infektion entgleist und das Blut mit entzündlichen Botenstoffen überschwemmt wird. Einer der wichtigsten davon ist Interleukin‑6 (IL‑6). Frühe Arbeiten deuteten an, dass IL‑6 Muskeln anweisen kann, ihre eigenen Proteine abzubauen, doch die Details waren unklar. Die Autorinnen und Autoren konzentrierten sich auf STAT3, ein zelluläres Protein, das die Botschaft von IL‑6 zum Zellkern weiterleitet, wo Gene ein- oder ausgeschaltet werden. Bei Mäusen, denen eine Blinddarm-Schlamm‑Injektion verabreicht wurde — praktisch eine kontrollierte Mischbakterien‑Infektion — stiegen die IL‑6‑Werte im Blut und in den Beinmuskeln, je stärker die Sepsis wurde. Gleichzeitig wurde STAT3 in den Muskeln aktiviert und die Tiere verloren gewicht, Muskelmasse und Griffkraft in einer schwerereitsabhängigen Weise, die dem ähnelt, was bei kritisch kranken Patientinnen und Patienten beobachtet wird.
Wie Sepsis Muskelzellen umprogrammiert
Um zu verstehen, was die Sepsis in den Muskelfasern anrichtet, analysierte das Team die Genaktivität im Musculus tibialis anterior, einem wichtigen Beinmuskel. Tausende Gene veränderten ihre Aktivität in septischen Mäusen im Vergleich zu gesunden Kontrollen. Signalwege, die an Entzündung, zellulärem Stress und insbesondere IL‑6/STAT3‑Signalübertragung beteiligt sind, wurden hochreguliert. Zwei zentrale Proteinentsorgungssysteme fuhren hoch: das Ubiquitin‑Proteasom‑System, das spezifische Muskelproteine für den Abbau markiert, und die Autophagie, ein allgemeineres Recyclingverfahren. Wichtige "Muskel‑Zerreiß"‑Enzyme, MuRF1 und Atrogin‑1, stiegen stark an, während wachstumsfördernde Signalwege und klassische Zelltod‑Signale weitgehend unverändert blieben. In parallelen Experimenten zeigten kultivierte Maus‑Muskelzellen, die Lipopolysaccharid (LPS), einem Bestandteil gramnegativer Bakterienwand, ausgesetzt wurden, dasselbe Muster: Aktivierung von IL‑6 und STAT3, Anstieg von MuRF1 und Atrogin‑1, verstärkte Autophagie und sichtbare Verdünnung der Muskelfasern.
Ein Schlüsselschalter blockieren, um Muskeln zu schützen
Das zentrale Experiment prüfte, ob das Ausschalten von STAT3 die Muskeln schonen kann. Mäuse mit Sepsis erhielten den kleinen Molekül‑STAT3‑Inhibitor C188‑9, beginnend eine Stunde nach der Infektion und dann täglich. Das Medikament milderte nicht den anfänglichen "Zytokinsturm" — die Blutwerte von IL‑6 und einem weiteren Entzündungsfaktor, TNF‑α, blieben hoch, und Körpergewicht sowie Appetit erholten sich nicht schnell. Dennoch schützte C188‑9 deutlich den Skelettmuskel: Behandelte Mäuse behielten mehr Masse des Musculus tibialis, zeigten stärkere Griffkraft und wiesen unter dem Mikroskop größere Muskelfasern auf als unbehandelte septische Mäuse. In den Muskeln reduzierte C188‑9 deutlich aktiviertes STAT3 und senkte die Werte von MuRF1 und Atrogin‑1, ließ die Autophagie‑Marker jedoch weitgehend unberührt. In Versuchen im Reagenzglas bremste die Vorbehandlung von Muskelzellen mit C188‑9 ebenfalls die STAT3‑Aktivierung und den Anstieg von MuRF1 und Atrogin‑1 und verhinderte das LPS‑induzierte Schrumpfen der Fasern, wiederum ohne die Autophagie auszuschalten.
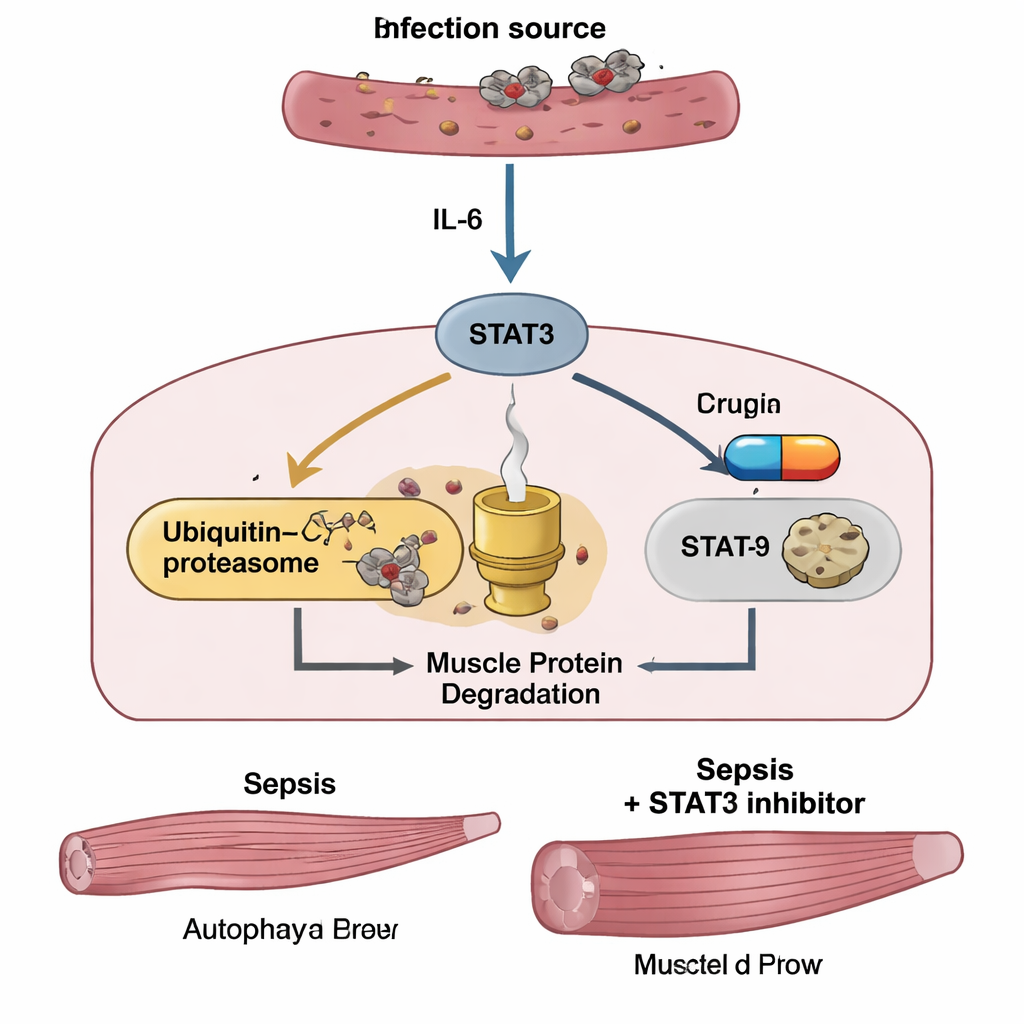
Hinweise aus der Intensivstation
Um zu prüfen, ob diese Mechanismen beim Menschen von Bedeutung sind, untersuchten die Forschenden 67 Erwachsene mit Sepsis, die auf einer Intensivstation in Japan aufgenommen wurden. Bluttests bei Aufnahme zeigten, dass Patientinnen und Patienten mit septischem Schock besonders hohe IL‑6‑Werte hatten. In der gesamten Gruppe korrelierte IL‑6 — nicht jedoch TNF‑α — eng mit Sepsis‑Schweregraden und mit Blutmarkern für Entzündung und Muskelschädigung. In einer Untergruppe von 45 Patientinnen und Patienten, die zwei CT‑Scans des Abdomens erhielten, sagten die IL‑6‑Werte bei Aufnahme voraus, wie stark der Musculus psoas am unteren Rücken in den folgenden ein bis drei Wochen schrumpfen würde. Wer am meisten Muskelmasse verlor, hatte eine deutlich schlechtere Zweijahres‑Überlebensrate als jene, die mehr ihrer Muskelmasse behielten, was unterstreicht, dass sepsisbedingter Muskelschwund nicht nur kosmetisch ist — er steht in Zusammenhang mit langfristiger Sterblichkeit.
Was das für zukünftige Behandlungen bedeuten könnte
Zusammengefasst zeichnen die Daten aus Maus‑, Zell‑ und Humanstudien eine plausible Erklärung: Während der Sepsis aktiviert das stark ansteigende IL‑6 STAT3 in den Muskeln, was wiederum ein proteinabbauendes System hochfährt, das Muskelfasern ihrer kontraktilen Bestandteile beraubt. Auch die Autophagie nimmt zu, scheint aber weniger direkt durch STAT3 gesteuert zu werden. Durch die pharmakologische Blockade von STAT3 mit C188‑9 konnten die Forschenden diesen "Selbstverzehr"‑Weg bei Mäusen und in kultivierten Muskelzellen unterbrechen und so die Kraft bewahren, obwohl Infektion und Entzündung weiter tobten. Zwar sind diese Ergebnisse noch präklinisch und beweisen nicht, dass STAT3‑Inhibitoren Menschen helfen werden, doch sie machen die IL‑6/STAT3‑Achse zu einem vielversprechenden Ziel für Medikamente, die verhindern oder verringern sollen, wie stark viele Sepsisüberlebende an Muskelkraft verlieren.
Zitation: Ono, Y., Saito, M., Yoshihara, I. et al. Sepsis-associated skeletal muscle wasting is ameliorated by pharmacological inhibition of the STAT3 signaling pathway in mice. Sci Rep 16, 5008 (2026). https://doi.org/10.1038/s41598-026-35815-9
Schlüsselwörter: Sepsis, Muskelschwund, STAT3, Entzündung, Erholung nach kritischer Erkrankung