Clear Sky Science · de
Metabolomische Vorhersage des Mutationsstatus gesunder Personen mit familiärer Belastung durch das hereditäre Brust‑ und Ovarialkarzinom‑Syndrom: die HRRmet‑Studie
Warum versteckte Hinweise im Blut wichtig sind
Viele wissen, dass Brust‑ und Eierstockkrebs familiär gehäuft auftreten können, oft aufgrund vererbter Veränderungen in Genen wie BRCA1 und BRCA2. Heute kann Gentestung zeigen, wer solche Risikomutationen trägt — sie ist jedoch teuer, nicht überall verfügbar und manche Menschen scheuen vor einem DNA‑Test zurück. Diese Studie stellt eine kühne Frage: Könnte ein einfacher Bluttest, der kleine vom Körper produzierte Moleküle misst, Hinweise darauf geben, ob eine gesunde Person solche erblichen, krebsassoziierten Mutationen trägt, lange bevor ein Tumor erscheint?
Winzige Moleküle als Frühboten
Unsere Zellen produzieren und bauen ständig Tausende kleiner Chemikalien — Metaboliten — ab, als Teil des normalen Stoffwechsels. Zusammen bilden diese Chemikalien einen „metabolomischen“ Fingerabdruck, der sowohl unsere Gene als auch unsere Umwelt widerspiegelt. Die Forscher überlegten, dass, wenn bestimmte Gene zur DNA‑Reparatur defekt sind — speziell solche, die an der homologen Rekombinationsreparatur beteiligt sind, die gefährliche DNA‑Brüche behebt — subtile Verschiebungen im Stoffwechsel im Blut sichtbar werden könnten. Das Nachweisen dieser Verschiebungen könnte einen neuen Weg bieten, Personen zu identifizieren, die stillschweigend schädliche Varianten in Genen wie BRCA1, BRCA2, PALB2, ATM, CHEK2 und RAD51 tragen.
Untersuchung gesunder Angehöriger mit Risiko
Das Team rekrutierte 260 gesunde Freiwillige aus Familien mit hereditärem Brust‑ und Ovarialkarzinom. Die Hälfte von ihnen war als Träger pathogenicer Varianten in einem der DNA‑Reparaturgene bekannt, die andere Hälfte waren eng angepasste Verwandte ohne solche Varianten. Entscheidend ist, dass keiner der Teilnehmenden Krebs hatte, sodass etwaige Unterschiede in der Blutchemie auf den erblichen genetischen Status und nicht auf einen Tumor zurückzuführen sind. Mit einer sensitiven Methode, die Flüssigchromatographie mit hochauflösender Massenspektrometrie koppelt, maßen die Wissenschaftler 285 Metaboliten im Plasma und analysierten 169 hochwertige Signale detailliert.
Muster, die Träger von Nichtträgern unterscheiden
Erste statistische Tests zeigten, dass Dutzende Metaboliten zwischen Trägern und Nichtträgern in mindestens einem Vergleich unterschiedlich waren. Die stärksten Signale stammten häufig von Lipiden, insbesondere fettrelevanten Molekülen wie Lysophosphatidylcholinen und Carnitinderivaten, sowie von bestimmten Aminosäuren wie Prolin, Tyrosin und Valin. Diese Moleküle sind bereits dafür bekannt, eine Rolle dabei zu spielen, wie Krebszellen ihren Energiehaushalt umstellen, was darauf hindeutet, dass das metabolische „Fundament“ für krebsähnliches Verhalten bereits bei derzeit gesunden Personen nachweisbar sein könnte. Als die Forschenden ein allgemeines Modell mit 31 Metaboliten zur Unterscheidung aller Träger von allen Nichtträgern erstellten, klassifizierte es etwa 62 Prozent der Individuen korrekt — besser als Zufall, aber noch nicht geeignet als alleiniges Testverfahren.
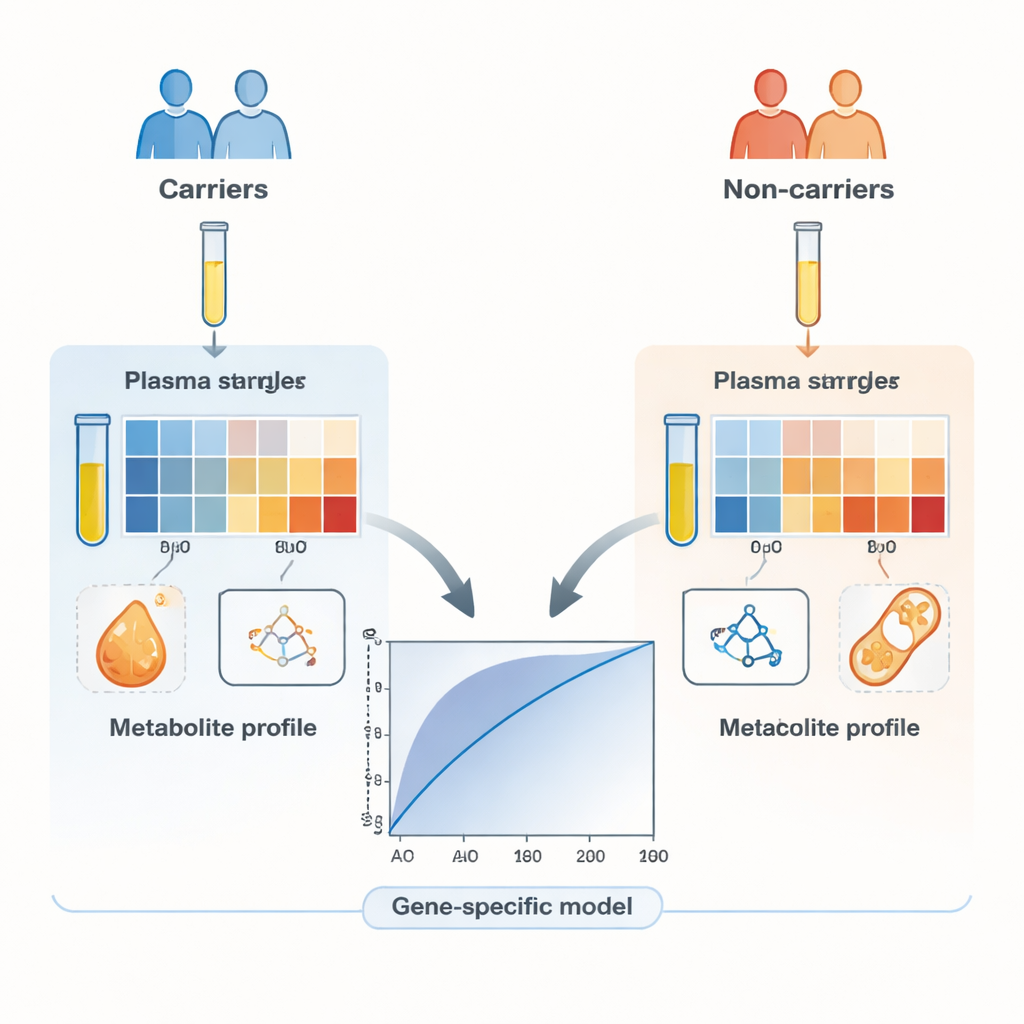
Schärfere Signale bei Fokussierung auf einzelne Gene
Das Bild verbesserte sich deutlich, als das Team separate Vorhersagemodelle für einzelne Gene erstellte. Indem ein Machine‑Learning‑Algorithmus die informativste Teilmenge von Metaboliten für jedes Gen auswählte, entstanden kompakte Signaturen — manchmal nur eine Handvoll Moleküle — die Träger von BRCA1, BRCA2, PALB2, ATM oder CHEK2 mit mehr als 80 Prozent Genauigkeit identifizierten, oft sogar deutlich besser. Modelle, die um Gene mit sogenannt moderatem Risiko aufgebaut waren, wie ATM und CHEK2, schnitten besonders gut ab, obwohl sie relativ wenige Metaboliten nutzten. Heatmaps der Daten zeigten, dass sich Ergebnisse klarer nach Metabolitentyp (zum Beispiel Lipide versus Aminosäuren) als nach dem mutierten Gen gruppierten, was unterstreicht, dass verschiedene Gendefekte überlappende Stoffwechselwege stören können.
Was das für Familien bedeuten könnte
Einfach gesagt zeigt diese Studie, dass sich die Blutchemie gesunder Personen mit erblichen Mutationen, die mit Brust‑ und Eierstockkrebs assoziiert sind, messbar von der ihrer nicht betroffenen Verwandten unterscheidet. Diese Unterschiede sind subtil und mit Standard‑Bluttests nicht sichtbar, treten jedoch hervor, wenn Hunderte von Metaboliten zusammen mit fortgeschrittenen statistischen Methoden betrachtet werden. Obwohl dieser Ansatz die Gentestung noch nicht ersetzen kann, weist er in eine Zukunft, in der ein metabolomischer Bluttest helfen könnte, Hochrisikopersonen zu identifizieren, Screening‑Strategien zu verfeinern oder zu priorisieren, wer eine umfassende DNA‑Untersuchung erhalten sollte. Für Familien mit hereditärem Krebs könnten solche Werkzeuge ein zusätzliches, nichtinvasives Fenster in das vererbte Risiko bieten — lange bevor sich eine Krankheit entwickelt.
Zitation: Roig, B., Fernández-Castillejo, S., Gumà, J. et al. Metabolomic-driven prediction of the mutational status of healthy individuals with a family history of hereditary breast and ovarian cancer syndrome: the HRRmet study. Sci Rep 16, 6844 (2026). https://doi.org/10.1038/s41598-026-35789-8
Schlüsselwörter: hereditärer Brustkrebs, Ovarialkarzinomrisiko, Metabolomik, genetische Mutationen, Blut‑Biomarker