Clear Sky Science · de
Schleyer‑artige hyperkonjugative Aromatizität in CH‑Isomeren von Diazolen aufgezeigt durch DFT‑ und NBO‑Analyse
Warum ringförmige Moleküle wichtig sind
Chemiker wissen schon lange, dass manche ringförmigen Moleküle ungewöhnlich stabil sind und sich auf spezielle Weise verhalten. Diese Eigenschaft, Aromatizität genannt, liegt allem zugrunde, von dem Geruch von Benzin bis zur Wirksamkeit vieler Arzneimittel. In dieser Studie untersuchten die Autoren, wie winzige chemische Anhängsel, sogenannte Substituenten, diese Stabilität in einer Familie stickstoffhaltiger Ringe, den Diazolen, verstärken oder abschwächen können. Durch das Verständnis und die Steuerung dieses feinen Effekts können Wissenschaftler Moleküle mit vorhersagbarerem Reaktionsverhalten entwerfen, was für die Wirkstoffforschung und die Entwicklung fortgeschrittener Materialien entscheidend ist.
Stabilität durch kleine Änderungen formen
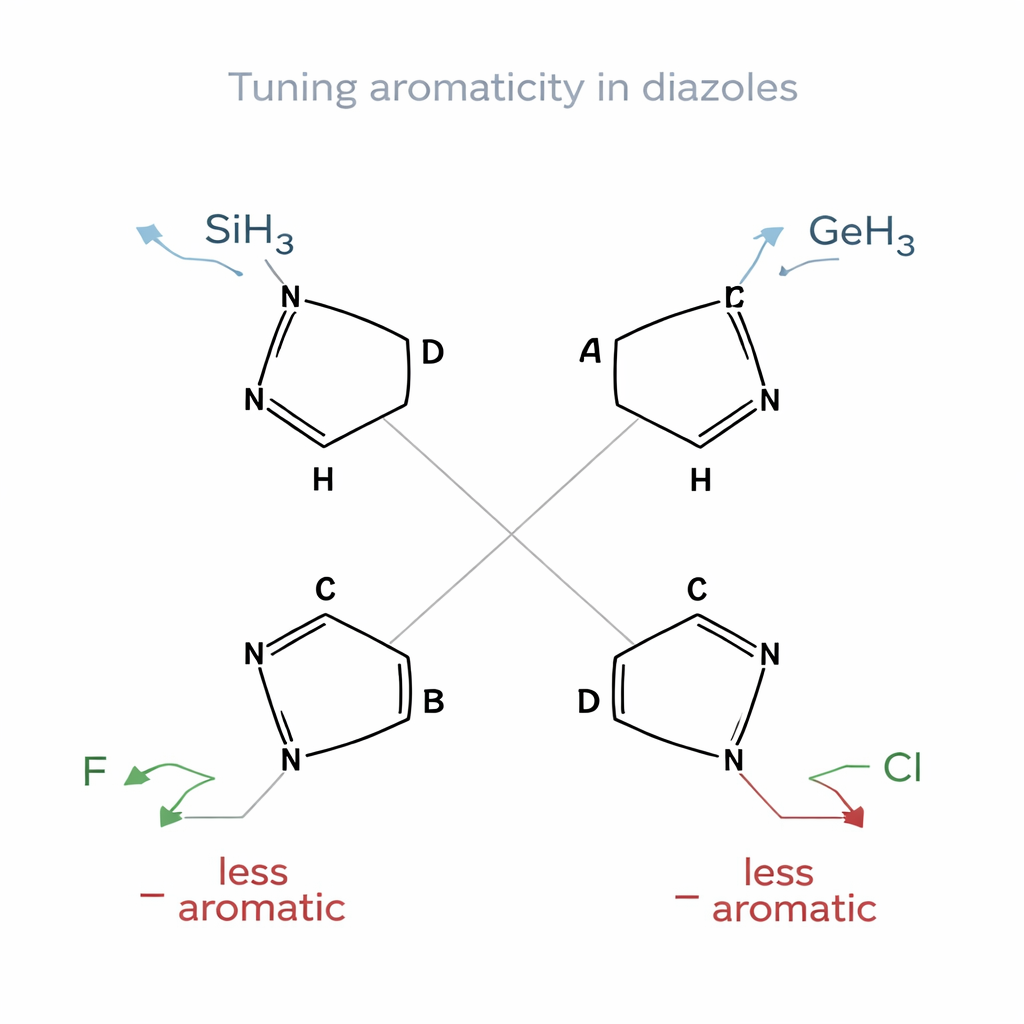
Diazole sind fünfgliedrige Ringe mit zwei Stickstoffen und drei Kohlenstoffen; hier konzentrierten sich die Autoren auf weniger verbreitete "CH‑Tautomere", bei denen eine Ringposition ein Kohlenstoff‑Wasserstoff‑Baustein statt der üblichen Stickstoff‑Wasserstoff‑Form ist. Sie untersuchten vier unterschiedliche Anordnungen der Stickstoffatome, bezeichnet A bis D, von denen jede die Elektronenverteilung im Ring verändert. Auf diese Gerüste setzten sie eine Reihe einfacher Gruppen, etwa Wasserstoff, Methyl, Halogene wie Fluor und Chlor, schwerere Atome wie Silicium und Germanium sowie klassische elektronenschiebende oder -ziehende Gruppen wie Amino (–NH₂), Hydroxy (–OH), Cyano (–CN) und Borhydrid (–BH₂). Mit quantenchemischen Rechnungen fragten sie, wie jeder Substituent den aromatischen Charakter und die Gesamtstabilität des Rings beeinflusst.
Wie das Team Aromatizität misst
Aromatizität lässt sich nicht direkt beobachten, daher nutzte das Team mehrere komplementäre Maßstäbe. Strukturelle Indizes, wie HOMED und der Bird‑Index, verfolgen, wie gleichmäßig die Bindungslängen im Ring sind; gleichmäßigere Bindungen deuten im Allgemeinen auf stärkeren aromatischen Charakter hin. Magnetische Indizes, bekannt als NICS‑Werte, sondieren winzige Magnetfelder, die durch zirkulierende Elektronen erzeugt werden – ein Kennzeichen aromatischer Ringe. Schließlich quantifiziert eine elektronische Methode, die Natural Bond Orbital (NBO)‑Analyse, wie stark Elektronen von einer Bindung in eine andere fließen können und liefert damit ein Maß für hyperkonjugative Stabilisierung. Durch den Vergleich dieser verschiedenen Indikatoren erstellen die Forscher ein multidimensionales Bild davon, wie jeder Substituent die Elektronendelokalisation in den Diazolringen beeinflusst.
Gewinner und Verlierer beim Verstärken von Ringströmen
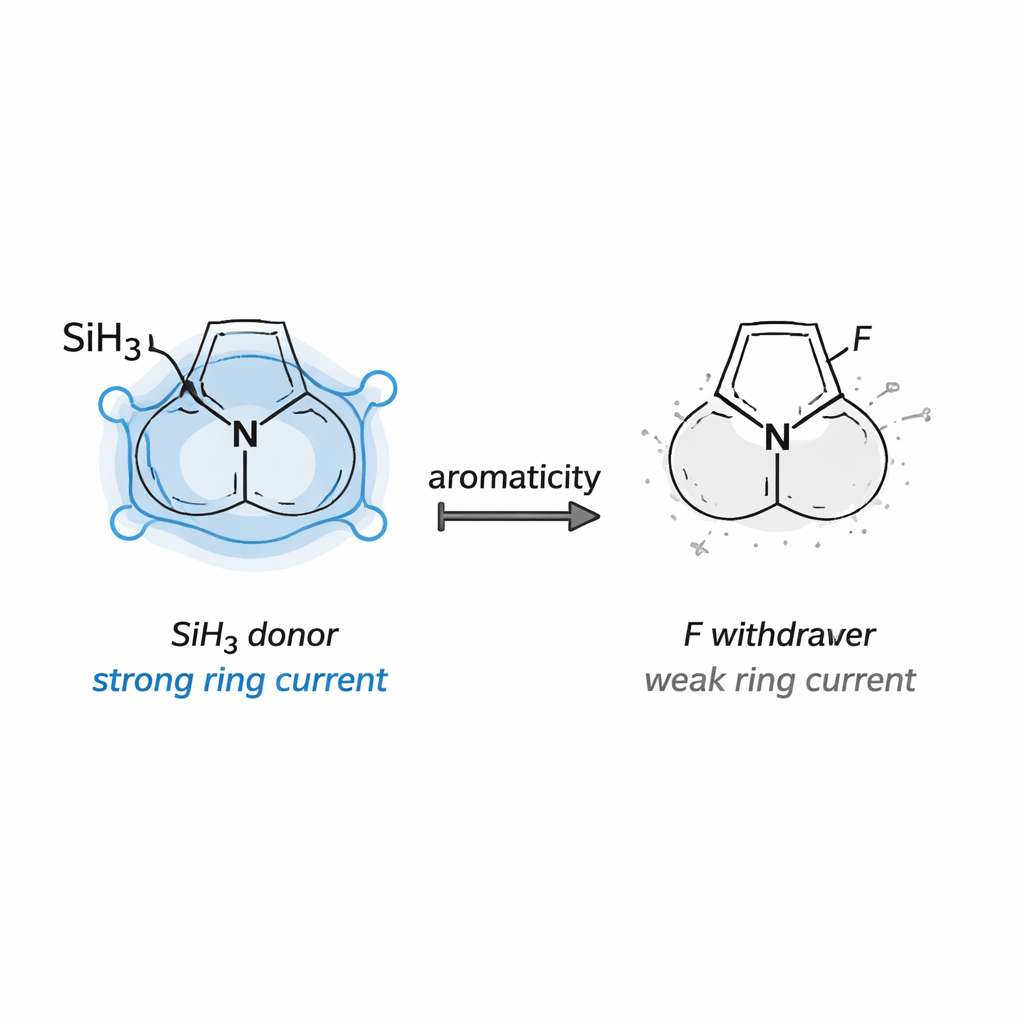
Ein klares Muster trat zutage. Substituenten mit Silicium (–SiH₃) und Germanium (–GeH₃) verstärkten durchweg die Aromatizität in allen vier Diazolfamilien. Ringe mit diesen Gruppen zeigten gleichmäßigere Bindungslängen, stärkere berechnete Ringströme und große Stabilisierungsenergien durch Elektronenspende in das Ringsystem. Dieses Verhalten passt zum Konzept der Schleyer‑artigen hyperkonjugativen Aromatizität, bei der bestimmte σ‑Bindungen als starke Donoren in den aromatischen Kreislauf fungieren. Eine kleine, spannende cyclopropyl‑ähnliche Brücke (–CH₂–CH₂–) verstärkte die Aromatizität ebenfalls und wirkte als Donor mittlerer Stärke. Im krassen Gegensatz dazu tendierten Fluor und in geringerem Maße Chlor dazu, Elektronendichte aus dem Ring zu entziehen, wodurch die Ringströme abgeschwächt wurden und in einigen Fällen der aromatische Charakter nahezu verschwunden war.
Überraschungen bei klassischen Donoren und Akzeptoren
Traditionelle π‑Donorgruppen wie –NH₂ und –OH, die oft verwendet werden, um die Elektronendichte in aromatischen Systemen zu erhöhen, zeigten hier nur moderate Effekte. Sie verbesserten leicht die Bindungsgleichheit und die Ringströme, erreichten aber niemals die Wirkung der Silicium‑ und Germaniumsubstituenten. Noch auffälliger war der Unterschied zwischen der Cyano‑ (–CN) und der Borhydrid‑Gruppe (–BH₂). Beide gelten formal als elektronengering, verhielten sich jedoch sehr unterschiedlich. Die Cyano‑Gruppe schwächte allgemein die Aromatizität, indem sie Elektronendichte aus dem Ring zog. Im Vergleich dazu fungierte –BH₂ überraschend stark als Aromatizitätsförderer: Seine Bindungen spendeten Elektronendichte in das Ringgerüst, ähnlich wie –SiH₃ und –GeH₃, und erzeugten beträchtliche hyperkonjugative Stabilisierung.
Eine Geschichte, erzählt von vielen Messungen
Als die Autoren alle ihre Indizes verglichen, war die Botschaft konsistent. Strukturelle Maße, magnetische Reaktionen und elektronische Stabilisierungsenergien bewegten sich im Gleichklang: Ringe, die geometrisch mehr benzolähnlich wirkten, wiesen auch stärkere berechnete Ringströme und größere hyperkonjugative Stabilisierung auf. Fluorierte Systeme gruppierten sich am Ende der Skala mit niedriger Aromatizität, während silicium‑, germanium‑, cyclopropyl‑ähnliche und –BH₂‑substituierte Ringe am hocharomatischen Ende standen. Für den allgemeinen Leser lautet die Erkenntnis, dass Chemiker durch die Wahl geeigneter Substituenten und Positionen an einem Ring den Elektronenfluss in winzigen molekularen Schaltkreisen fein abstimmen können. Diese Arbeit zeigt, wie dieses Feintuning in Diazolgerüsten funktioniert und bietet praktische Gestaltungsregeln zum Entwurf stabilerer, reaktiverer oder besser steuerbarer aromatischer Moleküle.
Zitation: Dehkordi, P.N., Saeidian, H., Mirjafary, Z. et al. Schleyer-type hyperconjugative aromaticity in CH isomers of diazoles revealed by DFT and NBO analysis. Sci Rep 16, 7131 (2026). https://doi.org/10.1038/s41598-026-35776-z
Schlüsselwörter: Aromatizität, Diazole, Hyperkonjugation, Substituenteneffekte, rechnergestützte Chemie