Clear Sky Science · de
Leichtgewichtige SwiM-UNet mit multidimensionalem Adapter für effiziente medizinische Bildsegmentierung direkt auf dem Gerät
Intelligentere Untersuchungen am Krankenbett
Hirnscans können lebensbedrohliche Tumoren sichtbar machen, doch aus Rohbildern genaue Umrisse zu erzeugen, die Ärztinnen und Ärzte nutzen können, ist nach wie vor zeitaufwändig und rechenintensiv. Diese Studie stellt SwiM‑UNet vor, einen neuen Algorithmus, der Hirntumoren aus 3D‑MRT‑Scans mit Spitzenqualität segmentieren kann und dabei effizient genug ist, um lokal auf Endgeräten zu laufen – was präzise Bildanalyse näher ans Krankenbett oder sogar in mobile Kliniken bringt. 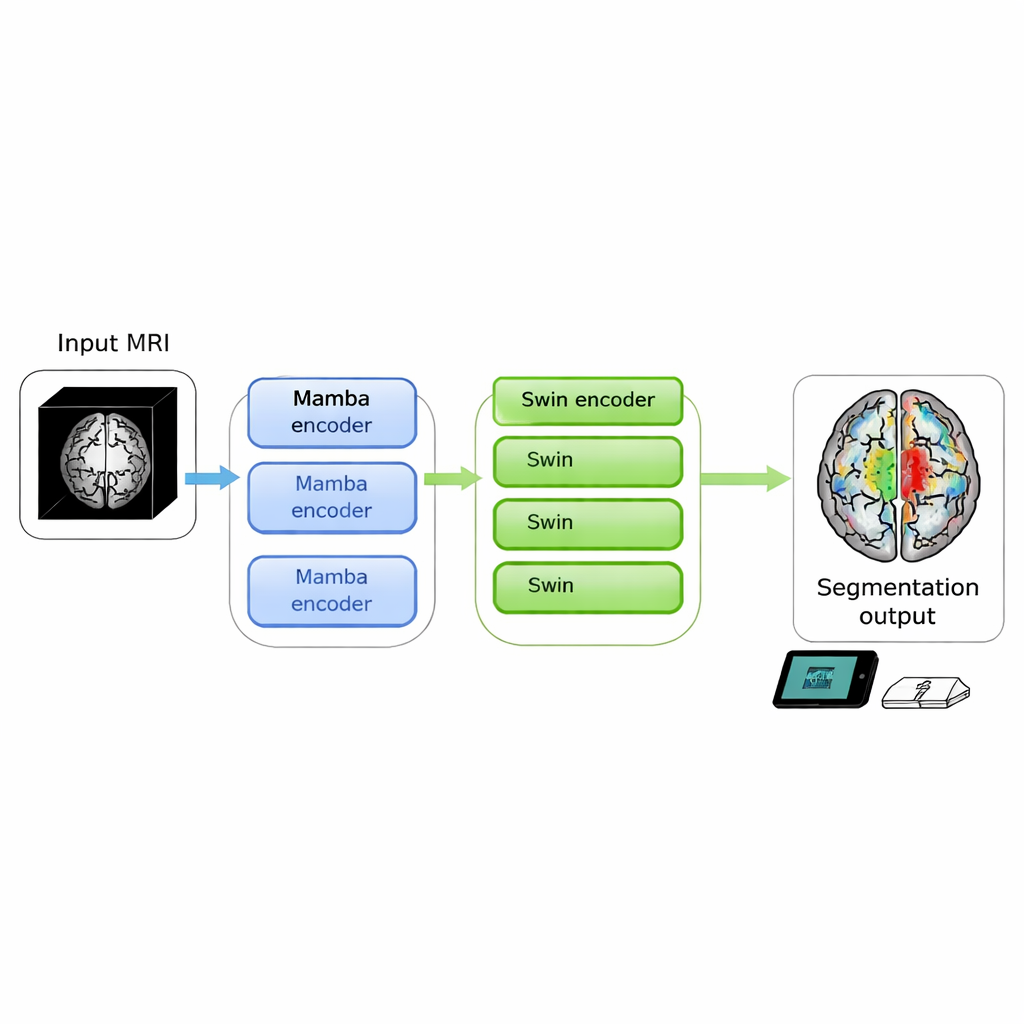
Warum präzise Tumorumrisse wichtig sind
Die moderne Medizin stützt sich stark auf Bildgebung zur Planung von Operationen, Strahlentherapie und medikamentösen Behandlungen. Bei Hirntumoren müssen Ärztinnen und Ärzte nicht nur feststellen, dass ein Tumor vorhanden ist, sondern auch genau wissen, wo verschiedene Bereiche beginnen und enden. Diese Aufgabe, Segmentierung genannt, wird meist von Spezialisten Schicht für Schicht durchgeführt oder nachbearbeitet – ein zeitaufwändiger Prozess, der Entscheidungen verzögern kann und zwischen Expertinnen und Experten variiert. Automatisierte Segmentierungswerkzeuge auf Basis tiefer neuronaler Netze haben die Lage verbessert, doch die genauesten Modelle verlangen häufig leistungsfähige Grafikprozessoren, wodurch ihre Nutzung direkt in der Klinik, insbesondere auf kleineren oder tragbaren Geräten, erschwert wird.
Zwei starke Ideen, die sich nicht leicht auf kleine Geräte übertragen lassen
Jüngste Durchbrüche in der Computer Vision stammen hauptsächlich aus zwei Modellfamilien. Transformer‑basierte Systeme wie der Swin Transformer sind hervorragend darin, globale Muster im gesamten 3D‑Scan zu erfassen und haben leistungsstarke Hirntumor‑Segmentierer ermöglicht. Ihre Kernoperation, die Self‑Attention, wird jedoch bei wachsender Bildgröße extrem rechenintensiv und begrenzt so den Einsatz in Echtzeit oder auf kompakter Hardware. Eine neuere Familie, bekannt als Mamba und basierend auf State‑Space‑Modellen, bietet einen cleveren Umweg: Sie verarbeitet Sequenzen effektiv in linearer Zeit und reduziert so die benötigten Berechnungen. Erste Experimente in der medizinischen Bildgebung zeigten, dass Mamba‑ähnliche Modelle schnell und effizient sind, aber in der Segmentierungsqualität oft hinter Transformern zurückbleiben, besonders bei komplexen Tumorformen.
Geschwindigkeit und Genauigkeit in einem Entwurf vereint
Die Autorinnen und Autoren verfolgten das Ziel, die Stärken beider Ansätze in einem einzigen 3D‑Modell zu verbinden. Ihre SwiM‑UNet behält die vertraute U‑förmige Struktur, die in der medizinischen Bildgebung weit verbreitet ist, mit einem Encoder, der Informationen komprimiert, und einem Decoder, der detaillierte Segmentierungen rekonstruiert. In den frühen Stadien, wenn der Scan noch groß und hochaufgelöst ist, setzen sie effiziente Mamba‑Blöcke ein, um die Berechnungen überschaubar zu halten. Tiefer im Netzwerk, nachdem die Daten heruntergesampelt wurden, wechseln sie zu vereinfachten Swin‑Transformer‑Blöcken, die nun langfristige Beziehungen modellieren können, ohne die Hardware zu überfordern. Eine maßgeschneiderte Brücke, der MS‑Adapter, verbindet diese beiden Bereiche. Er betrachtet Merkmale separat entlang Breite, Höhe und Tiefe des Volumens sowie kanalübergreifend und lernt über kleine Gate‑Einheiten, wie stark jede Sicht die endgültige Repräsentation beeinflussen sollte. 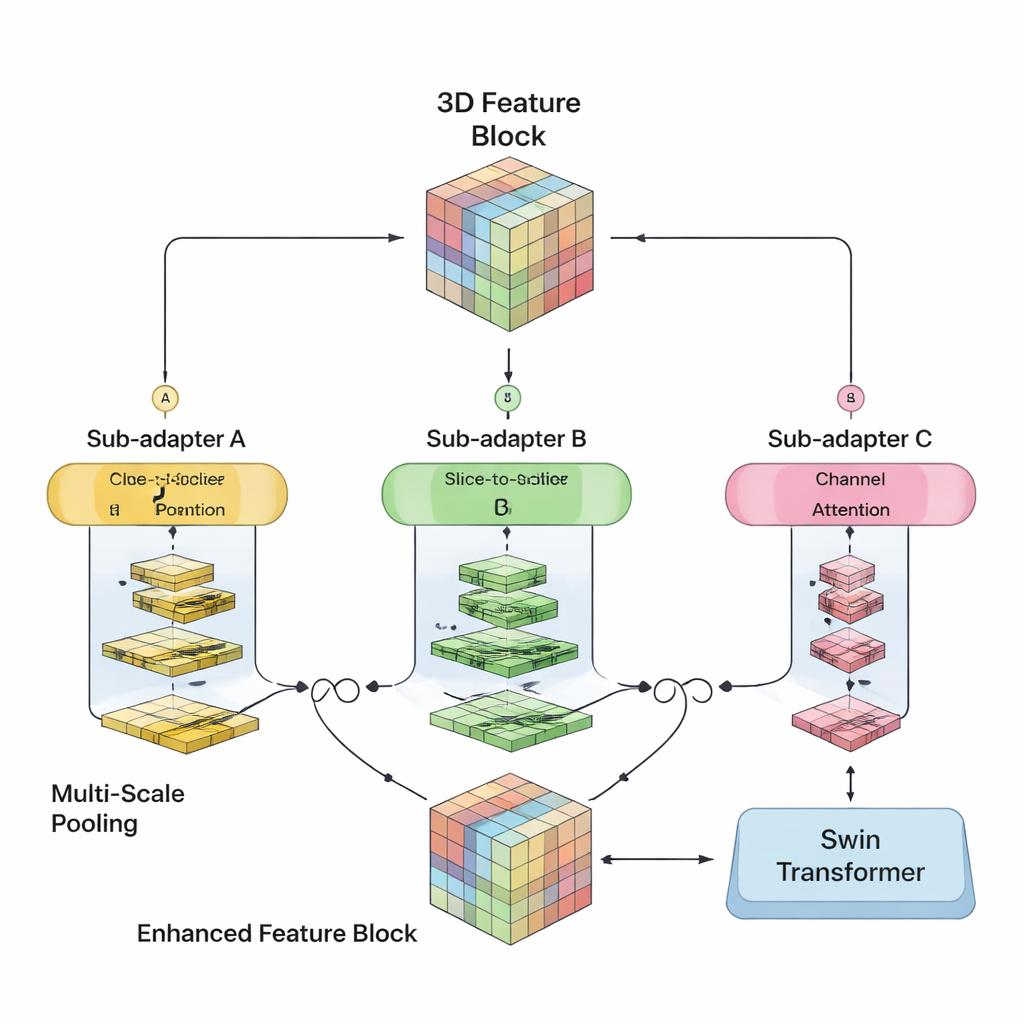
Mehr erreichen mit weniger Rechenaufwand
Über dieses hybride Layout hinaus reduziert das Team unnötige Rechenlast, indem es niedrigrangige vollverbundene Schichten und einen Decoder verwendet, der bewusst die Anzahl der zu verarbeitenden Kanäle verringert. Sie testeten mehrere Varianten mit unterschiedlichen Mischungen von Mamba‑ und Swin‑Schichten und fanden heraus, dass der Einsatz von Mamba in den ersten drei Encoder‑Stufen und Swin nur in der tiefsten Stufe das beste Verhältnis von Geschwindigkeit und Genauigkeit liefert. Auf zwei großen öffentlichen Hirntumor‑Datensätzen aus den BraTS‑Herausforderungen 2023 und 2024 erreichte SwiM‑UNet höhere Genauigkeit und präzisere Grenzen als führende reine Transformer‑, reine Mamba‑ und frühere Hybridmodelle, während es deutlich weniger Fließkommaoperationen benötigte und die Inferenzzeit auf einer modernen Grafikkarte auf etwa 45 Millisekunden pro Scan‑Patch reduzierte.
Bereit für echte Geräte
Um zu prüfen, ob diese Verbesserungen außerhalb des Labors relevant sind, verglichen die Forschenden den Rechenbedarf des Modells mit den Fähigkeiten typischer klinischer Edge‑Systeme – tragbaren MRT‑Konsolen, Point‑of‑Care‑Computern und OP‑Workstations. Ihre Analyse legt nahe, dass SwiM‑UNet, im Gegensatz zu schwereren Transformer‑Modellen, bequem innerhalb der Leistungs-, Speicher‑ und Geschwindigkeitsgrenzen solcher Geräte passt und oft Echtzeitanforderungen erfüllt. Es zeigte zudem starke Ergebnisse auf einem separaten abdominalen CT‑Datensatz, was darauf hindeutet, dass sich der Ansatz über Hirntumoren und sogar über MRT hinaus verallgemeinern lässt.
Was das für Patientinnen, Patienten und Klinikpersonal bedeutet
Praktisch bedeutet SwiM‑UNet, dass es möglich ist, an die Genauigkeit der anspruchsvollsten Segmentierungsmodelle heranzukommen und gleichzeitig die Rechenlast so gering zu halten, dass eine Nutzung direkt auf dem Gerät realistisch wird. Das könnte schnellere, konsistentere Tumorumrisse in Notaufnahmen, ländlichen Krankenhäusern oder mobilen Bildgebungseinheiten ermöglichen, ohne sensible Scans an entfernte Server senden zu müssen. Obwohl weitere Arbeiten nötig sind, um die Methode an verschiedene Scanner und Bedingungen anzupassen, deutet dieses hybride Design auf eine Zukunft hin, in der hochwertige Bildanalyse dort läuft, wo sich die Patientin oder der Patient befindet – nicht nur in Rechenzentren.
Zitation: Noh, Y., Lee, S., Jin, S. et al. Lightweight SwiM-UNet with multi-dimensional adaptor for efficient on-device medical image segmentation. Sci Rep 16, 5807 (2026). https://doi.org/10.1038/s41598-026-35771-4
Schlüsselwörter: Hirntumorsegmentierung, KI in der medizinischen Bildgebung, hybride neuronale Netzwerke, On-Device-Inferenz, 3D-MRT-Analyse