Clear Sky Science · de
KChIP1-Spleißvarianten modulieren Kv4-Kanäle, indem sie P/C‑Typ-Inaktivitätsmerkmale fördern
Wie winzige Poren den elektrischen Rhythmus des Gehirns formen
Jeder Gedanke, jede Erinnerung und jede Bewegung im Gehirn beruht auf schnellen elektrischen Signalen in Nervenzellen. Diese Signale werden von mikroskopisch kleinen Poren — Ionenkanälen — fein gesteuert, die geladene Teilchen ein- und ausströmen lassen. Dieser Beitrag untersucht, wie subtile Varianten eines Hilfsproteins, KChIP1, das Verhalten einer dieser Kanalgruppen (Kv4‑Kanäle) deutlich verändern können und damit beeinflussen, wie leicht Neurone wiederholt elektrische Aktivitätsbursts erzeugen können.
Kaliumkanäle als Bremsmechanismus des Gehirns
Kv4‑Kanäle tragen einen sogenannten A‑Typ‑Kaliumstrom, der sich am Zellkörper und in den Verästelungen von Neuronen schnell ein‑ und ausschaltet. Dieser Strom bestimmt mit, wie leicht ein Neuron feuert und wie zuverlässig es eingehenden Signalen folgen kann, besonders bei niedrigen Feuerraten. Kv4‑Kanäle wirken nicht allein: sie bündeln sich mit Hilfsproteinen zu einem Komplex, der DPP‑Proteine und KChIP‑Proteine umfasst. Diese Partner beeinflussen, wie schnell die Kanäle abschalten und wie rasch sie wieder bereit sind zu öffnen. Bislang legten die meisten Arbeiten nahe, dass KChIPs allgemein die Erholung von Kv4‑Kanälen nach dem Abschalten beschleunigen und Neuronen so erlauben, schnell auf wiederholte Eingänge zu reagieren.
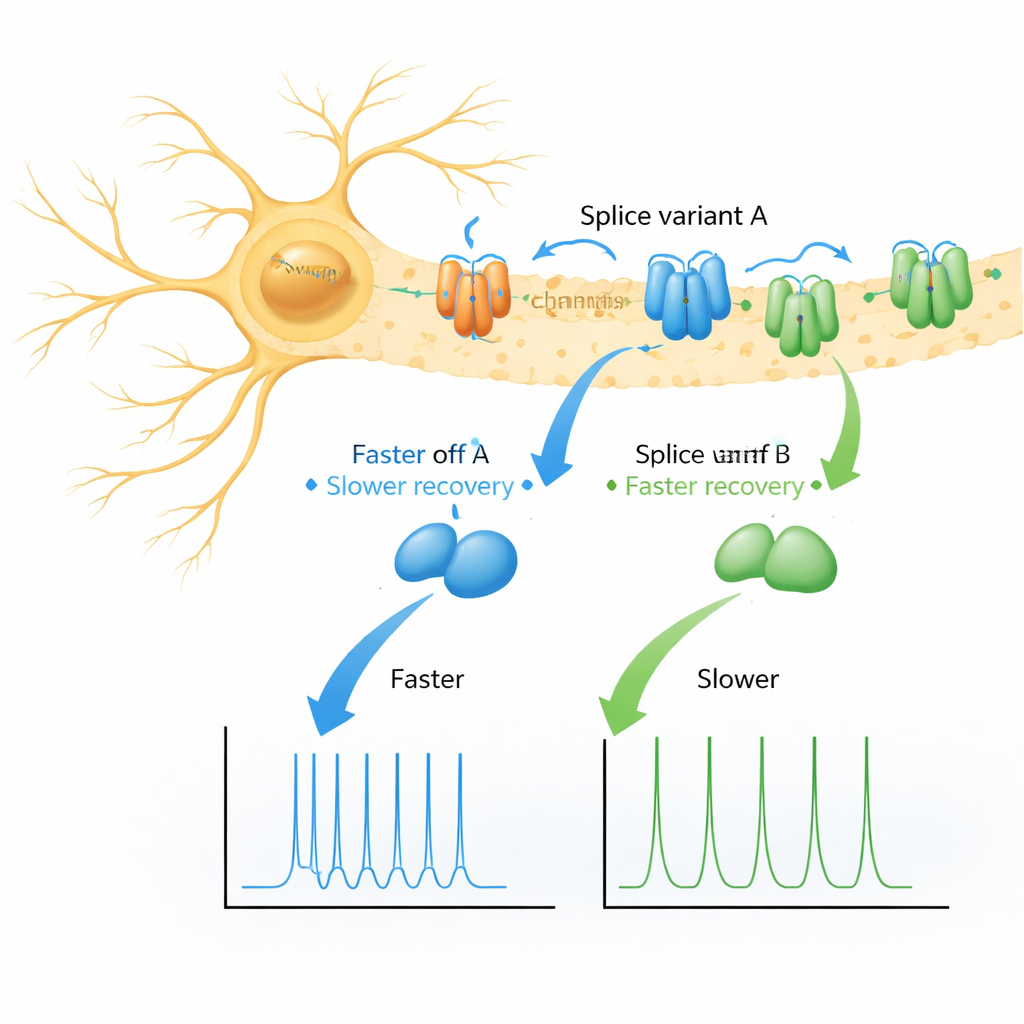
Zwei Proteinvarianten, zwei Arten der Erholung
Die Autoren konzentrierten sich auf zwei nahezu identische Versionen (Spleißvarianten) von KChIP1, genannt 1a und 1b, die sich nur durch eine kurze aromatische »Schwanz«‑Sequenz am Beginn von 1b unterscheiden. In einem kontrollierten Testsystem mit Froscheiern exprimierten sie mehrere Kv4‑Kanäle allein, mit jeder KChIP1‑Variante, mit DPP oder mit beiden Hilfsproteinen zusammen. Wie erwartet formten sowohl 1a als auch 1b das Abschaltverhalten der Kanäle bei Spannungsänderungen moderat um, ohne dramatische Effekte. Die Überraschung zeigte sich bei der Untersuchung der Erholung nach dem Abschalten: Anstatt einer einzigen, glatten Rückkehr in den Bereitschaftszustand zeigten Kanäle in Kombination mit entweder 1a oder 1b zwei deutlich getrennte Erholungsphasen — eine schnelle und eine deutlich langsamere — wobei der langsame Pfad bei 1b viel stärker ausgeprägt war.
Ein verborgener langsamer Weg tritt zutage
Wurden Kv4‑Kanäle ohne KChIP1 exprimiert, erholten sie sich über einen einfachen, schnellen Weg, und DPP beschleunigte diese Erholung zusätzlich. Die Zugabe von KChIP1 änderte dieses Muster. Mit 1a erholte sich der Großteil der Kanäle weiterhin schnell, doch ein kleiner Anteil nahm einen langsamen Umweg zurück in den Bereitschaftszustand. Mit 1b trat ein deutlich größerer Anteil diesen langsamen Pfad an, wodurch sich die Erholung auf Sekunden ausdehnte. Dieser Effekt zeigte sich in allen getesteten Kv4‑Subtypen und blieb selbst in Gegenwart von DPP erhalten, was darauf hinweist, dass der langsame Weg eine inhärente Eigenschaft von KChIP1‑haltigen Komplexen ist und kein Artefakt eines bestimmten Kanals oder Versuchsaufbaus. Die Autoren fanden außerdem, dass 1b den Abschalt‑Spannungsbereich der Kanäle zu negativeren Werten verschob, wodurch sie während andauernder Aktivität weiter inaktiviert und damit weniger verfügbar waren.
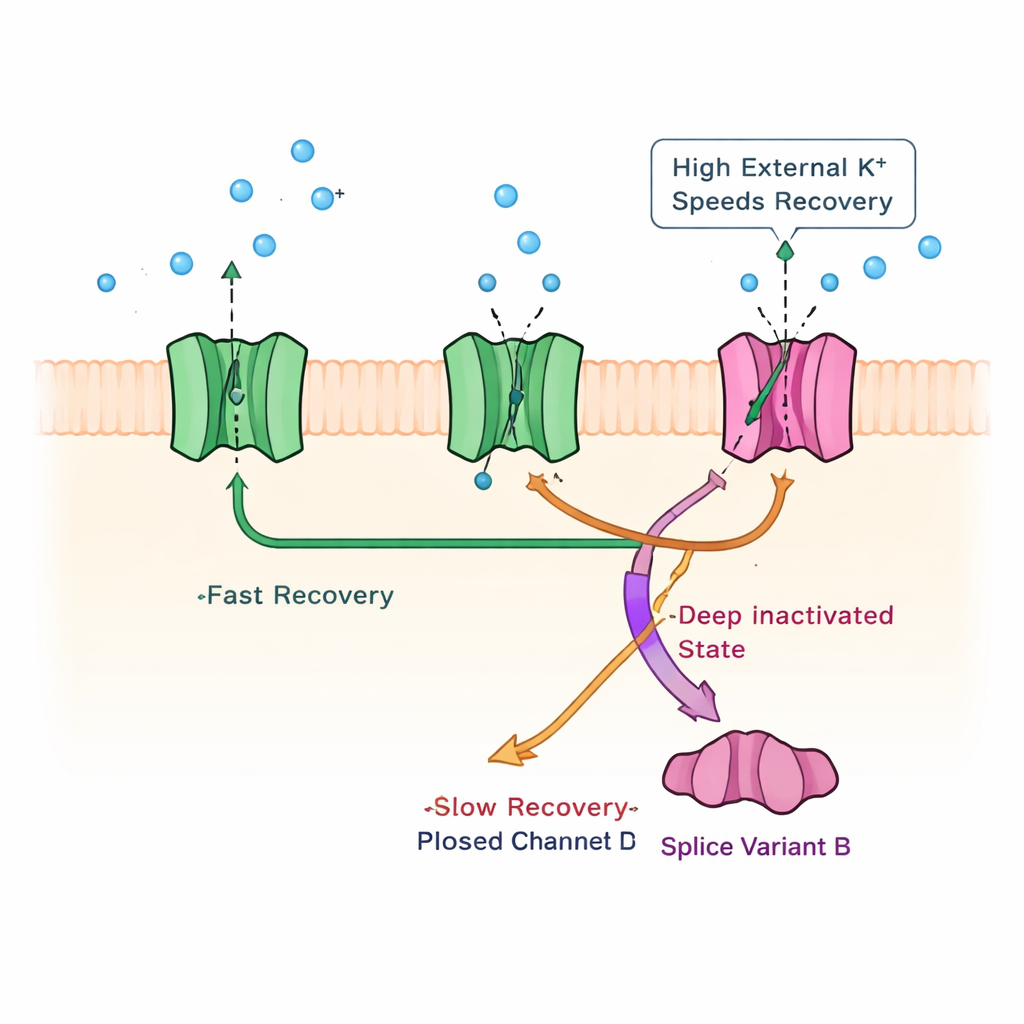
Aufdeckung eines ruhenden Inaktivierungsmechanismus
Um zu verstehen, welcher physikalische Kanalwechsel dieser langsamen Erholung zugrunde liegt, prüfte das Team bekannte Inaktivierungsmechanismen aus anderen Kaliumkanälen. Sie schlossen eine klassische »Ball‑and‑Chain«‑Blockade am inneren Kanalmund aus, indem sie Teile des inneren Schwanzes des Kanals entfernten; die langsame Phase blieb bestehen. Anschließend setzten sie hohe externe Kaliumkonzentrationen ein, einen Trick, der in anderen Kanälen eine porenbasierte Inaktivierung beeinflusst. Unter diesen Bedingungen wurde das Abschalten des Stroms schneller, aber entscheidend: die langsame Erholungsphase selbst beschleunigte sich spezifisch, als würde das hohe Kalium die Kanäle aus einem tiefen, langanhaltenden blockierten Zustand befreien. Strategische Mutationen in einem Gating‑Abschnitt des Kanals stützten zusätzlich die Idee, dass KChIP1b einen porenzentrierten Inaktivierungsweg fördert — normalerweise schwach in Kv4‑Kanälen — der koexistiert mit ihrer üblichen, schnelleren geschlossenen Zustandsinaktivierung.
Warum das für die Gehirnaktivität wichtig ist
Die Ergebnisse legen nahe, dass Neurone durch die Auswahl von KChIP1a, KChIP1b oder Mischungen aus beiden fein einstellen können, wie schnell sich A‑Typ‑Ströme zwischen Aktionspotentialen erholen. In Zellen mit viel KChIP1b wird ein erheblicher Anteil der Kv4‑Kanäle in einem tiefen, langsam umkehrbaren inaktivierten Zustand »geparkt« und steht während schneller Feuerraten nur begrenzt zur Verfügung. Das könnte bestimmten Interneuronen — Zellen, die Aktivität in neuronalen Schaltkreisen koordinieren und drosseln — erlauben, mit höheren Frequenzen oder mit spezifischen zeitlichen Mustern zu feuern. Im Kern öffnet ein kleiner Spleißunterschied in einem Hilfsprotein einen verborgenen Bremsmodus in Kaliumkanälen und fügt eine neue Flexibilitätsebene hinzu, mit der das Gehirn seine eigenen elektrischen Rhythmen steuern kann.
Zitation: Cao, W., Tachtsidis, G. & Bähring, R. KChIP1 splice variants modulate Kv4 channels by promoting P/C-type inactivation features. Sci Rep 16, 2632 (2026). https://doi.org/10.1038/s41598-026-35770-5
Schlüsselwörter: Kv4-Potassiumkanäle, KChIP1-Spleißvarianten, A‑Typ-Strom, neurale Erregbarkeit, Kanalinaktivierung