Clear Sky Science · de
Die Rolle des α7-nikotinen Acetylcholinrezeptors bei der Förderung der M2-Makrophagenpolarisation an Entzündungsstellen
Wie Nerven helfen, ausufernde Entzündungen zu beruhigen
Wenn wir uns in den Finger schneiden oder eine Infektion bekämpfen, löst unser Körper eine Entzündungsreaktion aus, um uns zu schützen. Hält diese Reaktion jedoch zu lange an, kann sie gesundes Gewebe schädigen und chronische Erkrankungen fördern. Diese Studie untersucht, wie ein spezifischer „beruhigender“ Rezeptor auf Immunzellen, der α7-nikotinerge Acetylcholinrezeptor (α7nAChR), dazu beiträgt, Entzündungen in Richtung Heilung statt Schaden zu lenken. Das liefert Hinweise für neue Therapien bei Erkrankungen wie Sepsis, Darmerkrankungen und Arthritis.
Die zwei Seiten der immunen Aufräumtruppen
Makrophagen sind Immunzellen, die als Aufräum- und Reparaturtrupps fungieren. Sie können zwischen zwei Hauptmodi wechseln. Im „Angriffs“-Modus, oft M1 genannt, setzen sie aggressive Substanzen frei, um Erreger zu töten und Ablagerungen zu entfernen. Im „Heilungs“-Modus, bekannt als M2, geben sie beruhigende Signale ab, die Entzündungen dämpfen und die Gewebereparatur fördern. Eine gesunde Reaktion beginnt mit einer Dominanz von M1-Zellen und verschiebt sich dann allmählich zugunsten von M2-Zellen, wenn die Gefahr vorüber ist. Die Autoren wollten wissen, ob α7nAChR — ein Rezeptor, der ursprünglich für seine Rolle in der Nervenkommunikation und bei den Effekten von Nikotin im Gehirn bekannt ist — auch dabei hilft, Makrophagen während einer Entzündung in diesen heilungsfördernden M2-Zustand zu steuern.
Ein nervengekoppelter Schalter in Richtung Heilung
Um das zu untersuchen, verwendeten die Forscher Mäuse, die den α7nAChR entweder hatten oder bei denen er fehlte, und lösten eine Entzündung in der Bauchhöhle auf zwei Arten aus: mit einem bakteriellen Bestandteil (als Infektionsmodell) und durch schonende Manipulation des Darms (als Modell steriler chirurgischer Verletzung). Sie bestimmten molekulare Marker, die M1 von M2 unterscheiden, und nutzten Durchflusszytometrie, um die jeweiligen Anteile der Makrophagen zu zählen. Bei normalen Mäusen dominierte in der frühen Phase der Entzündung das M1-Signal, doch im Verlauf von ein bis zwei Tagen stiegen die M2-Marker an — ein Hinweis auf den natürlichen Übergang zur Reparatur. Bei Mäusen ohne α7nAChR waren jedoch proinflammatorische Marker erhöht, Heilungsmarker reduziert, und der Anteil der M2-Makrophagen im entzündeten Bereich war konsistent verringert, wodurch das lokale Gleichgewicht zugunsten eines M1-lastigen, schädigenderen Zustands kippte.
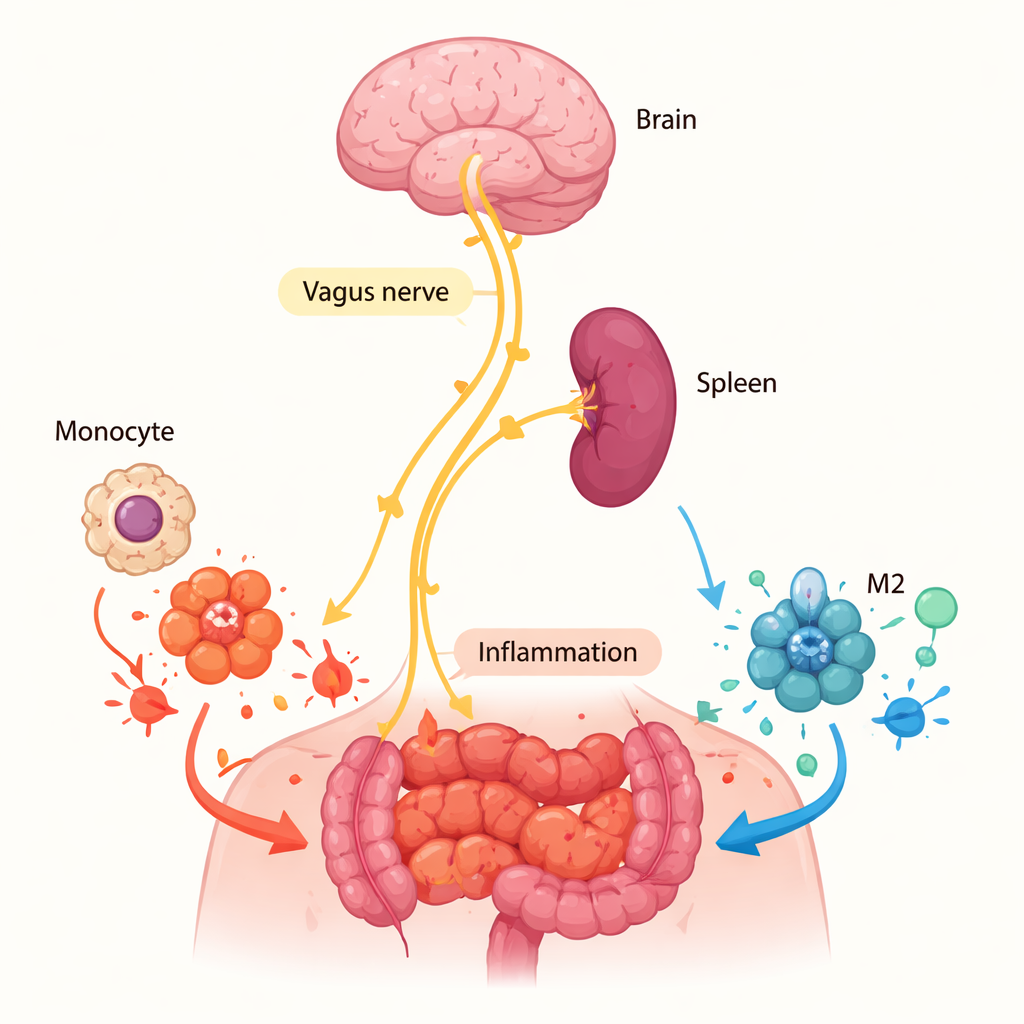
Warum die Milz wichtiger ist als die Wunde
Als Nächstes fragten die Forscher, wo α7nAChR diese Wirkung entfaltet. Der Rezeptor hätte direkt vor Ort am entzündeten Ort aktiv sein können, falls lokale Zellen Acetylcholin freisetzen, die chemische Verbindung, die den Rezeptor aktiviert. Messungen von Acetylcholin in der Bauhöhlflüssigkeit und in Zellkulturen aus dem entzündeten Gewebe ergaben jedoch im Wesentlichen nichts, was gegen ein starkes lokales Signal spricht. Stattdessen richtete sich die Aufmerksamkeit auf die Milz, ein zentrales Immunorgan, das bereits dafür bekannt ist, am „cholinergen antiinflammatorischen Weg“ unter Kontrolle des Vagusnervs beteiligt zu sein. Als die Forscher die Milz normaler Mäuse chirurgisch entfernten und dann eine Bauchhöhlenentzündung auslösten, sank der Anteil der M2-Makrophagen in der Peritonealhöhle, und die Gesamtzahl der Makrophagen nahm ab. Dieses Muster spiegelte das Verhalten der Mäuse ohne α7nAChR wider und legt nahe, dass nervengesteuerte Signale in der Milz Monozyten — die Vorläufer der Makrophagen — bereits vor ihrer Ankunft im entzündeten Gewebe darauf vorbereiten, zu M2-Zellen zu werden.
Den Schalter an menschlichen Zellen testen
Um zu prüfen, ob derselbe Rezeptor menschliche Zellen beeinflussen kann, nutzten die Wissenschaftler im Labor gezüchtete Monozyten aus einer Leukämie-Zelllinie (THP-1) und aus gespendetem menschlichem Blut. Sie leiteten diese Zellen standardmäßig zur Entwicklung in entweder M1- oder M2-Makrophagen und setzten anschließend ein spezifisches α7nAChR-aktivierendes Medikament zu. In beiden menschlichen Zellquellen erhöhte die Aktivierung von α7nAChR nicht die M1-Marker, wohl aber deutlich wichtige Kennzeichen der M2-Aktivität, einschließlich des Oberflächenproteins CD206 und des antiinflammatorischen Moleküls Interleukin-10. Diese Experimente stützen die Idee, dass α7nAChR wie ein biasierender Schalter wirkt und es entwickelnden Makrophagen erleichtert, eine heilungsorientierte Identität anzunehmen, ohne die Immunantwort insgesamt einfach abzuschalten.
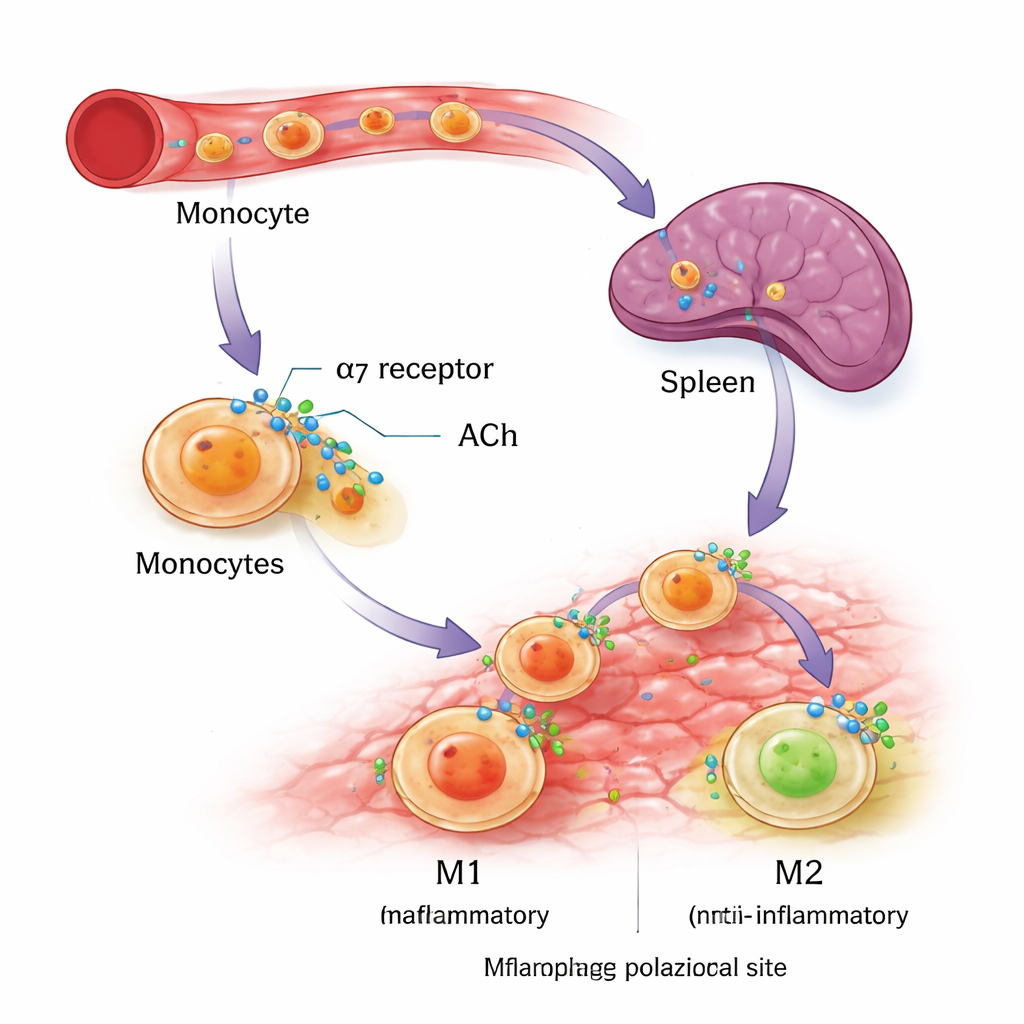
Von Nikotin-Hinweisen zu zukünftigen Therapien
Die Ergebnisse helfen, mehrere rätselhafte Beobachtungen zu erklären, etwa warum die Stimulation des Vagusnervs Entzündungskrankheiten verbessern kann und warum Raucher — trotz vieler Gesundheitsrisiken — offenbar ein etwas geringeres Risiko für bestimmte Darmerkrankungen haben; Nikotin kann α7nAChR aktivieren. Anstatt nur entzündungsfördernde Chemikalien zu blockieren, scheint α7nAChR dem Körper zu helfen, seine immunen Aufräumtrupps in stärker reparaturorientierte M2-Zellen umzuwandeln, insbesondere durch milzbasierte Schulung von Monozyten. Für Laien bedeutet das: Unser Nervensystem tut mehr, als nur Schmerz zu registrieren oder Muskeln zu steuern; es coacht auch stillschweigend Immunzellen, wann sie kämpfen und wann sie heilen sollen. Zu lernen, wie man diesen eingebauten Schalter sicher mit Medikamenten oder gezielter Nervenstimulation umlegt, könnte neue Wege eröffnen, schädliche Entzündungen zu beruhigen und gleichzeitig die Abwehrfähigkeit des Körpers zu erhalten.
Zitation: Mihara, T., Tanabe, H., Nonoshita, Y. et al. The role of the α7 nicotinic acetylcholine receptor in promoting M2 macrophage polarization at inflammatory sites. Sci Rep 16, 5267 (2026). https://doi.org/10.1038/s41598-026-35757-2
Schlüsselwörter: Makrophagenpolarisation, Entzündung, Vagusnerv, nikotinerger Acetylcholinrezeptor, Immunregulation