Clear Sky Science · de
Physiologisch relevante Formen von Tc‑ und Re‑Pyrophosphat-Radiotracern und die Grundlage ihrer Sensitivität gegenüber Transthyretin‑Amyloid
Warum diese Herzbildgebungsgeschichte wichtig ist
Viele Menschen bilden mit dem Alter stille Ablagerungen fehlgefalteter Proteine, sogenannte Amyloide, im Herzen. Einige dieser Ablagerungen, insbesondere solche aus einem Blutprotein namens Transthyretin, können das Herz versteifen und zu schwerwiegenden Erkrankungen führen. Ärztinnen und Ärzte stützen sich zunehmend auf einen radioaktiven Radiotracer, bekannt als Technetium‑99m‑Pyrophosphat (99mTc‑PYP), um diese Ablagerungen in Untersuchungen sichtbar zu machen. Überraschenderweise war jedoch bislang unklar, welche konkrete Form dieser Tracer im Körper annimmt und warum er offenbar bestimmte Amyloid‑Typen „bevorzugt“. Diese Arbeit kombiniert Theorie und Experiment, um aufzudecken, wie der Tracer unter physiologischen Bedingungen tatsächlich aussieht und wie diese Gestalt ihm möglicherweise erlaubt, sich an schädliche Transthyretin‑Fibrillen anzulagern.
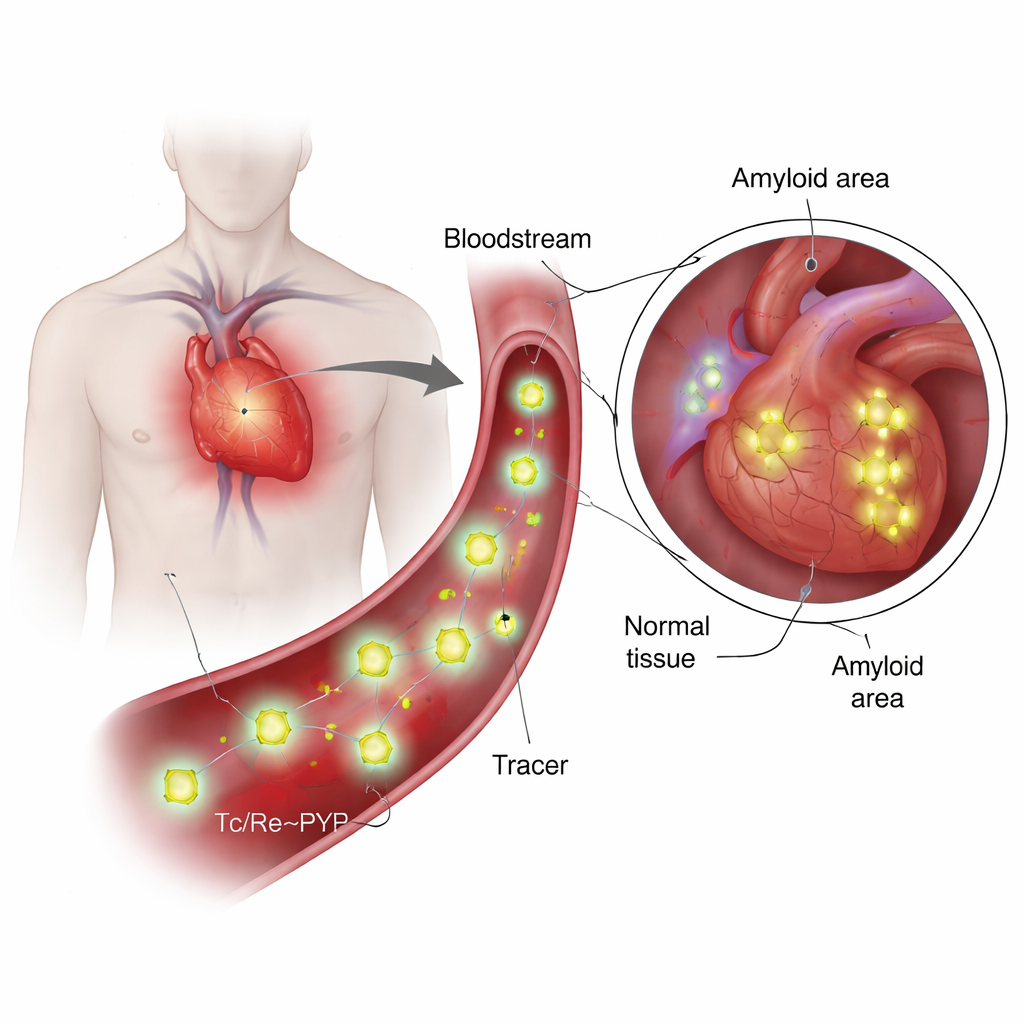
Was sind diese Tracer und warum sind sie besonders?
99mTc‑PYP wird seit Jahrzehnten zur Bildgebung von Knochen verwendet, weil es sich dort anreichert, wo Kalzium und Mineralumsatz hoch sind. Neuerdings entdeckten Ärztinnen und Ärzte, dass es auch zwischen zwei Hauptformen der kardialen Amyloidose unterscheiden kann: einer aus Leichtketten der Antikörper (AL) und einer aus Transthyretin (ATTR). Bei ATTR leuchtet das Herz in PYP‑Scans oft stark auf, während AL‑Fälle meist schwach bleiben, selbst wenn Kalziumablagerungen ähnlich erscheinen. Diese Diskrepanz warf eine zentrale Frage auf: Haftet der Tracer nur an Kalzium oder interagiert er direkt mit dem Amyloidprotein? Die Antwort erfordert Kenntnis der wahren chemischen Struktur des Tracers unter blutähnlichen Bedingungen — etwas, das frühere Arbeiten nur grob skizziert hatten.
Ein sicherer Stellvertreter, um das Unsichtbare zu sehen
Da Technetium radioaktiv ist und in medizinischen Präparaten nur in winzigen Mengen vorkommt, ist es mit vielen Labormethoden schwer direkt zu untersuchen. Die Autorinnen und Autoren nutzten daher Rhenium, ein eng verwandtes Element mit nahezu identischer Größe und ähnlichen Bindungsvorlieben, dessen Chemie aber handhabbarer ist. Sie stellten Rhenium‑Pyrophosphat‑Mischungen unter Bedingungen her, die klinische PYP‑Kits nachahmen, und untersuchten sie mit einem Bündel von Methoden: hochrangigen Quantenchemie‑Berechnungen, UV‑sichtbarer Lichtabsorption, verschiedenen Vibrationsspektroskopien (Infrarot und Raman), Kernspinresonanz, Massenspektrometrie und Zinn‑Mössbauer‑Spektroskopie. Zusammen ermöglichten diese Techniken, viele Kandidatenstrukturen zu prüfen und einzugrenzen, welche Spezies bei neutralem pH‑Wert, wie im Blut, wahrscheinlich vorhanden sind.
Eine flexible, aber erkennbare molekulare Gestalt
Die gesammelten Befunde deuten auf eine gemeinsame „Kern“-Struktur hin: ein oktaedrisches Komplex in dem ein Technetium‑ oder Rhenium‑Atom im Oxidationszustand +4 an zwei Pyrophosphatgruppen und zwei Wassermoleküle gebunden ist. Vereinfacht gesagt sitzt das Metall im Zentrum eines nahezu oktaedrischen Käfigs aus Sauerstoffatomen, wobei die Pyrophosphate als mehrzähnige Anker wirken und die Wassermoleküle die verbleibenden Positionen besetzen. Diese grundlegende Diaqua‑Dipyrophosphat‑Einheit ist nicht starr. Weil sich die Pyrophosphat‑Arme verdrehen und innere Wasserstoffbrücken mit den gebundenen Wassern ausbilden können, nimmt das Molekül in Lösung viele leicht unterschiedliche Formen ein. Rechnungen und Spektren legen nahe, dass diese Variationen seine Lichtabsorptions‑ und Vibrationsmarken verschieben, was erklärt, warum experimentelle Banden breit sind und warum frühere Studien Mühe hatten, eine einzige klare Struktur festzulegen.
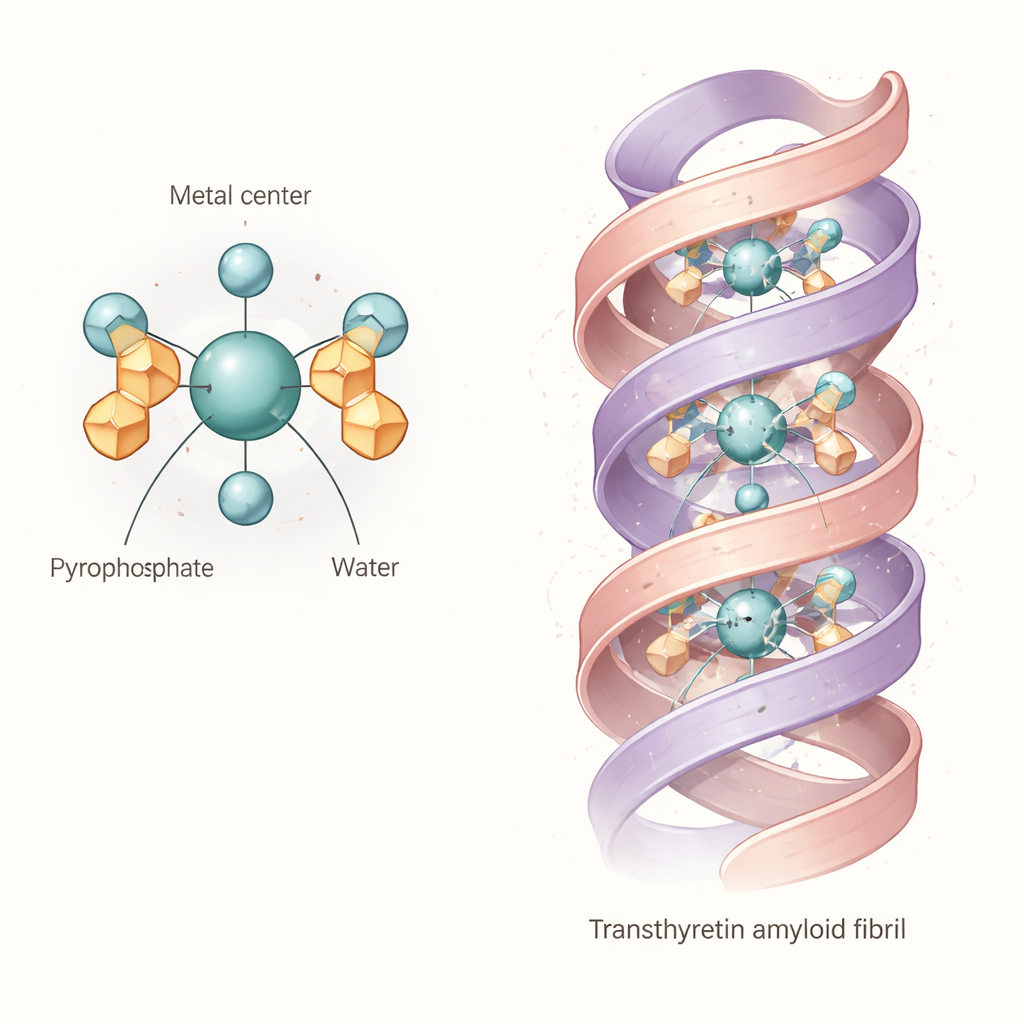
Was das für die Bindung an Herz‑Amyloid bedeutet
Die Autorinnen und Autoren fragten anschließend, ob sich dieser flexible Komplex plausibel direkt in Transthyretin‑Amyloid‑Fibrillen einlagern könnte. Unter Verwendung einer detaillierten Kryo‑Elektronenmikroskopie‑Struktur einer menschlichen Transthyretin‑Fibrille führten sie computergestützte Docking‑Suchen mit dem modellierten Technetium‑Pyrophosphat‑Komplex durch. Die Ergebnisse zeigen, dass die Diaqua‑Dipyrophosphat‑Einheit in einen zentralen Kanal entlang der Fibrille passen kann und dabei mehrere Wasserstoffbrücken und Salzbrücken mit geladenen Seitenketten ausbildet, die die Höhlung säumen. Das deutet darauf hin, dass der Tracer — zumindest für manche Transthyretin‑Fibrilformen — nicht nur benachbarte Mineralablagerungen markiert, sondern vom Proteingerüst selbst direkt gefasst werden kann. Die strukturelle „Nachgiebigkeit“ des Tracers hilft ihm wahrscheinlich, sich an leicht unterschiedliche Taschen und Ladungsmuster in realen Patientenfibrillen anzupassen.
Folgen für Diagnostik und künftige Tracer
Für eine fachferne Leserin oder einen fachfernen Leser lautet die Quintessenz: Der weit verbreitete PYP‑Herzscan beruht auf einem Tracer, der subtiler und proteinbewusster ist als bislang angenommen. Unter physiologischen Bedingungen ist er am besten als kleine, wasserhaltige Metall‑Pyrophosphat‑Kapsel zu verstehen, die sich verformen und multiple Kontaktpunkte mit Transthyretin‑Amyloidkanälen ausbilden kann. Diese Einsicht hilft zu erklären, warum der Tracer in einigen Amyloid‑Erkrankungen starke Signale zeigt, in anderen jedoch nicht, und warum winzige Veränderungen im Protein oder seiner Umgebung zu unerwarteten Sensitivitätsverlusten führen können. Durch die Klärung von Gestalt und Ladungsmuster des Tracers schafft die Studie eine Grundlage für das Design nächster Generationen von Bildgebungs‑ oder therapeutischen Agenzien, die krankheitsverursachende Fibrillen im Herzen und darüber hinaus selektiver erkennen.
Zitation: Simon, K.Z., Béres, K.A., Farkas, A. et al. Physiologically relevant forms of Tc- and Re-pyrophosphate radioactive tracers and the basis of their transthyretin amyloid sensitivity. Sci Rep 16, 6111 (2026). https://doi.org/10.1038/s41598-026-35746-5
Schlüsselwörter: Kardiale Amyloidose, Transthyretin, Technetium‑Pyrophosphat, Molekulare Bildgebung, Radiotracer‑Chemie