Clear Sky Science · de
Synergistische antipersister-, Efflux‑hemmende und antibiofilm‑Aktivitäten von vaginalen Lactobacillus‑abgeleiteten Postbiotika gegen UPEC: hin zu einer neuartigen Therapie für Harnwegsinfekte
Warum hartnäckige Harnwegsinfekte wichtig sind
Harnwegsinfektionen (HWI) gehören zu den häufigsten bakteriellen Infektionen, insbesondere bei Frauen, und viele Betroffene leiden wiederholt darunter, obwohl sie Antibiotika einnehmen. Diese Studie untersucht einen neuen, antibiotikasparenden Ansatz zur Bekämpfung dieser hartnäckigen, rezidivierenden Infektionen: die Nutzung nützlicher vaginaler Bakterien und ihrer chemischen Nebenprodukte, um problematisches E. coli zu stoppen, bevor es sich festsetzt, sich versteckt und wieder auflebt.
Die verborgenen Überlebenden hinter wiederkehrenden Infektionen
Konventionelle Antibiotika können die meisten Bakterien abtöten, doch eine winzige Subpopulation, sogenannte „Persister‑Zellen“, überlebt, indem sie in einen ruhenden, wenig aktiven Zustand wechselt. Diese Schläfer sind nicht genetisch resistent, tolerieren jedoch sehr hohe Antibiotikadosen und können später wieder aktiv werden, wodurch chronische und wiederkehrende HWI entstehen. Die Forschenden arbeiteten mit einem häufigen HWI‑verursachenden Stamm, E. coli UTI89, und zeigten, dass potente Antibiotika wie Colistin und Meropenem leicht Persister‑Zellen auslösen. In Laborversuchen, die Urin nachahmen, überdauerten kleine Bruchteile von E. coli extreme Antibiotikabelastungen, was bestätigt, wie leicht Persister entstehen und warum Standardtherapien oft nicht für anhaltende Linderung sorgen.
Freundliche vaginale Bakterien in eine Behandlung verwandeln
Eine gesunde Vagina wird meist von Lactobacillus‑Arten dominiert, die helfen, schädliche Mikroben in Schach zu halten. Statt lebende „Probiotika“ zu verwenden, konzentrierte sich diese Studie auf deren zellfreies Überstandsmaterial — im Wesentlichen der Cocktail aus von ihnen abgegebenen Molekülen, sogenannte Postbiotika. Aus vaginalen Lactobacillus‑Stämmen gesunder Frauen separierte und analysierte das Team diese sekretorischen Verbindungen. Zwei Schlüsselmetaboliten, Itaconsäureanhydrid und (−)-Terpinen‑4‑ol, fielen durch ihre Fähigkeit auf, zusammenzuarbeiten und die Anzahl der E. coli‑Persister‑Zellen in Kombination mit Antibiotika deutlich zu reduzieren. Eine dritte Verbindung, Tryptamin, die zuvor gezeigt hatte, dass sie die schleimige Biofilm‑Matrix abbaut, wurde hinzugefügt, um die antibiofilmische Wirkung zu verstärken.
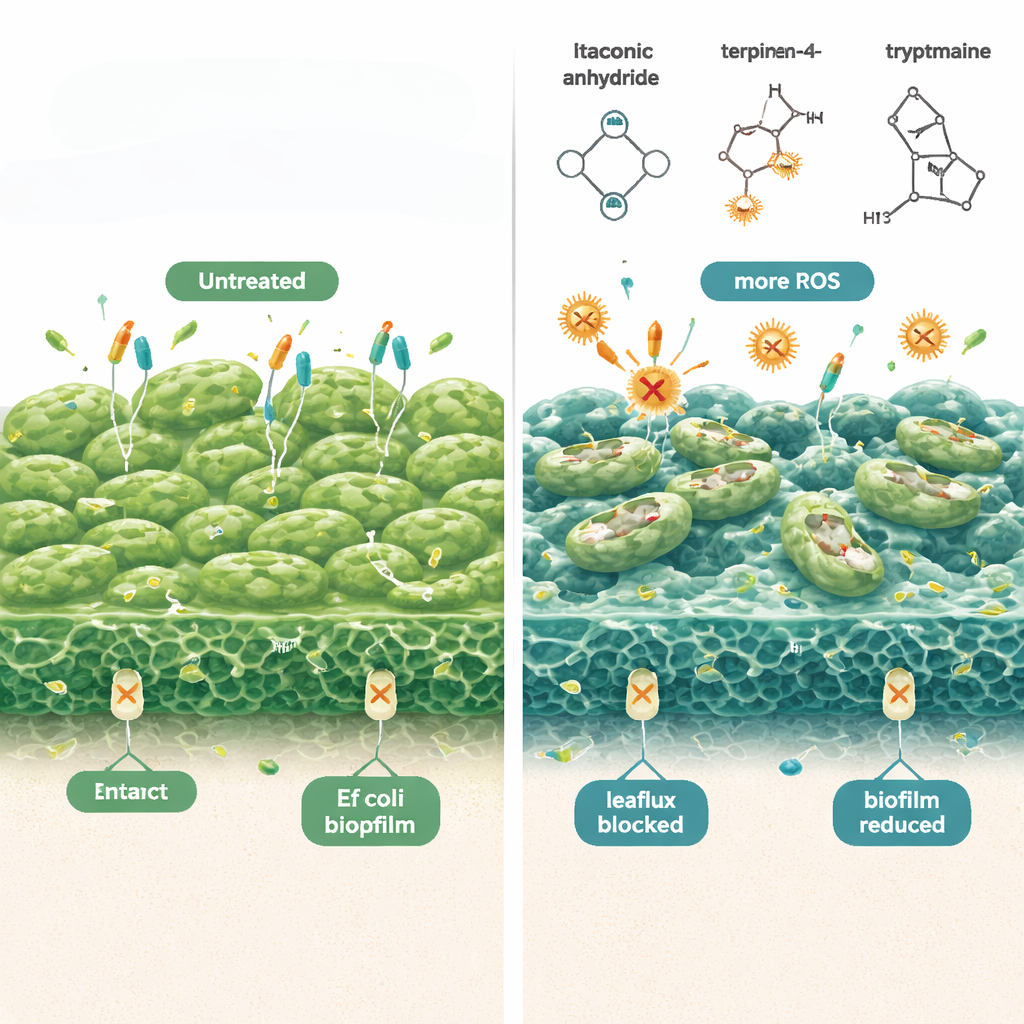
Wie die neue Mischung schwer zu tötende Bakterien schwächt
Die Wissenschaftler stellten fest, dass diese aus Lactobacillus stammenden Moleküle E. coli‑Persister auf mehreren Ebenen gleichzeitig angreifen. Erstens erhöhen sie die Produktion reaktiver Sauerstoffspezies — chemisch reaktive Formen von Sauerstoff, die bakterielle Bestandteile schädigen — und machen Antibiotika für ruhende Zellen wesentlich tödlicher. Als Antioxidantien hinzugefügt wurden, verringerte sich dieser abtötende Effekt, was die Rolle von oxidativem Stress unterstreicht. Zweitens machen die Verbindungen die bakterielle Außenmembran „leckager“, wie Fluoreszenzfärbemittel zeigten, die nach der Behandlung leichter in Zellen eindringen. Drittens hemmen sie zelluläre „Effluxpumpen“, winzige Exportmaschinen, die normalerweise Antibiotika wieder aus der Zelle pumpen. Mit blockierten Pumpen verbleibt mehr Wirkstoff im Inneren der Bakterien, und weniger Persister überleben. Zusammengenommen reduzierten diese Veränderungen vorgeformte E. coli‑Biofilme in Labortests um bis zu zehn Größenordnungen, ohne die getesteten Säugetier‑Immunzellen bei den verwendeten Dosen zu schädigen.
Vom Labortisch zu einem praktischen Vaginalwaschmittel
Um diese Erkenntnisse in etwas Alltagsbrauchbares zu überführen, entwickelte das Team ein angepasstes Vaginalwaschmittel auf Basis eines thermosensitiven Gelträgers, Poloxamer 407. Bei Raumtemperatur verhält es sich flüssig für eine einfache Anwendung und verdickt sich bei Körpertemperatur leicht, um den Kontakt mit den Vaginalwänden zu verbessern. Das Gel enthält eine definierte, sichere Kombination aus Itaconsäureanhydrid, (−)-Terpinen‑4‑ol und Tryptamin. In Laborplatten funktionierte diese Formulierung über einen pH‑Bereich, der vaginalen Bedingungen ähnelt, unterdrückte stark die E. coli‑Biofilmbildung und verringerte die Zahl lebender Bakterien um etwa neun Größenordnungen. Sie blieb bei kalter Lagerung mindestens drei Monate stabil und biologisch aktiv und zeigte außerdem eine breite Wirkung gegen andere problematische Bakterien wie Klebsiella, MRSA und Pseudomonas.
Sicherheits‑ und Schutztests an Mäusen
Als Nächstes bewerteten die Forschenden das Waschmittel in einem Mausmodell für vaginale E. coli‑Infektionen. Mäuse wurden mit leuchtenden (GFP‑markierten) E. coli inokuliert und dann entweder mit dem neuen Metaboliten‑Waschmittel, einem Probiotika‑Waschmittel mit lebenden Lactobacillus, einem kommerziellen Vaginalwaschmittel oder einer Placebo‑Basis behandelt. Tiere, die das zugeschnittene Metaboliten‑Waschmittel erhielten, zeigten deutlich weniger vaginale Entzündung, behielten ihr Körpergewicht und wiesen im Vaginalsekret dramatisch niedrigere Bakterienzahlen auf als die anderen Gruppen. Am auffälligsten war, dass bei den behandelten Mäusen kein nachweisbares E. coli im Urin, in Blase, Nieren oder Vaginalgewebe gefunden wurde und die Nierenfunktion normal blieb, was darauf hindeutet, dass die Formulierung nicht nur die lokale Infektion reduzierte, sondern auch eine Ausbreitung in die oberen Harnwege verhinderte.
Was das für Menschen mit wiederkehrenden HWI bedeuten könnte
Die Studie kommt zu dem Schluss, dass ein Vaginalwaschmittel, aufgebaut aus präzisen Metaboliten natürlicherweise schützender Lactobacillus‑Arten, UTI‑verursachendes E. coli auf mehreren Ebenen schwächen kann: Verringerung der Persister‑Populationen, Störung von Biofilmen und Verbesserung der Wirksamkeit standardmäßiger Antibiotika. Da der Ansatz auf nicht‑lebenden Molekülen statt auf lebenden Bakterien oder langen systemischen Medikamentenkuren beruht, könnte er sicherer, stabiler und leichter regulierbar sein. Während noch klinische Studien am Menschen erforderlich sind, deutet dieses metabolitbasierte Waschmittel auf eine Zukunft hin, in der wiederkehrende HWI nicht nur durch stärkere Antibiotika, sondern durch das gezielte Stärken der eigenen mikrobiellen Abwehr an der Quelle verhindert werden.
Zitation: Nair, V.G., Chellappan, D.R., Durai, R.D. et al. Synergistic antipersister, efflux inhibitory & antibiofilm activities of vaginal Lactobacillus-derived postbiotics against UPEC: toward a novel therapeutic for utis. Sci Rep 16, 5005 (2026). https://doi.org/10.1038/s41598-026-35736-7
Schlüsselwörter: Harnwegsinfektion, vaginales Mikrobiom, Lactobacillus‑Postbiotika, Antibiotika‑Toleranz, bakterielle Biofilme