Clear Sky Science · de
Gehirnorganoid-Modelle der SZT2-assoziierten Erkrankung zeigen eine Überproduktion von äußeren radialen Gliazellen durch Aktivierung von mTORC1
Wenn das Gehirnwachstum außer Kontrolle gerät
Warum entwickeln manche Kinder ungewöhnlich große Köpfe, Anfälle und schwere Entwicklungsverzögerungen? Diese Studie geht der Frage nach einer seltenen genetischen Erkrankung nach, die mit dem Gen SZT2 verknüpft ist. Mithilfe winziger, im Labor erzeugter „Mini-Gehirne“ aus Stammzellen zeigen die Forschenden, wie ein defekter Wachstumsregler dazu führen kann, dass bestimmte Gehirnstammzellen überproduziert werden — ein möglicher Erklärungsansatz für das beobachtete Gehirnüberwachstum und die Verdrahtungsprobleme bei betroffenen Kindern.
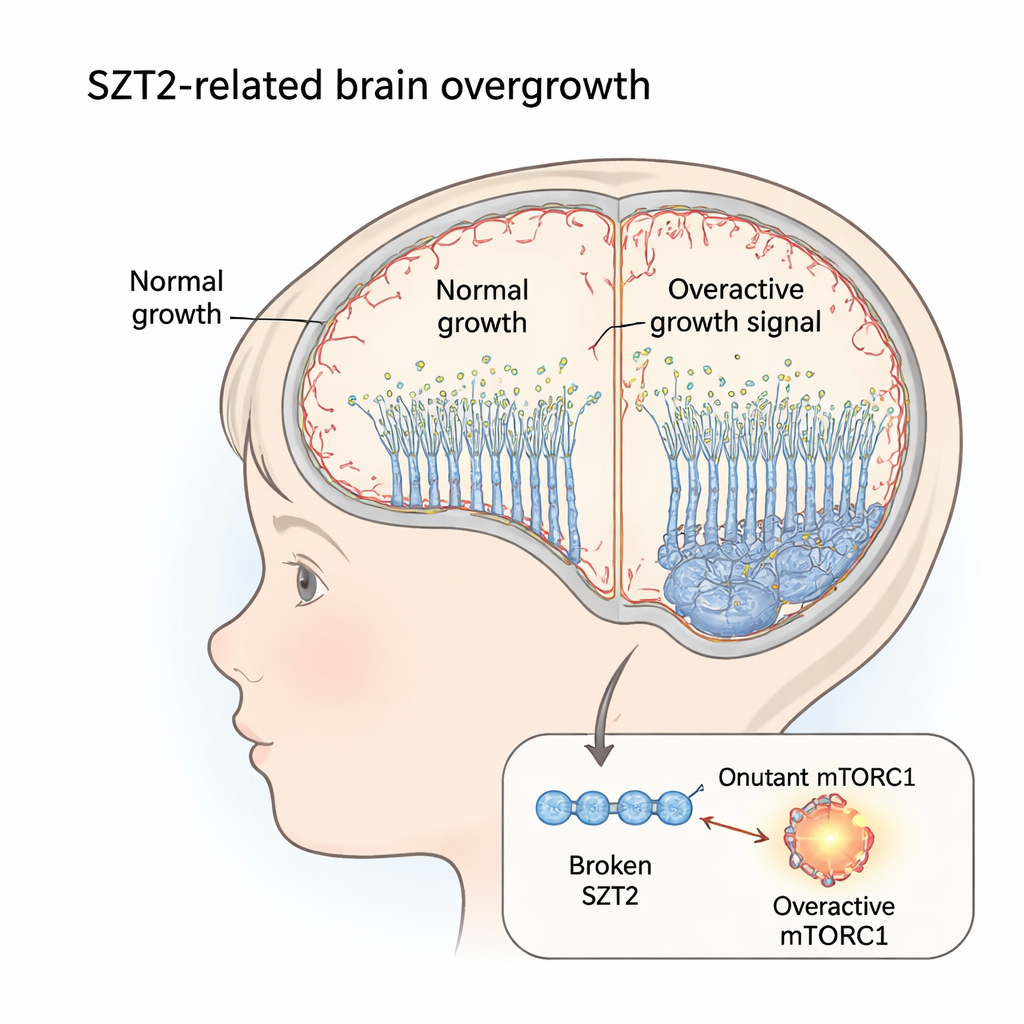
Bremse des Wachstums im Gehirn defekt
Das SZT2-Gen hilft normalerweise, einen starken Wachstumsweg, bekannt als mTORC1, unter Kontrolle zu halten. Wenn beide Kopien von SZT2 beschädigt sind, können Kinder Epilepsie, geistige Behinderung und Makrozephalie — einen ungewöhnlich großen Kopf — entwickeln. Frühere Arbeiten zeigten, dass Zellen dieser Patient:innen mTORC1 im dauerhaft „eingeschalteten“ Zustand haben. Unklar blieb jedoch, wie sich dies während der frühen menschlichen Gehirnentwicklung auswirkt, wenn die grundlegende Struktur und Größe der Großhirnrinde festgelegt werden.
Mini-Gehirne bauen, um die Krankheit zu modellieren
Um das direkt im menschlichen Gewebe zu untersuchen, verwendete das Team induzierte pluripotente Stammzellen, die sich in nahezu jeden Zelltyp verwandeln lassen. Sie bearbeiteten das SZT2-Gen in diesen Zellen mit CRISPR/Cas9 und erzeugten eine mutierte Version, die eine kleine, aber entscheidende Proteinstrecke vermissen lässt. Diese editieren Zellen und unveränderte Kontrollzellen wurden zu dreidimensionalen Gehirnorganoiden kultiviert — kugelförmigen Strukturen, die wichtige Schritte der frühen Gehirnentwicklung nachahmen, einschließlich der Ausbildung geschichteter Zonen und der Neuronenproduktion. Die Organoide beider Gruppen entwickelten sich insgesamt ähnlich und zeigten dieselbe grundlegende Identität wie das sich entwickelnde menschliche Vorderhirn.
Mehr Stammzellen in der Wachstumszone des Gehirns
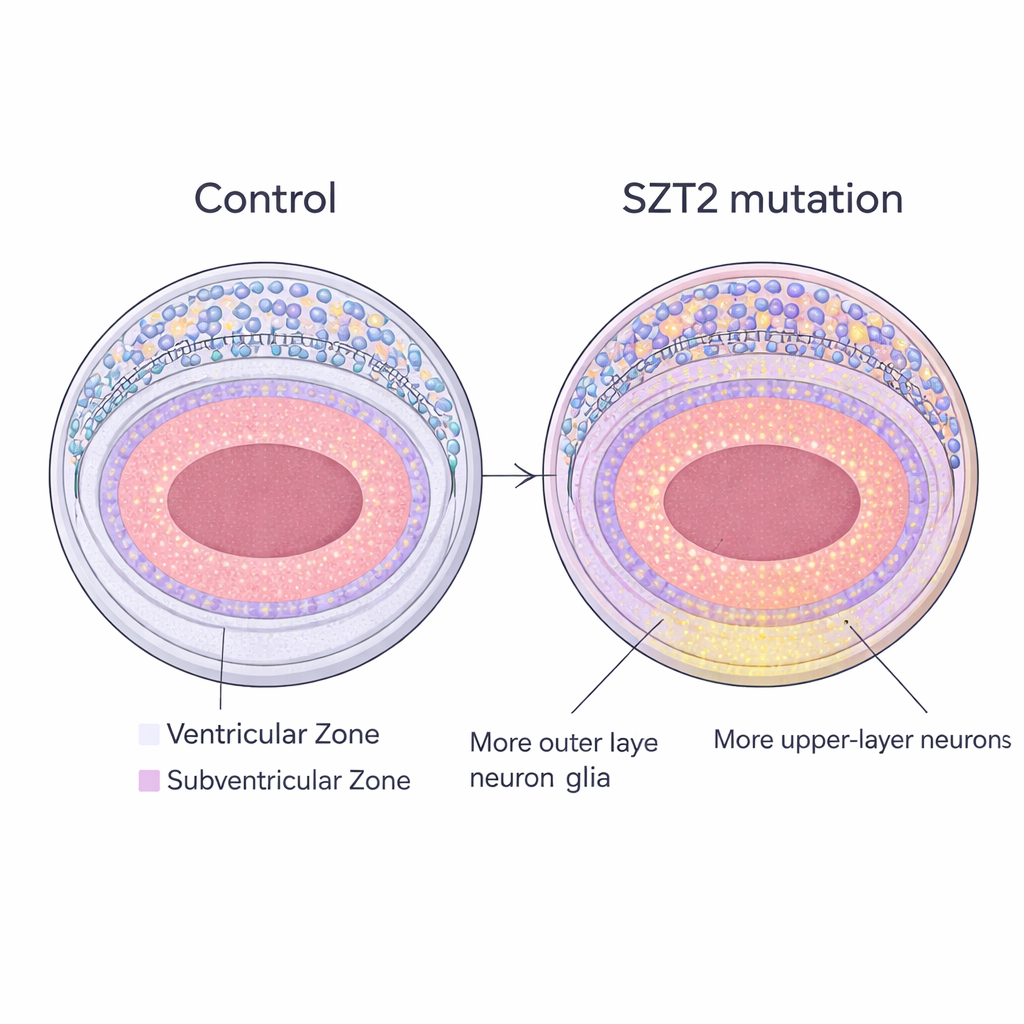
Im Inneren jedes Mini-Gehirns richteten die Forschenden ihr Augenmerk auf zwei Schlüsselregionen: die innere Ventrikelzone, reich an Stammzellen, die eine flüssigkeitsgefüllte Höhle auskleiden, und die äußere Subventrikularzone (SVZ), in der ein spezieller Typ von Stammzellen, die äußeren radialen Gliazellen, angesiedelt ist. Diese äußeren radialen Gliazellen sind beim Menschen besonders zahlreich und gelten als Motor für die Vergrößerung und Faltung unseres großen Gehirns. In den SZT2-mutanten Organoiden war die SVZ im Verhältnis zur inneren Zone vergrößert und enthielt deutlich mehr äußere radiale Gliazellen als in den Kontrollen. Wichtig ist, dass eine andere Vorläuferzellpopulation in derselben Region nicht zunahm, was auf eine spezifische Verstärkung gerade dieser beim Menschen expandierten Stammzellpopulation hinweist.
Von zusätzlichen Stammzellen zu zusätzlichen Neuronen
Das Team blickte dann weiter nach außen, auf die der kortikalen Platte ähnliche Schicht, in der Neuronen ihre Position einnehmen. Dort zählten sie zwei Haupttypen von Neuronen: Tiefenschichtneuronen und Oberflächenschichtneuronen, die später gebildet werden und für die Langstreckenkommunikation zwischen Gehirnregionen wichtig sind. In den SZT2-mutanten Organoiden war die Zahl der Oberflächenschichtneuronen deutlich erhöht, während die Tiefenschichtneuronen etwa gleich blieben. Dieses Muster passt zu aktuellen Modellen, nach denen äußere radiale Gliazellen vor allem Oberflächenschichtneurone hervorbringen. Interessanterweise fanden die Forschenden nicht insgesamt mehr teilende Zellen, was darauf hindeutet, dass die Veränderung eher aus einer veränderten Schicksalsentscheidung oder Entwicklungsprogression der Stammzellen resultiert als aus einer bloß erhöhten Teilungsrate.
Ein hyperaktives Signal, das behandelbar sein könnte
Um diese strukturellen Veränderungen mit dem Wachstumsregulator in Verbindung zu bringen, maßen die Wissenschaftler:innen einen Marker für mTORC1-Aktivität. Sie fanden eine stärkere mTORC1-Signalgebung nicht nur in der SVZ, wo äußere radiale Glia sitzen, sondern auch in der inneren Zone und der neuronreichen äußeren Schicht der SZT2-mutanten Organoide. Das stützt die Vorstellung, dass SZT2 in der frühen Gehirnentwicklung als Bremse für mTORC1 wirkt; versagt diese Bremse, dehnen sich die äußeren radialen Gliazellen aus, es werden mehr Oberflächenschichtneurone produziert, und die Großhirnrinde kann unnormal groß und fehlverdrahtet werden. Die Autor:innen weisen darauf hin, dass derselbe Signalweg durch vorhandene mTOR-blockierende Medikamente abgeschwächt werden kann, was die Möglichkeit eröffnet — die noch geprüft werden muss — dass zeitlich abgestimmte Behandlungen eines Tages helfen könnten, SZT2-assoziierte Störungen zu behandeln.
Was das für Patient:innen und Familien bedeutet
Einfach ausgedrückt legt diese Studie nahe, dass ein defektes SZT2-Gen ein zentrales Wachstumssignal im sich entwickelnden Gehirn überhitzen lässt. Dieses übermäßige Signal scheint eine spezifische Gruppe menschlicher Stammzellen zur Überproduktion zu treiben, was zu einer übergroßen und potenziell fehlvernetzten Großhirnrinde führen kann, die der Ursache für große Kopfgröße, Balkenanomalien und Anfälle zugrunde liegen könnte. Obwohl die Arbeit in im Labor gezüchteten Mini-Gehirnen aus einer einzigen Zelllinie durchgeführt wurde und daher noch keine Vorhersagen für einzelne Kinder erlaubt, liefert sie den ersten direkten, am Menschen basierten Nachweis, der SZT2-Fehlfunktion mit frühem Gehirnüberwachstum verbindet. Sie weist außerdem auf mTOR-blockierende Medikamente als einen begründeten Forschungsweg für mögliche zukünftige Therapien hin.
Zitation: Sato, E., Nakamura, Y., Fujimoto, M. et al. Brain organoid models of SZT2-related disease reveal an overproduction of outer radial glial cells through mTORC1 activation. Sci Rep 16, 5193 (2026). https://doi.org/10.1038/s41598-026-35733-w
Schlüsselwörter: Gehirnorganoide, mTORC1, SZT2, Makrozephalie, äußere radiale Glia