Clear Sky Science · de
Prognostische Bedeutung räumlicher Nischen beim Prostatakrebs
Warum die „Nachbarschaften“ des Tumors wichtig sind
Prostatakrebs ist häufig, aber nicht alle Tumoren verhalten sich gleich. Manche wachsen langsam, andere schreiten schnell voran und gefährden das Leben der Betroffenen. Ärztinnen und Ärzte stützen sich derzeit auf Marker wie PSA‑Werte und histologische Grade, um einzuschätzen, welche Tumoren gefährlich sind. Diese Studie stellt eine neue Frage: Kann der genaue Ort, an dem Krebszellen innerhalb eines Tumors vorkommen – der geschäftige äußere Rand versus der tiefere Kern – dabei helfen, das Patientenoutcome vorherzusagen?
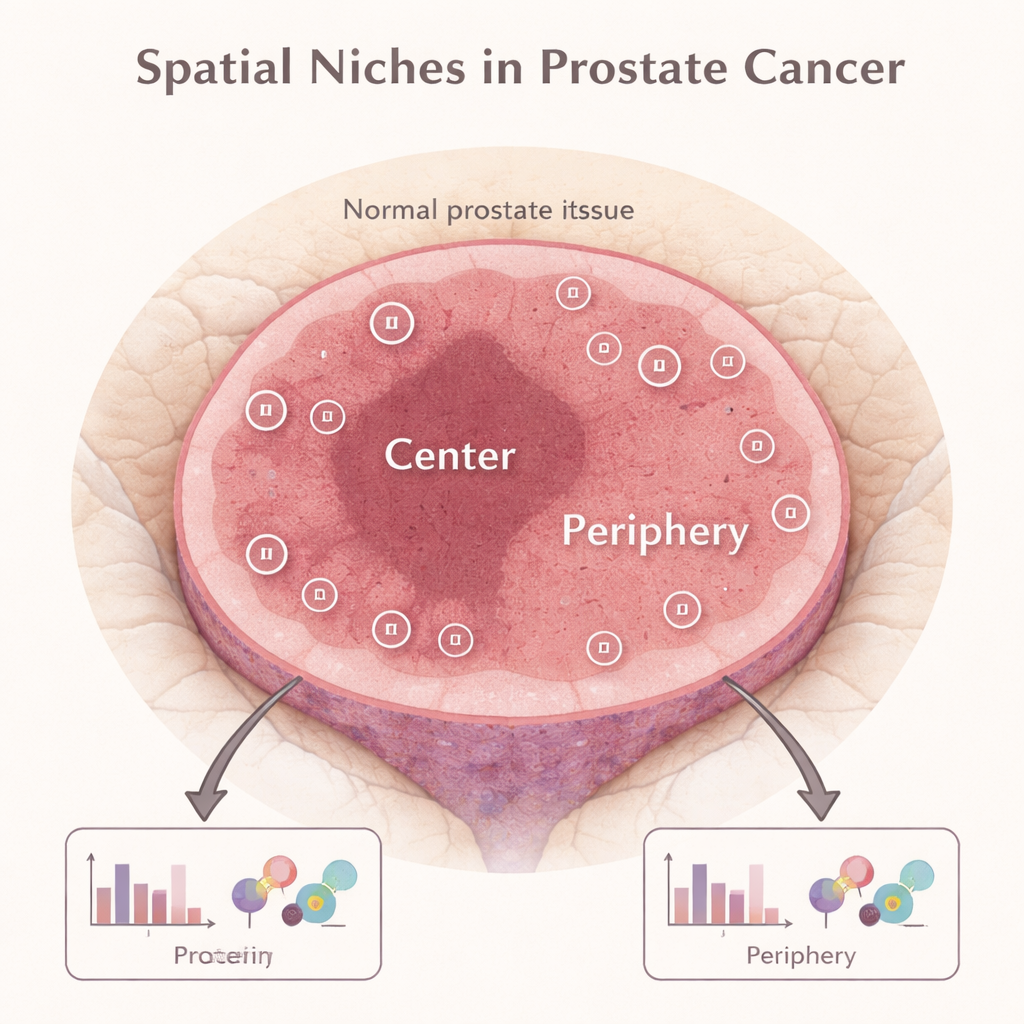
Den Tumor als kleines Ökosystem sehen
Moderne Forschung zeigt, dass ein Tumor keine einheitliche Kugel aus identischen Zellen ist. Vielmehr ähnelt er einem kleinen Ökosystem mit unterschiedlichen „Nachbarschaften“ oder räumlichen Nischen. Beim Prostatakrebs können der innere Tumorkern und die äußere Grenze, wo Krebs auf gesundes Gewebe trifft, unterschiedliche Mischungen aus Krebszellen, Immunzellen und stützenden Strukturen beherbergen. Die Autoren verwendeten eine Technik namens digitale räumliche Profilierung, mit der sie Dutzende von Proteinen direkt in dünnen Schnittpräparaten aus aufgefangenem Tumorgewebe messen können, wobei sie genau festhalten, aus welchem Bereich des Tumors jede Messung stammt.
Proteine im Tumormittelpunkt und -rand messen
Das Team analysierte Tumorproben von 49 Männern mit Hochrisiko‑Prostatakrebs, die operiert worden waren. Für jeden Tumor wählten sie Regionen im Zentrum und am Peripherie‑Rand aus und bestimmten die Spiegel von 46 verschiedenen Proteinen, die mit Immunzellen, Zelltod und Wachstumssignalen zusammenhängen. Daraus entstanden Zehntausende von Datenpunkten. Betrachteten sie Zentrum und Peripherie getrennt, bestätigte sich, dass diese Bereiche unterschiedlich sind: Viele Proteine, insbesondere solche, die mit Immunaktivität verknüpft sind, waren am Tumorrand häufiger, während bestimmte Regulatoren des Zelltods im Zentrum höher exprimiert waren.
Wenn getrennte Betrachtungen nicht ausreichen
Die Forschenden fragten dann, ob Proteinmuster nur im Zentrum oder nur an der Peripherie vorhersagen könnten, wie lange Patienten nach der Operation ohne Krankheitsprogression bleiben. Mithilfe statistischer Methoden zur Gruppierung von Patienten anhand der Proteinmuster in jedem Kompartiment fanden sie für Zentrum und Peripherie jeweils zwei Hauptcluster. Keines dieser Cluster stellte sich jedoch als mit dem klinischen Verlauf über die Zeit übereinstimmend heraus, noch korrelierte es klar mit klassischen Risikofaktoren wie dem Gleason‑Score oder bekannten Genmutationen wie BRCA1/2 und TP53. Anders gesagt: Die isolierte Betrachtung einer einzelnen „Nachbarschaft“ ergab keinen nützlichen neuen prognostischen Marker.
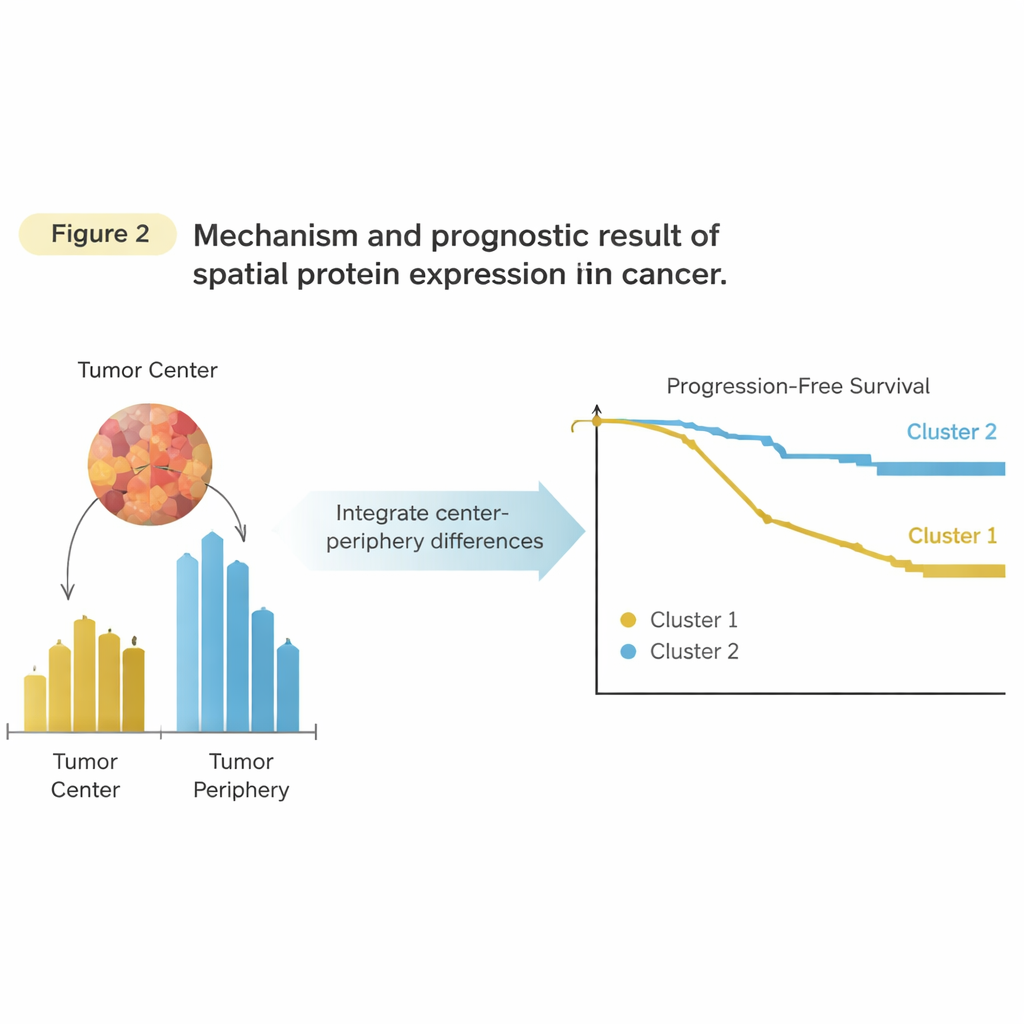
Die Kombination beider Nachbarschaften zeigt ein Signal
Der entscheidende Schritt war, Informationen aus Zentrum und Peripherie zu kombinieren, statt sie getrennt zu betrachten. Für jedes Protein und jeden Patienten berechneten die Forschenden, um wie viel dieses Protein in der Peripherie gegenüber dem Zentrum stärker (oder schwächer) exprimiert war. Das ergab einen einzelnen „Balancewert“ pro Protein, der weiterhin erfasste, wo im Tumor das Protein höher war. Gruppierten sie Patienten anhand dieser räumlichen Balancen, bildeten sich zwei neue Cluster. Dieses Mal hatten die Cluster Bedeutung: Eine Gruppe hatte eine deutlich kürzere Zeit bis zur Krankheitsprogression als die andere. Wichtig war, dass die Aussagekraft dieses Ansatzes nicht von einem einzelnen dominanten Protein stammte, sondern vom gesamten räumlichen Muster über viele Proteine hinweg, insbesondere solche, die mit Immunzellen und Gewebsumbau am Tumorrand verknüpft sind.
Was das für Patienten bedeuten könnte
Für Menschen mit Prostatakrebs deuten diese Befunde darauf hin, dass nicht nur die Gesamtmenge eines Proteins, sondern auch dessen räumliche Verteilung innerhalb des Tumors wertvolle Hinweise zum künftigen Krankheitsverlauf liefern kann. Die Studie ist zwar klein und verwendet eine spezialisierte, kostspielige Technologie, sie liefert jedoch einen Proof‑of‑Concept dafür, dass räumlich informierte Proteinmessungen prognostische Informationen zutage fördern können, die Standardtests nicht erfassen. Mit weiterer Validierung und vereinfachten Laborverfahren könnte ein solcher räumlicher Biomarker eines Tages Ärzten helfen, besser zu unterscheiden, welche Hochrisiko‑Prostatakarzinome wahrscheinlich schnell fortschreiten und welche einen moderateren Verlauf nehmen – und damit individuellere Therapieentscheidungen zu ermöglichen.
Zitation: Schneider, F., Böning, S.H., Antunes, B.C. et al. Prognostic impact of spatial niches in prostate cancer. Sci Rep 16, 2598 (2026). https://doi.org/10.1038/s41598-026-35720-1
Schlüsselwörter: Prostatakrebs, räumliche Profilierung, tumormikroumgebung, prognostischer Biomarker, intratumorale Heterogenität