Clear Sky Science · de
Korrelationen zwischen m6A-Methylierungs-assoziierten mRNAs und Schilddrüsenkrebs
Warum winzige Veränderungen in RNA für Schilddrüsenkrebs wichtig sind
Schilddrüsenkrebs ist oft heilbar, doch einige Patienten erleben weiterhin Rückfälle oder Metastasen. Diese Studie untersucht eine aufkommende biologische Ebene, die man als RNA‑„Markierung“ bezeichnet: kleine chemische Anhängsel, die an RNA‑Moleküfte innerhalb unserer Zellen angefügt werden. Die Forscher stellten eine gezielte Frage: Ändern sich diese RNA‑Marken bei Menschen mit papillärem Schilddrüsenkarzinom ohne Autoimmunerkrankung der Schilddrüse so, dass sie das Krebswachstum fördern könnten, und könnten diese Änderungen auf neue Diagnose‑ oder Behandlungsansätze hinweisen?
Fokus auf Schilddrüsentumoren ohne Immunerkrankung
Viele Menschen mit Schilddrüsenkrebs haben zugleich eine autoimmune Schilddrüsenerkrankung, bei der das Immunsystem die Schilddrüse angreift und dadurch das biologische Bild verkomplizieren kann. Um das zu vermeiden, untersuchte das Team 26 Patienten, deren papilläres Schilddrüsenkarzinom ohne Hinweise auf Autoimmunität auftrat. Von jedem Patienten entnahmen sie ein Stück des Tumors und ein benachbartes, nicht‑tumoröses Schilddrüsengewebe. Bei einer Untergruppe von drei Patienten führten sie umfassende Analysen durch, welche Gene ein- oder ausgeschaltet sind und wie stark die entsprechenden RNAs mit einem spezifischen chemischen Anhängsel namens m6A versehen sind, der häufigsten inneren Modifikation auf RNA in menschlichen Zellen.
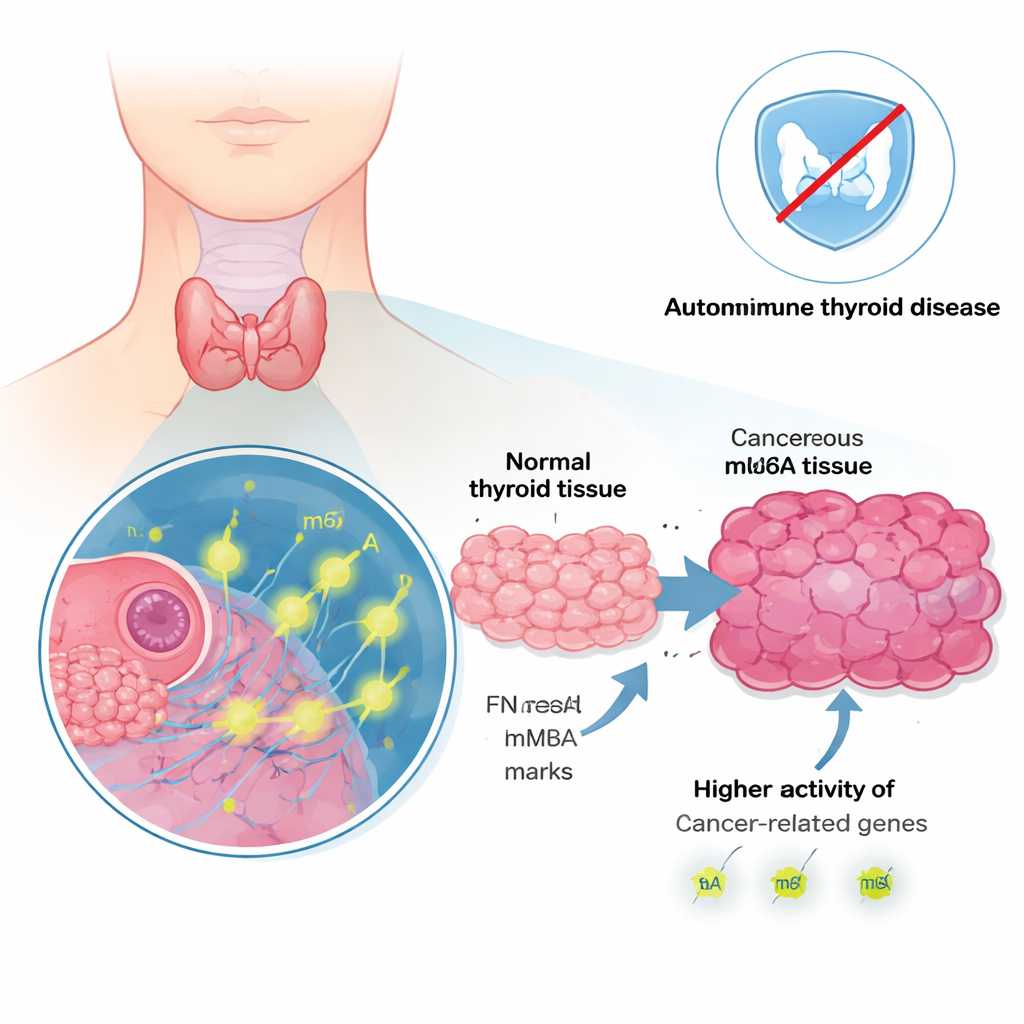
Ein Anstieg krebsassoziierter Gene und Signalwege
Beim Vergleich von Tumorgewebe mit dem benachbarten gesunden Gewebe fanden die Forscher 486 Gene, die im Tumor stärker aktiv waren, und 39, die weniger aktiv waren. Viele der am stärksten erhöhten Gene sind bereits mit Tumorwachstum, Metastasierung oder Therapieresistenz in Verbindung gebracht worden. Dazu gehören Gene wie LAMB3, FN1 und NMU, die Zellen helfen, mit ihrer Umgebung und benachbarten Zellen zu interagieren. Computergestützte Analysen zeigten, dass die verstärkten Gene sich in Signalwegen bündelten, die bereits als treibende Kräfte von Krebs bekannt sind, darunter Netzwerke im Zusammenhang mit Zellteilung, Stressreaktionen und Kommunikation zwischen Zellen und dem Immunsystem. Mit anderen Worten: Die Tumoren hatten ihre Genaktivität eindeutig in Richtung Wachstum und Invasion umprogrammiert.
RNA‑Marken und ein wichtiger „Reader“ sind erhöht
Die nächste Frage war, ob das m6A‑Anhänge auf RNA in diesen Tumoren verändert ist. Mit einem biochemischen Test stellte das Team fest, dass die Gesamtm6A‑Level im Tumorgewebe höher waren als im passenden Normalgewebe. Anschließend untersuchten sie die Gene, die dieses Markierungssystem steuern: die „Writer“, die m6A hinzufügen, die „Eraser“, die es entfernen, und die „Reader“, die an markierte RNA binden und deren Schicksal beeinflussen. Nur ein Faktor hob sich in den Tumoren deutlich hervor: das Reader‑Protein IGF2BP2 wurde in deutlich höheren Mengen produziert. Frühere Arbeiten haben gezeigt, dass IGF2BP2 an m6A‑markierte RNAs binden kann und diese stabiler macht sowie ihre Übersetzung in Protein fördert. Beim papillären Schilddrüsenkarzinom wurde IGF2BP2 bereits mit aggressiverem Verhalten, schlechteren Ergebnissen und erhöhter Lymphknotenmetastasierung in Verbindung gebracht.
Welche RNAs zusätzliche Marken tragen — und warum das zählt
Indem sie m6A‑Kartierung mit Messungen der Genaktivität in denselben Proben kombinierten, identifizierten die Forscher 367 RNAs, die in Tumoren stärker markiert waren, und 12, die weniger markiert waren. Auffällig war, dass die meisten der am stärksten hyper‑markierten RNAs zu derselben Gruppe krebsfördernder Gene gehörten, die insgesamt stärker exprimiert waren. Bei 147 Genen zeigten Tumoren sowohl erhöhte m6A‑Level als auch erhöhte Expression, darunter FN1, LAMB3, NMU und CDKN2B. Netzwerk‑Analysen deuteten darauf hin, dass diese Gene im Zentrum von Systemen stehen, die steuern, wie Tumorzellen an ihrem Umfeld haften, auf entzündliche Signale reagieren und das umgebende Gewebe umgestalten — Schlüsselprozesse für Invasion und Metastasierung. Das Team fand außerdem Dutzende markierter langer nichtkodierender RNAs, darunter solche, die mit bekannten Krebswegen verknüpft sind, was nahelegt, dass RNA‑Markierung nicht nur proteinkodierende Botschaften, sondern auch regulatorische RNAs beeinflussen kann, die die Genaktivität feinjustieren.
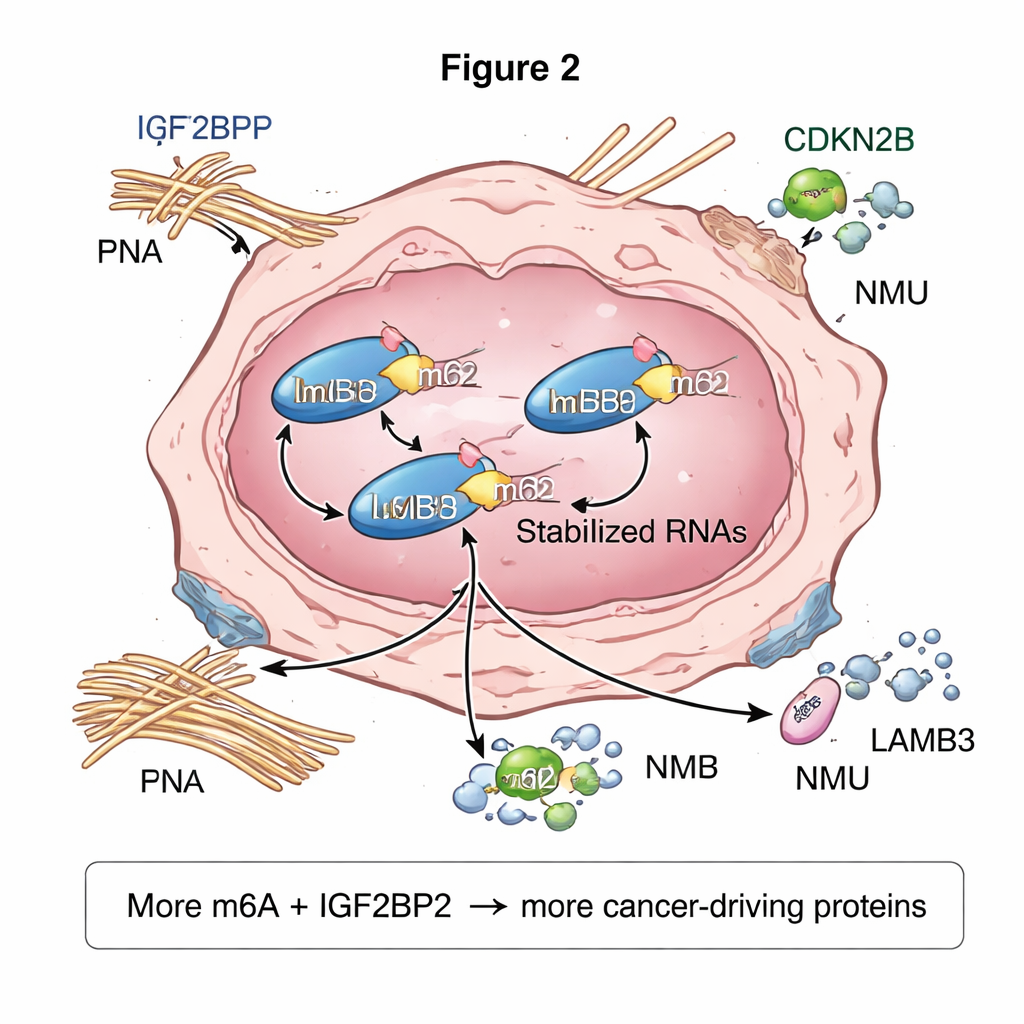
Was das für Patientinnen und Patienten bedeuten könnte
Für Nicht‑Spezialisten ist die Kernbotschaft: Papilläre Schilddrüsenkarzinome — selbst bei Patienten ohne autoimmune Schilddrüsenerkrankung — scheinen ein chemisches Markierungssystem auf RNA zu nutzen, um krebsfördernde Netzwerke zu verstärken. Tumorzellen zeigen höhere globale m6A‑Werte und vermehrte Mengen des Reader‑Proteins IGF2BP2, die zusammen Schlüsselgene stabilisieren und deren Produktion steigern, was Wachstum und Ausbreitung fördert. Obwohl diese Arbeit hauptsächlich auf fortgeschrittenen rechnerischen und laborbasierten Analysen einer kleinen Patientengruppe beruht, hebt sie konkrete Akteure — wie IGF2BP2 und die m6A‑markierten Gene FN1, LAMB3 und NMU — als vielversprechende Kandidaten für neue Tests oder gezielte Therapien hervor. Zukünftige Studien müssen diese Ergebnisse in größeren Kohorten und experimentellen Modellen bestätigen, doch die Resultate deuten darauf hin, dass „epigenetische“ Markierungen auf RNA eine wichtige und potenziell medikamentös angreifbare Ebene der Schilddrüsenkrebsbiologie darstellen.
Zitation: Jiang, Z., Luo, S., Lin, Y. et al. Correlations of m6A methylation-related mRNAs with thyroid cancer. Sci Rep 16, 5688 (2026). https://doi.org/10.1038/s41598-026-35712-1
Schlüsselwörter: papilläres Schilddrüsenkarzinom, RNA-Methylierung, m6A-Modifikation, IGF2BP2, Krebs-Biomarker