Clear Sky Science · de
HIV‑Protein Vpr induziert Demethylierung des SNCA‑Antisense‑Promotors und führt zu neurokognitiven Beeinträchtigungen
Warum HIV das Gehirn weiterhin beeinträchtigen kann
Menschen mit HIV leben dank moderner antiretroviraler Medikamente länger und gesünder. Dennoch leiden viele weiterhin unter Gedächtnis‑, Konzentrations‑ und Bewegungsproblemen, selbst wenn das Virus im Blut gut kontrolliert ist. Diese Studie untersucht, warum das so ist, indem sie sich auf ein kleines virales Protein namens Vpr und ein Gehirnprotein, Alpha‑Synuklein, konzentriert, das auch bei der Parkinson‑Krankheit zentral ist. Zu verstehen, wie diese beiden Moleküle miteinander interagieren, kann erklären, warum HIV das Gehirn altern lassen kann, und neue Ansätze zum Schutz des Gehirns aufzeigen.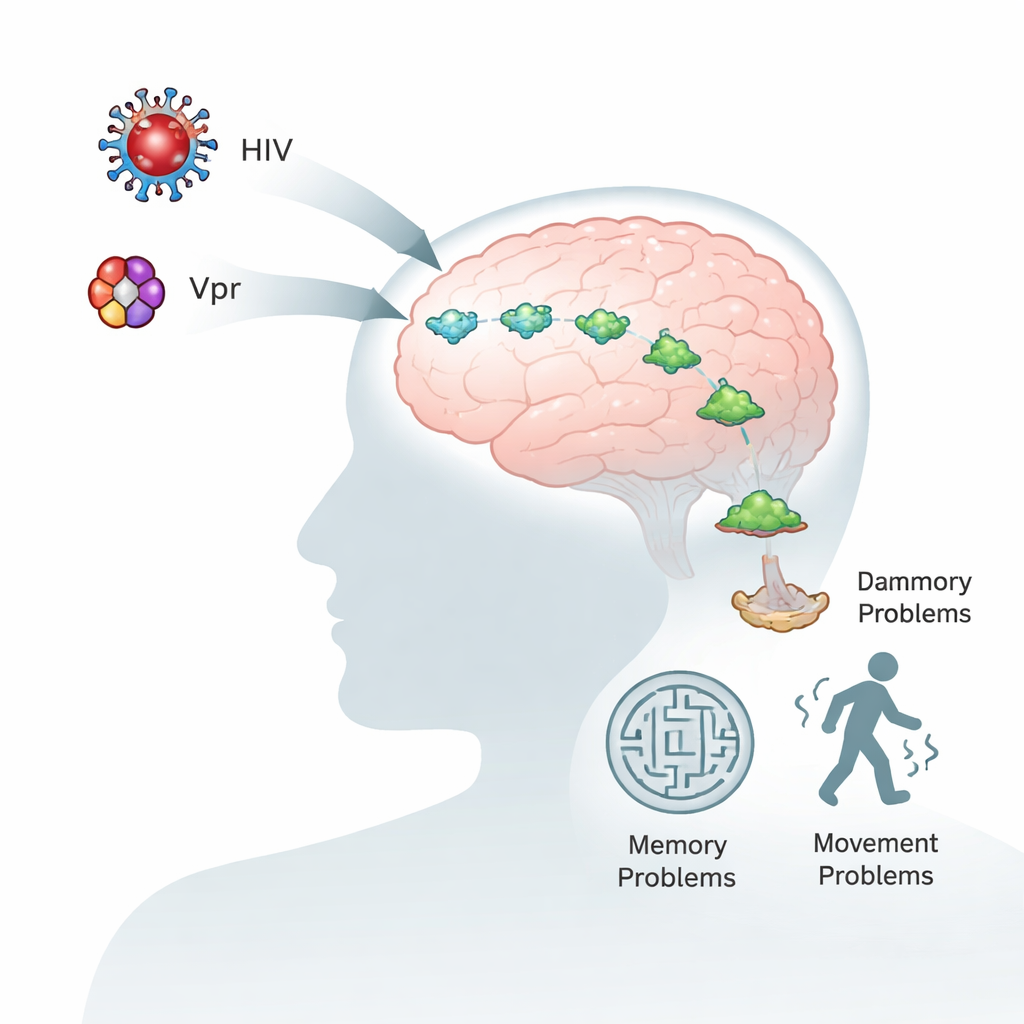
Ein Gehirnprotein an der Schnittstelle von HIV und Parkinson
Alpha‑Synuklein ist ein Protein, das Nervenzellen hilft, zu kommunizieren, insbesondere in Hirnregionen, die Bewegung und Gedächtnis steuern. Wenn sich zu viel Alpha‑Synuklein anreichert, bildet es Aggregate, die Synapsen schädigen, die Energie produzierenden Mitochondrien belasten und Entzündungen fördern. Solche Aggregate sind ein Kennzeichen der Parkinson‑Krankheit. Die Autoren zeigen, dass Alpha‑Synuklein auch beim normalen Altern von Mäusen zunimmt und dass das HIV‑Protein Vpr seine Menge in nervenähnlichen Zellen noch weiter erhöht. Damit steht Alpha‑Synuklein an der Schnittstelle zwischen HIV‑bedingten Denkstörungen und klassischen Bewegungsstörungen.
Wie ein virales Protein die zelluläre „Interpunktion“ umschreibt
Jede Zelle verwendet chemische Markierungen auf der DNA — oft als molekulare Interpunktionszeichen beschrieben — um Gene ein‑ oder auszuschalten. In dieser Arbeit konzentrierte sich das Team auf einen wenig bekannten Kontrollschalter innerhalb des Alpha‑Synuklein‑Gens, den sogenannten Antisense‑Promotor. In gesunden Zellen ist dieser Schalter stark mit Methylgruppen markiert und bleibt dadurch relativ inaktiv. Die Forschenden fanden heraus, dass Vpr diese Markierungen an bestimmten Stellen in diesem Bereich entfernt, ein Prozess, der als Demethylierung bekannt ist. Sobald diese Markierungen entfernt sind, wird der Antisense‑Promotor aktiver und treibt die vermehrte Produktion von Alpha‑Synuklein an, was die Grundlage für schädliche Aggregationen legt.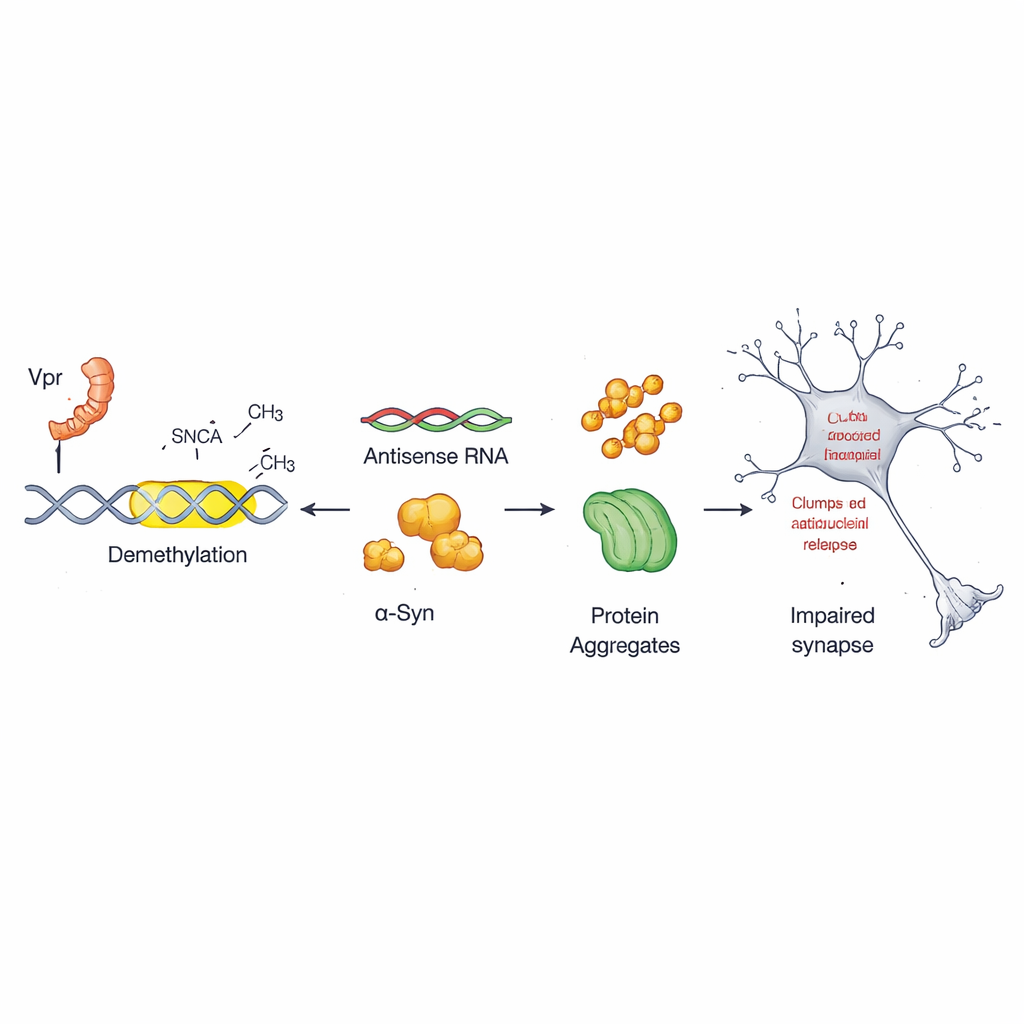
Belege aus Zellen, Mäusen und menschlichen Gehirnen
Mithilfe kultivierter humaner nervenähnlicher Zellen und primärer Mausneurone zeigten die Autorinnen und Autoren, dass die Zugabe von Vpr die Alpha‑Synuklein‑mRNA‑ und Proteinspiegel im Verlauf erhöht. Ein Wirkstoff, der allgemein die DNA‑Demethylierung fördert, ahmte einige dieser Effekte nach und unterstreicht damit die Rolle der epigenetischen Kontrolle. Im Gegensatz dazu verhinderte eine Verbindung namens DMOG, die demethylisierende Enzyme blockiert, dass Vpr den Antisense‑Promotor vollständig aktiviert. Das Team untersuchte anschließend menschliche Gehirnproben von Personen mit und ohne HIV. Gehirne von HIV‑positiven Spendern — sowohl vor als auch nach antiretroviraler Behandlung — wiesen weniger Methylmarkierungen in derselben DNA‑Region sowie höhere Werte von Alpha‑Synuklein und dessen Antisense‑Transkript auf, insbesondere bei Spendern mit HIV‑bedingter Demenz. Das deutet darauf hin, dass das Virus eine dauerhafte epigenetische Narbe im Gehirn hinterlässt.
Von molekularen Veränderungen zu Gedächtnisproblemen
Um diese molekularen Veränderungen mit Verhalten zu verknüpfen, untersuchten die Forschenden, wie Vpr Gehirnschaltkreise bei Mäusen beeinflusst. Als sie Vpr auf Schnitte des Maus‑Hippocampus aufbrachten — einer Region, die für Gedächtnis wichtig ist — blieb die grundlegende Signalstärke zwischen Neuronen unverändert, doch die Fähigkeit, Verbindungen zu verstärken — ein Prozess, der als Langzeitpotenzierung bezeichnet wird — war reduziert. In lebenden Mäusen führten gezielte Injektionen von Vpr in den Hippocampus zu schlechteren Leistungen bei einer räumlichen Gedächtnisaufgabe, bei der die Tiere sich die Lage von Objekten merken müssen. Zusammen legen diese Experimente nahe, dass durch Vpr bedingte Alpha‑Synuklein‑Veränderungen keine bloßen biochemischen Kleinigkeiten sind, sondern in geschwächte Synapsen und messbare Gedächtnisdefizite münden.
Was das für Menschen mit HIV bedeutet
Die Studie schlägt eine klare Ereigniskette vor: HIV setzt Vpr frei, Vpr reprogrammiert einen wichtigen DNA‑Schalter, der Alpha‑Synuklein kontrolliert, das Protein sammelt sich an und verklumpt, und Neurone verlieren nach und nach ihre Fähigkeit zur Kommunikation und zur Unterstützung des Gedächtnisses. Da ähnliche Alpha‑Synuklein‑Probleme die Parkinson‑Krankheit zugrunde liegen, deutet die Arbeit darauf hin, dass HIV und klassische neurodegenerative Erkrankungen überlappende Mechanismen teilen. Wichtig ist, dass die Ergebnisse mögliche neue Strategien hervorheben — etwa Medikamente, die die DNA‑Methylierung am Antisense‑Promotor stabilisieren oder die Ansammlung von Alpha‑Synuklein begrenzen — um den kognitiven Abbau und Bewegungsprobleme im Zusammenhang mit HIV zu verlangsamen oder zu verhindern.
Zitation: Santerre, M., Wang, Y., Kalamarides, D. et al. HIV Vpr induces demethylation of the SNCA antisense promoter, leading to neurocognitive impairment. Sci Rep 16, 6078 (2026). https://doi.org/10.1038/s41598-026-35691-3
Schlüsselwörter: HIV‑assoziierte neurokognitive Störungen, Alpha‑Synuklein, Epigenetik, DNA‑Methylierung, Parkinson‑ähnliche Symptome