Clear Sky Science · de
Rationales Redesign eines hochaktiven G‑Quadruplex‑DNAzymes durch Umgebungs‑ und Schleifenbasen
Kleine DNA‑Maschinen mit großem Potenzial
Stellen Sie sich vor, fragile Protein‑Enzyme durch winzige DNA‑Stränge zu ersetzen, die Hitze, Chemikalien und rauer Behandlung trotzen und dennoch nützliche chemische Reaktionen ausführen können. Diese Studie untersucht genau diese Idee. Die Forscher verändern spezielle DNA‑Strukturen so, dass sie wie miniaturisierte Reinigungsenzyme funktionieren und Wasserstoffperoxid nutzen können, um ein starkes Signal zu erzeugen. Diese robusteren, schnelleren DNA‑„Maschinen“ könnten künftige medizinische Tests, Umweltsensoren und tragbare Diagnostika günstiger, zuverlässiger und einfacher im Einsatz außerhalb des Labors machen.
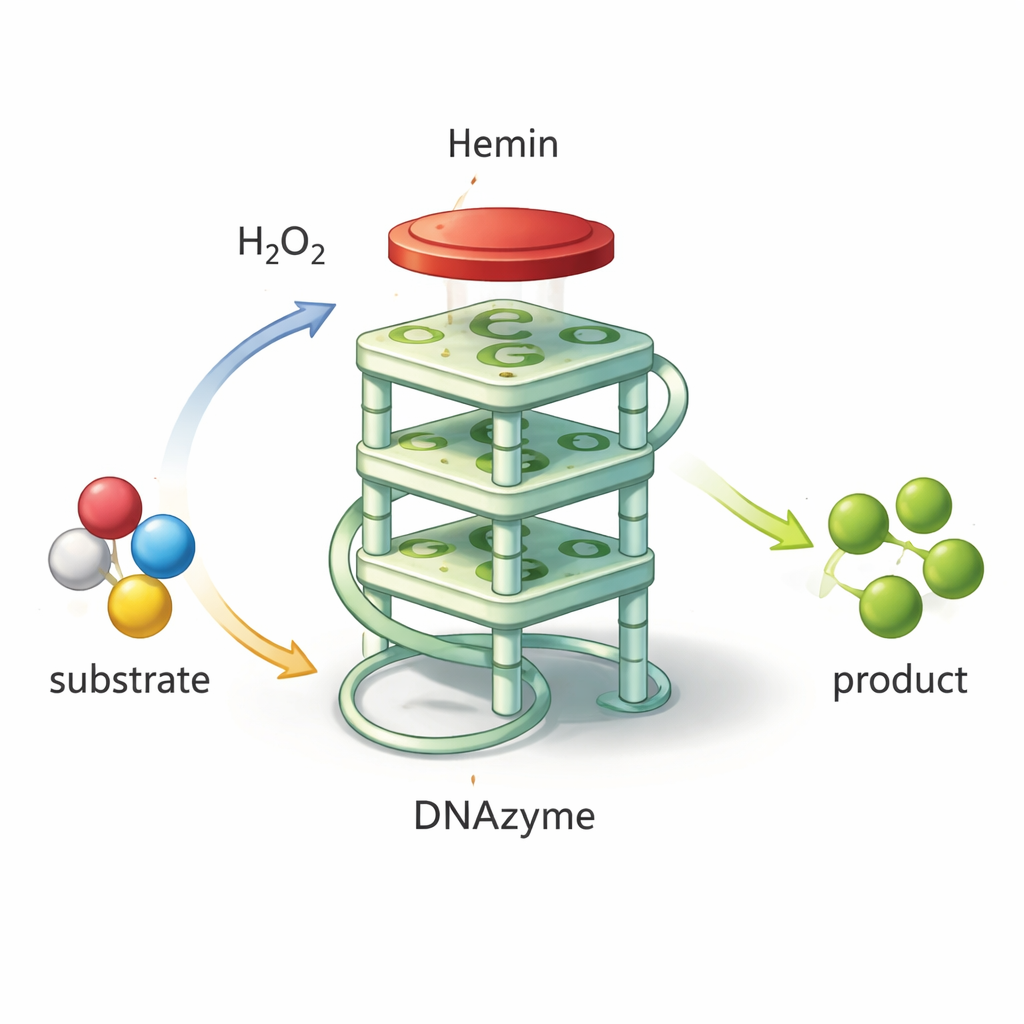
DNA als winziges chemisches Werkzeug
Nicht alle DNA dient nur als passiver Träger genetischer Information. Bestimmte kurze Sequenzen können sich zu ungewöhnlichen Formen falten, die bestimmte Moleküle binden oder sogar chemische Reaktionen beschleunigen. Eine solche Struktur ist das G‑Quadruplex, bei dem guaninreiche DNA zu einem kompakten, vierlagigen Stapel zusammenfaltet. Wenn ein kleines eisenhaltiges Molekül namens Häm auf diesem Stapel sitzt, wirkt das Paar wie ein „DNAzym“: ein DNA‑basiertes Katalysator, das natürliche Peroxidasen nachahmt. Es kann Wasserstoffperoxid nutzen, um eine farbbildende Verbindung zu oxidieren und ein kräftiges grünes Signal zu erzeugen, das sich leicht messen lässt. Da diese DNAzyme kostengünstig herstellbar, sehr stabil und einfach umgestaltbar sind, stellen sie vielversprechende Bausteine für Biosensoren dar, die Krankheitserreger, Toxine oder Krankheitsmarker nachweisen.
Warum aktuelle DNA‑Enzyme ein Upgrade brauchen
Trotz ihres Potenzials sind die meisten DNAzyme weiterhin langsamer und weniger effizient als natürliche Proteinenzyme. Bestehende Biosensoren müssen oft das Zielmolekül mit Techniken wie PCR amplifizieren oder zusätzliche Hilfsstoffe zugeben, was Kosten und Komplexität erhöht. Frühere Versuche zur Verbesserung von DNAzymen umfassten das Verknüpfen zweier DNA‑Einheiten, das permanente Anbinden von Häm oder das Umgeben der reaktiven Stelle mit zusätzlichen chemischen Gruppen. Solche Tricks helfen manchmal, können aber auch Volumen einführen, das stört, oder aufwendige Chemie erfordern. Eine zentrale offene Frage war, wie einfache Änderungen an benachbarten DNA‑Basen — insbesondere solche, die die Kernform des G‑Quadruplexes nicht zerstören — die Aktivität in vorhersehbarer, „designbarer“ Weise feinabstimmen könnten.
Neugestaltung eines leistungsstarken DNA‑Enzyms
Das Team konzentrierte sich auf ein besonders aktives DNAzym namens B730, das bereits zu den besten unveränderten G‑Quadruplex‑Katalysatoren zählt. Sie veränderten systematisch die DNA unmittelbar außerhalb des Kerns, indem sie übliche Basen wie Adenin, Thymin und Cytosin in den Schleifen‑ und Endbereichen hinzufügten oder umpositionierten. Eine neu gestaltete Variante, B730‑1.2 genannt, kombinierte zusätzliche Adenine in den Schleifen mit einem kurzen Thymin‑Cytosin‑Paar an einem Ende des Strangs. Unter moderaten Wasserstoffperoxid‑Bedingungen verdreifachte diese Variante die Anfangsgeschwindigkeit der Reaktion und vervierfachte etwa die Gesamtausbeute des gefärbten Produkts verglichen mit dem ursprünglichen B730. Sie übertraf zudem deutlich zwei andere bekannte DNAzyme, AS1411 und CatG4, bei einem direkten Vergleich.
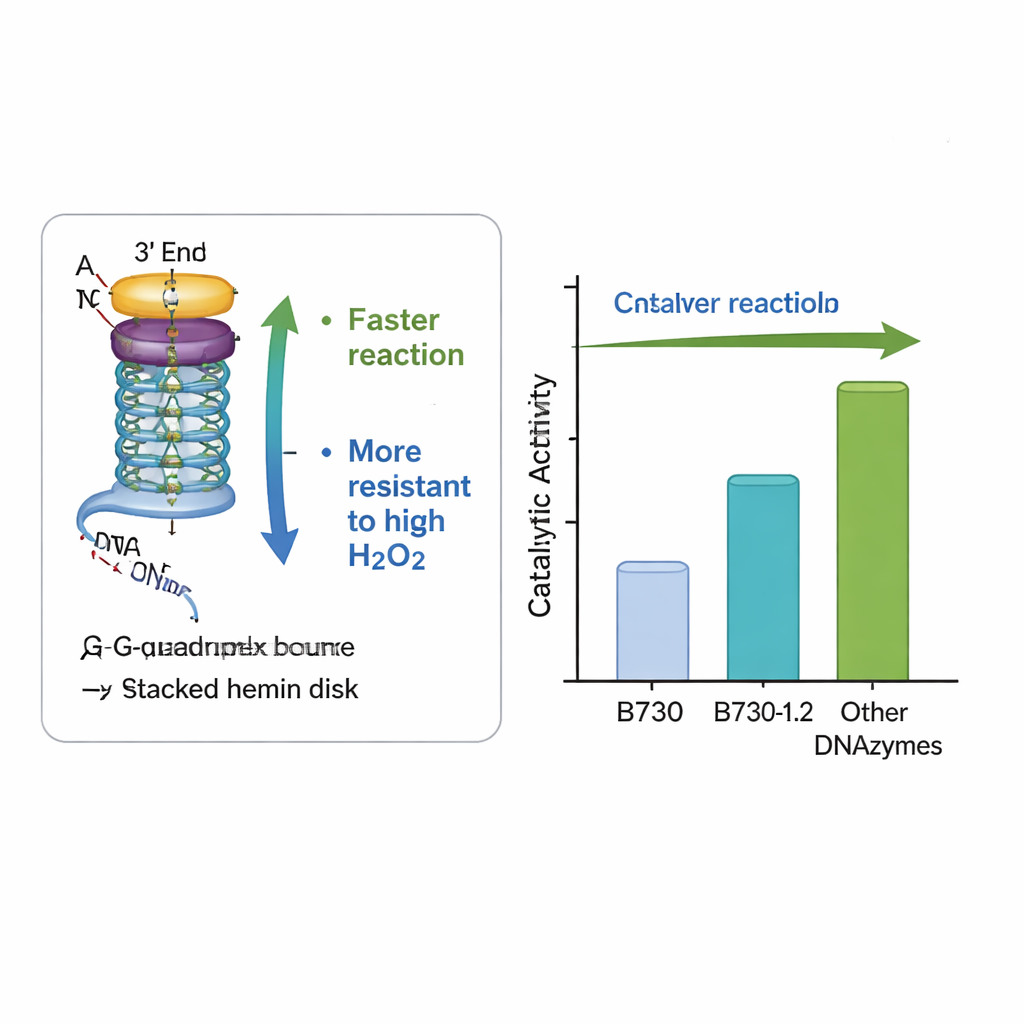
Ausgelegt für raue Bedingungen
Eine wichtige praktische Hürde sowohl für natürliche als auch künstliche Peroxidasen ist, dass hohe Wasserstoffperoxid‑Konzentrationen — der Stoff, der die Reaktion antreibt — das Enzym zerstören und den Prozess zum Erliegen bringen können. Das umgestaltete B730‑1.2‑DNAzym zeigte bemerkenswerte Widerstandsfähigkeit: Es behielt seine Aktivität bei und steigerte sie sogar bei Peroxid‑Werten, die ähnliche Systeme typischerweise inaktivieren. Messungen der Lichtabsorption bestätigten, dass die modifizierte DNA die Bildung des entscheidenden reaktiven Intermediats — des sogenannten Komplex I — schneller förderte, ohne die Gesamtstruktur des G‑Quadruplex zu stören. Anders ausgedrückt schufen subtile Änderungen der umliegenden Basen ein vorteilhafteres lokales Umfeld für die Chemie, beschleunigten die nützlichen Schritte und schützten zugleich das katalytische Zentrum besser vor Selbstzerstörung.
Was das für künftige Sensoren bedeutet
Für Nicht‑Spezialisten ist die Botschaft klar: Durch das gezielte Anpassen nur weniger „Buchstaben“ an beiden Seiten eines bereits guten DNA‑Enzyms erzeugten die Autoren eine Variante, die schneller arbeitet und unter härteren Bedingungen weiterfunktioniert. Ihre Strategie, flankierende und Schleifenbasen zu modifizieren, bietet ein einfaches, kostengünstiges Rezept, um leistungsfähigere DNA‑basierte Katalysatoren zu bauen, ohne auf komplexe chemische Modifikationen zurückzugreifen. Solche robusten, effizienten DNAzyme könnten das Herzstück nächster Teststreifen und tragbarer Geräte bilden, die unsichtbare biologische Signale — etwa Spuren von Viren oder Schadstoffen — schnell in leicht ablesbare Farbveränderungen umwandeln.
Zitation: Adeoye, R.I., Babbudas, N., Birchenough, M. et al. Rational redesign of high-activity G-quadruplex DNAzyme through flanking and looping of nucleobases. Sci Rep 16, 5060 (2026). https://doi.org/10.1038/s41598-026-35686-0
Schlüsselwörter: G‑Quadruplex‑DNAzym, Peroxidase‑Imitat, Biosensorik, Aptamer‑Engineering, Katalyse mit Wasserstoffperoxid