Clear Sky Science · de
Untersuchung von Acoramidis-basierten ionischen Flüssigkeiten als potenzielle Stabilisierungsmittel für Transthyretin mittels DFT-Berechnungen, molekularem Docking und ADMET-Studien
Warum eine Tablette gegen eine seltene Herzerkrankung so schwer herzustellen ist
Die Transthyretin-Amyloidose (ATTR) ist eine schwere Erkrankung, bei der sich ein Blutprotein im Herz und in den Nerven ablagert und diese langsam schädigt. Ein neues Medikament, Acoramidis, kann helfen, diese Ablagerungen zu verhindern, doch es gibt ein praktisches Problem: Das Medikament löst sich schlecht in Wasser, was seine Aufnahme als Tablette erschwert. Diese Studie untersucht einen raffinierten Ansatz, Acoramidis in neue salzähnliche Formen umzuwandeln — sogenannte ionische Flüssigkeiten — die das Arzneimittel leichter schluckbar und wirksamer machen könnten.
Ein vielversprechendes Medikament in trinkbare Form bringen
Damit eine Tablette wirkt, muss sie sich zunächst in den wässrigen Flüssigkeiten von Magen und Darm auflösen und dann die Darmwand in den Blutkreislauf passieren. Acoramidis stabilisiert das Transthyretin-(TTR-)Protein wirkungsvoll und hilft so, schädliche Proteinaggregate, die mit ATTR verbunden sind, zu verhindern. Allerdings ist es schlecht löslich und besitzt eine geringe orale Bioverfügbarkeit. Die Forschenden gingen das Problem an, indem sie Acoramidis chemisch mit verschiedenen geladenen Gegenmolekülen kombinierten und so drei neue ionische Flüssigkeiten (IL1, IL2 und IL3) erzeugten. Diese Formen sollen sich eher wie fließende Salze als wie starre Kristalle verhalten und so die Löslichkeit und Verteilung des Wirkstoffs im Körper verbessern. 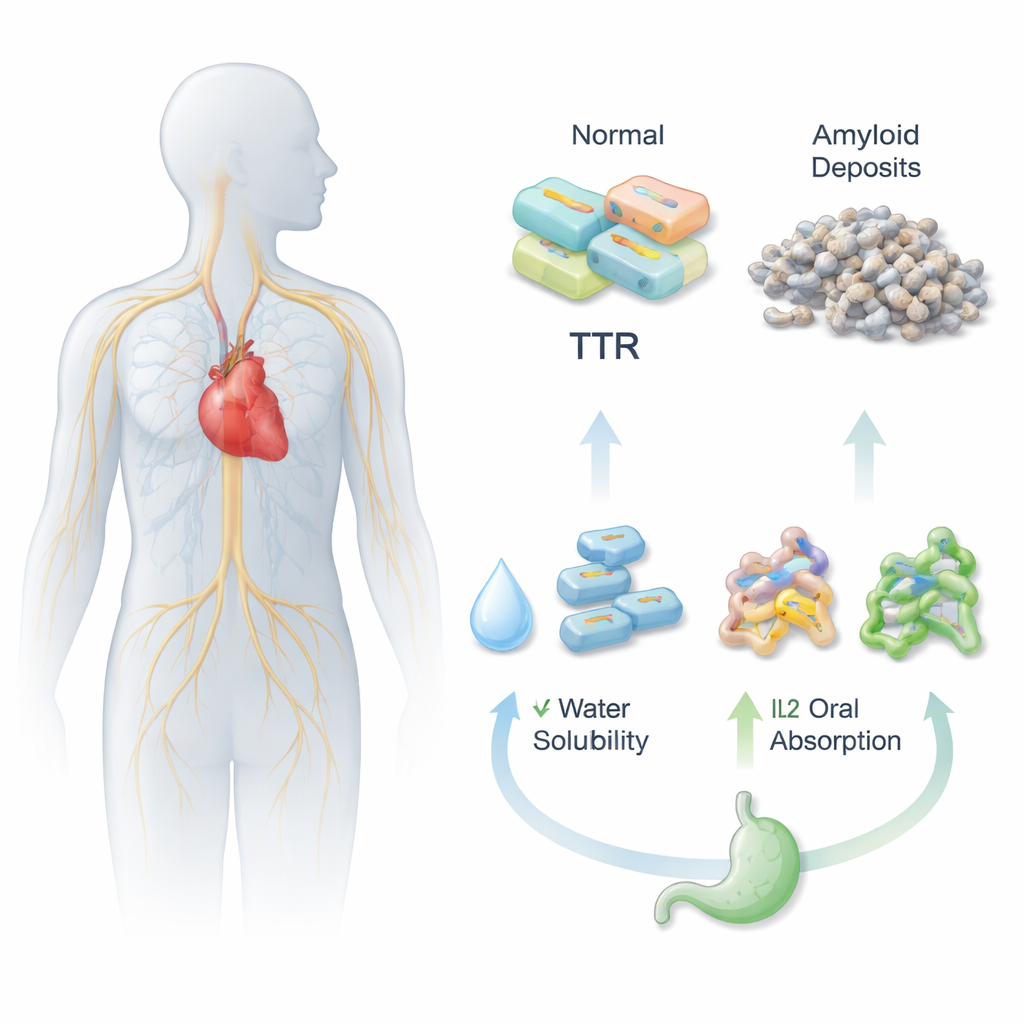
Die neuen Moleküle am Computer untersuchen
Statt direkt Tierversuche oder Studien am Menschen zu starten, nutzte das Team fortgeschrittene Computermethoden, um vorherzusagen, wie sich diese neuen Formen verhalten würden. Quantenchemische Berechnungen schätzten die Polarität jedes Moleküls — ein zentraler Prädiktor für Wasserlöslichkeit — und wie leicht sich seine Elektronen verschieben lassen, was Aufschluss darüber gibt, wie es mit Proteinen interagieren könnte. IL1 fiel durch das höchste Dipolmoment und die stärkste elektronische Reaktionsfähigkeit auf, was darauf hindeutet, dass es sich besser in Wasser löst und stärkere, flexiblere Wechselwirkungen mit Zielmolekülen eingehen kann. Die Energiebetrachtungen deuteten zudem darauf hin, dass IL1 thermisch stabiler ist als das Ausgangsmedikament und die beiden anderen ionischen Flüssigkeiten, also weniger dazu neigen sollte, sich vor Erreichen ihres Ziels zu zersetzen.
Wie fest das Medikament an sein Ziel binden kann
Als Nächstes verwendeten die Forschenden molekulares Docking, einen virtuellen „Schloss-und-Schlüssel“-Test, um zu prüfen, wie gut Acoramidis und seine drei ionischen Formen in den Bindungskanal des TTR-Proteins passen. Alle vier Verbindungen dockten in die korrekte Region von TTR ein, doch IL1 bildete den festesten Kontakt, mit der günstigsten Bindungsenergie und mehreren stabilisierenden Wechselwirkungen — insbesondere Wasserstoffbrücken — mit wichtigen Aminosäuren des Proteins. Diese stärkere Bindung legt nahe, dass IL1 möglicherweise sogar besser als das Ausgangsmedikament darin ist, TTR in seiner sicheren, vierteiligen Struktur zu halten und so den gefährlichen Zerfall und die Fehlfaltung zu verhindern, die zu Amyloidablagerungen führen.
Wird der Körper diese neuen Formen aufnehmen und ausscheiden?
Schließlich nutzte das Team Online-Pharmakologie-Tools, um zu untersuchen, wie der Körper mit diesen Verbindungen umgehen könnte — wie gut sie sich lösen, die Darmwand passieren, im Blut zirkulieren und schließlich eliminiert werden. Alle drei ionischen Flüssigkeiten wurden prognostisch als wasserlöslicher eingestuft als Acoramidis, wobei IL3 die höchste rohe Löslichkeit zeigte. Messgrößen zur intestinalen Permeabilität und zur Gesamtaufnahme nach oraler Gabe verbesserten sich bei allen drei ionischen Flüssigkeiten; IL1 und IL2 zeigten dabei das beste Gleichgewicht aus Darmdurchlässigkeit und vorhergesagter Bioverfügbarkeit. Plasmaeiweißbindung, Eliminationsraten und Halbwertszeiten verschoben sich ebenfalls in einer Weise, die darauf hindeutet, dass die ionischen Flüssigkeiten nach oraler Gabe eine zuverlässigere Exposition bieten könnten — wobei IL1 erneut ein besonders günstiges Profil zeigte. 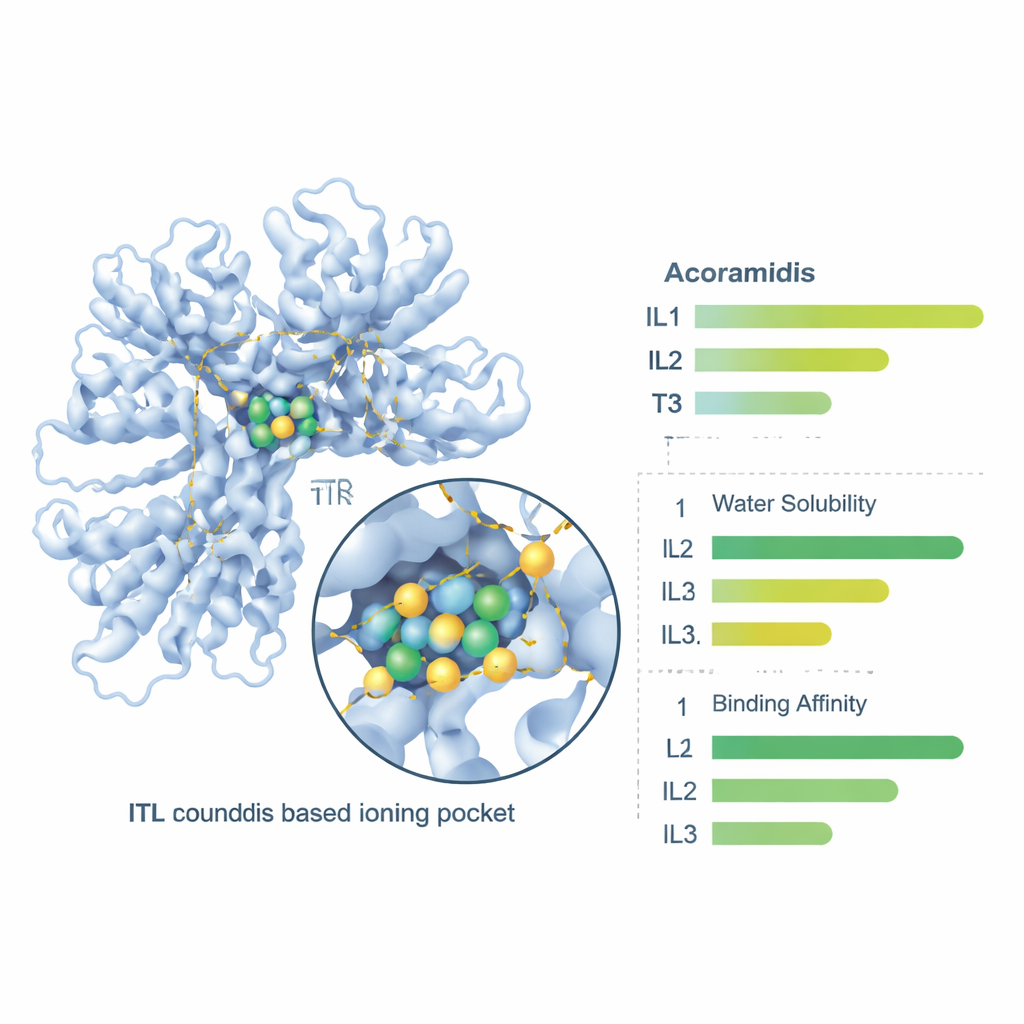
Was das für künftige ATTR-Therapien bedeuten könnte
Für Nicht-Spezialisten lautet die Kernbotschaft: Das Medikament Acoramidis erscheint bereits vielversprechend gegen eine seltene, aber schwere Herz- und Nervenerkrankung, doch seine schlechte Löslichkeit beschränkt die Wirksamkeit bei oraler Gabe. Durch die Umwandlung von Acoramidis in speziell gestaltete ionische Flüssigkeiten zeigt diese Studie — vollständig auf Computertests basierend — dass es möglich sein könnte, Varianten zu entwickeln, die besser löslich sind, stärker an ihr Protein-Ziel binden und effizienter aufgenommen werden. Unter den drei Kandidaten scheint IL1 die beste Balance aus Stabilität, Bindungsstärke, Löslichkeit und vorhergesagter oraler Aufnahme zu bieten und ist somit ein starker Kandidat für weitere Labor- und klinische Entwicklungen mit dem Ziel, wirksamere und leichter einzunehmende Therapien für ATTR bereitzustellen.
Zitation: Mostaghni, F., Mahani, N.M. Investigation of Acoramidis-based ionic liquids as potential stabilizers of transthyretin using DFT calculations, molecular docking, and ADMET studies. Sci Rep 16, 6540 (2026). https://doi.org/10.1038/s41598-026-35684-2
Schlüsselwörter: Transthyretin-Amyloidose, Acoramidis, ionische Flüssigkeiten, Proteinfehlfaltung, orale Arzneimittelverabreichung