Clear Sky Science · de
In silico-Design eines Multi‑Epitop-Impfstoffs, der auf DENV‑1 und DENV‑3 abzielt
Warum Dengue-Impfstoffe weiterhin wichtig sind
Denguefieber ist längst keine seltene tropische Erkrankung mehr; es bedroht heute Milliarden Menschen in mehr als 100 Ländern und überlastet in Teilen Asiens, Lateinamerikas und darüber hinaus regelmäßig Krankenhäuser. Selbst mit zwei zugelassenen Impfstoffen auf dem Markt ist der Schutz jedoch uneinheitlich, insbesondere bei Menschen, die noch nie Dengue hatten, und in Regionen, in denen mehrere Virustypen gleichzeitig zirkulieren. Diese Studie stellt eine aktuelle Frage: Kann computergestütztes Design uns helfen, einen sichereren, präziseren Impfstoff zu entwickeln, der speziell auf gefährliche Koinfektionen mit zwei Dengue-Serotypen abzielt, die häufig gemeinsam auftreten?
Zwei heimtückische Virustypen und warum sie ein Problem sind
Das Denguevirus tritt in vier Varianten auf, den Serotypen DENV‑1 bis DENV‑4. Eine Infektion mit einem dieser Typen kann hohes Fieber, starke Schmerzen und in einigen Fällen lebensbedrohliche Blutungen oder Schock verursachen. Besorgniserregend ist, dass eine zweite Erkrankung mit einem anderen Serotyp die Krankheit manchmal verschlimmern kann statt zu schützen, weil vorhandene Antikörper dem neuen Virus das Eindringen in Zellen erleichtern können – ein Prozess, der als Antikörper‑vermittelte Verstärkung (antibody‑dependent enhancement) bezeichnet wird. In jüngsten Ausbrüchen berichteten Ärztinnen und Ärzte von gleichzeitig mit DENV‑1 und DENV‑3 infizierten Patienten, eine Kombination, die mit schwererem Krankheitsverlauf und verwirrenden Testergebnissen in Verbindung gebracht wird. Aktuelle Impfstoffe schützen nicht zuverlässig alle Altersgruppen und Serotypen, insbesondere Menschen ohne vorherige Exposition, wodurch eine gefährliche Lücke in der Abwehr besteht.
Design eines Impfstoffs vom Molekül aus
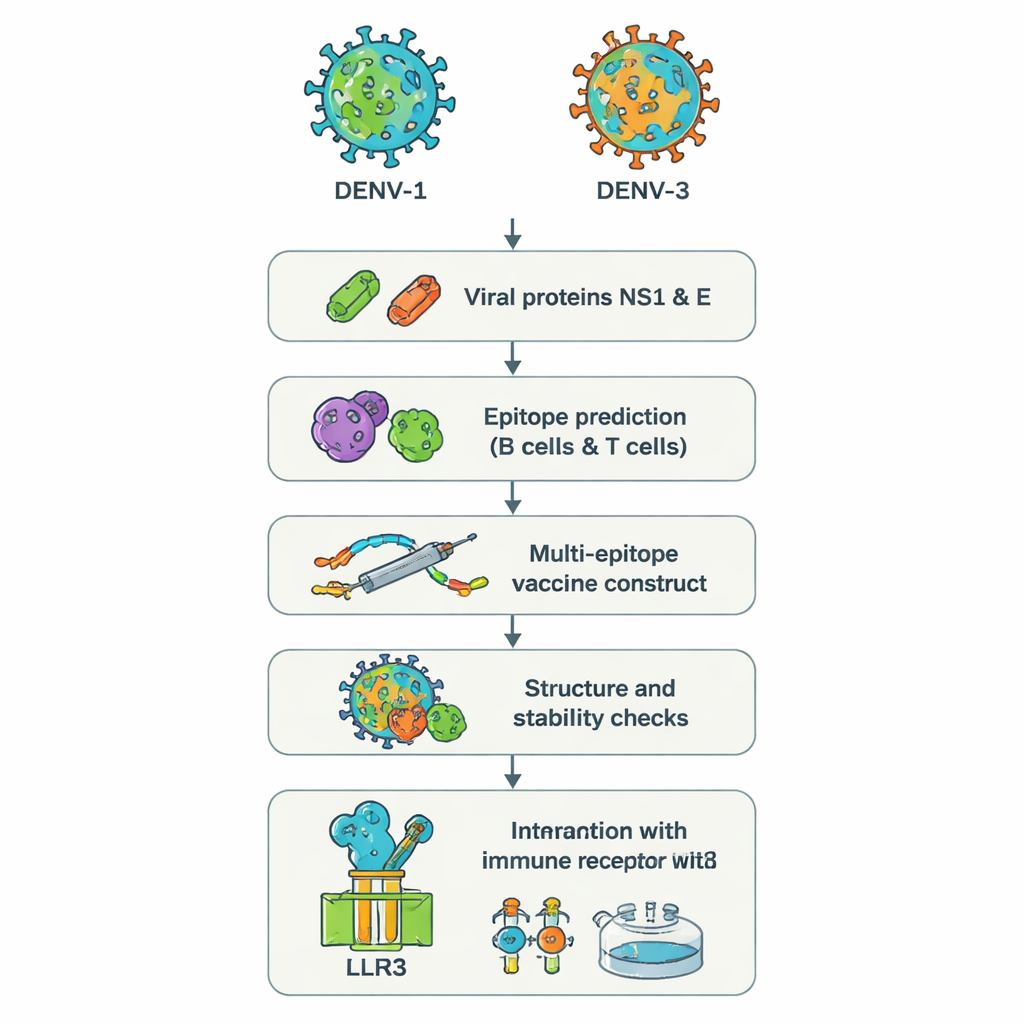
Anstatt ganze Viren im Labor zu züchten, verwendeten die Forschenden einen Ansatz, der manchmal als „Reverse Vaccinology“ bezeichnet wird. Sie begannen mit den genetischen Sequenzen zweier Dengue-Proteine, NS1 und E, aus DENV‑1 und DENV‑3. Diese Proteine sind zentral für das Eindringen des Virus in Zellen und dafür, wie das Immunsystem das Virus wahrnimmt. Leistungsfähige Webtools durchsuchten die Proteinsequenzen, um kurze Abschnitte – Epitope – zu finden, die am wahrscheinlichsten von menschlichen B‑Zellen (die Antikörper produzieren) und T‑Zellen (die infizierte Zellen töten und Antworten koordinieren) erkannt werden. Aus Hunderten von Kandidaten wählte das Team eine kleine Anzahl aus, die voraussichtlich gut vom Immunsystem sichtbar sind, zwischen den beiden Serotypen geteilt werden und hilfreiche antivirale Signale wie Interferon‑Gamma auslösen können.
Aufbau eines einzelnen multifunktionalen Impfstoffmoleküls
Die ausgewählten Epitope wurden dann digital zu einem langen künstlichen Protein zusammengesetzt, einem „Multi‑Epitop“-Impfstoff. Kurze Aminosäure‑Linker dienen als flexible Abstände, damit jedes Epitop seine Struktur behält und für Immunzellen zugänglich bleibt. Ein zusätzliches Stück, basierend auf einem natürlichen menschlichen antimikrobiellen Peptid namens Beta‑Defensin, wurde als Adjuvans hinzugefügt, um die Gesamtantwort zu verstärken. Computergestützte Analysen sagten voraus, dass das finale Konstrukt mit 575 Aminosäuren stabil, hydrophil (und damit leichter löslich) und unwahrscheinlich allergen ist. Weitere Strukturvorhersage‑Tools erzeugten ein dreidimensionales Modell und überprüften, dass die meisten Bausteine in realistischen Positionen lagen, ähnlich denen bekannter Proteinstrukturen.
Prüfung des Kandidaten in einem virtuellen Körper
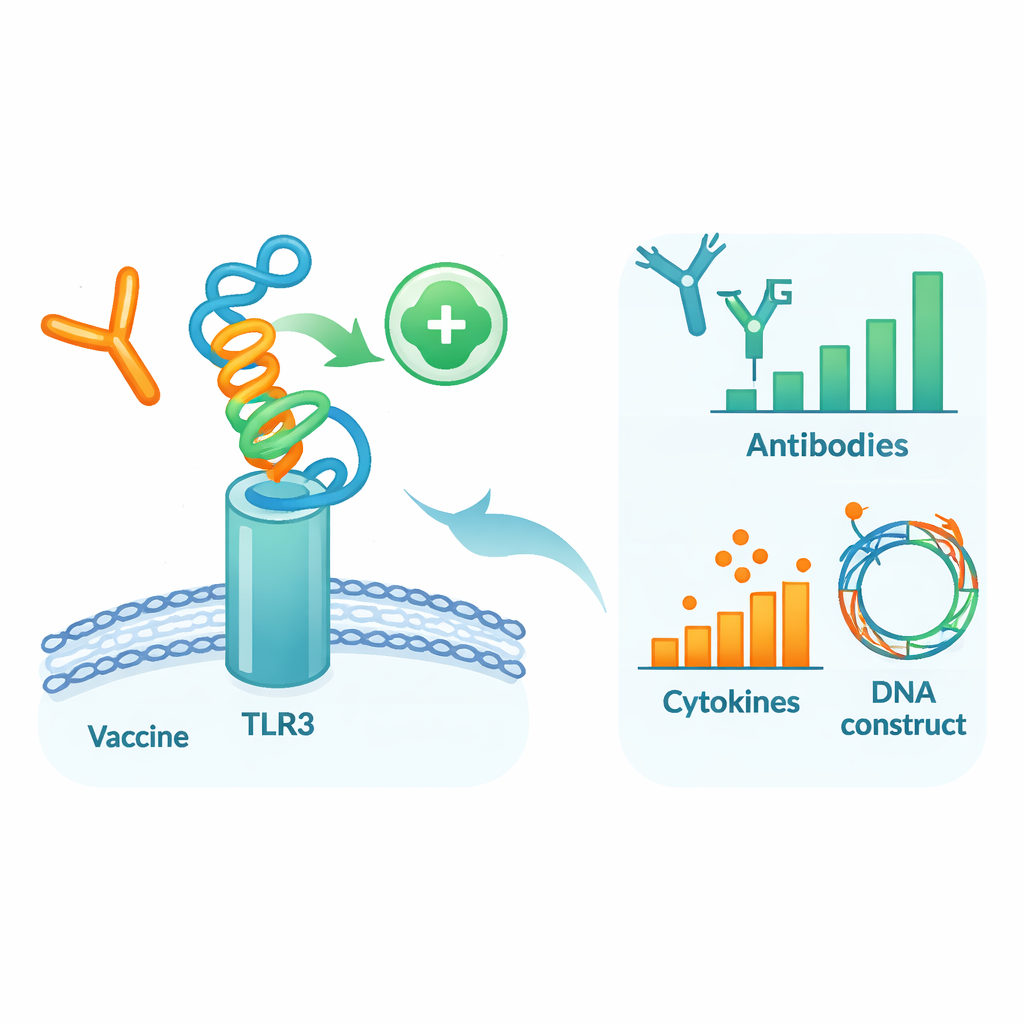
Um zu sehen, wie sich dieses entworfene Protein in einer menschenähnlichen Umgebung verhalten könnte, führten die Autorinnen und Autoren eine Reihe detaillierter Computersimulationen durch. Zuerst dockten sie das Impfstoffmodell an TLR3 an, ein Sensorprotein auf Immunzellen, das virales Material erkennt und hilft, frühe Abwehrreaktionen einzuleiten. Molekulardynamik‑Simulationen – virtuelle Filme von Atomen in Bewegung – deuteten darauf hin, dass Impfstoff und TLR3 einen stabilen Komplex bilden, gestützt durch günstige Bindungsenergien und zahlreiche Wasserstoffbrücken. Zusätzliche Analysen von Bewegung und Energie wiesen auf spezifische Bereiche beider Moleküle hin, die als Kontakt‑„Hotspots“ fungieren. Anschließend wurde ein Immunsimulationsprogramm verwendet, um drei Impfdosen über mehrere Monate zu imitieren. Das virtuelle Immunsystem erzeugte starke Wellen schützender IgG‑Antikörper, langlebige B‑ und T‑Zell‑Gedächtnisse sowie Signalstoffe, die mit einer robusten antiviralen Reaktion übereinstimmen.
Vom Computermodell zur laborbereiten Blaupause
Abschließend passten die Forschenden den genetischen Code des Impfstoffs für eine effiziente Produktion in gängigen Labormikroben an und platzierten diese optimierte DNA‑Sequenz erfolgreich in ein standardmäßiges Expressionsplasmid, bereit für zukünftige experimentelle Tests. Einfacher ausgedrückt liefert ihre Arbeit eine detaillierte Blaupause für einen neuen Dengue‑Impfstoff, der sorgfältig ausgewählte Teile von DENV‑1 und DENV‑3 adressiert, voraussichtlich stabil und sicher ist und beide Arme des Immunsystems stark ansprechen sollte. Zwar sind diese Ergebnisse rein computergestützt und müssen in Zellen, Tieren und schließlich beim Menschen bestätigt werden, doch zeigen sie, wie moderne Bioinformatik schnell maßgeschneiderte Impfstoffkandidaten für komplexe Probleme wie Dengue‑Koinfektionen erzeugen kann.
Zitation: Ishwar, D., Padavu, S., Kumar, M. et al. In silico design of a multi-epitope vaccine targeting DENV-1 and DENV-3. Sci Rep 16, 5308 (2026). https://doi.org/10.1038/s41598-026-35678-0
Schlüsselwörter: Dengue-Impfstoff, Multi‑Epitop, DENV‑1, DENV‑3, Immunoinformatik