Clear Sky Science · de
Integrative Analyse von Proteomik und Metabolomik deckt gestörten Aminosäurestoffwechsel in adriamycinresistenten akuten myeloischen Leukämiezellen auf
Warum einige Leukämie-Medikamente ihre Wirkung verlieren
Die Chemotherapie hat die Behandlung der akuten myeloischen Leukämie (AML), einer schnell wachsenden Blutkrebserkrankung, grundlegend verändert. Dennoch kehrt die Krankheit bei vielen Patienten zurück, weil die Krebszellen Wege finden, den Wirkungen der eigentlichen Abtötungsmechanismen zu widerstehen. Diese Studie stellt eine einfache, aber entscheidende Frage: Was verändert sich in Leukämiezellen, wenn sie gegen Adriamycin, eines der Standardchemotherapeutika, resistent werden, und könnten diese Veränderungen Hinweise auf neue Strategien geben, die Wirksamkeit des Medikaments wiederherzustellen?
Ein Blick in die Leukämiezellen
Um das zu untersuchen, verglichen die Forschenden eine verbreitete menschliche AML-Zelllinie namens HL60 mit einer Schwesterlinie, die gegenüber Adriamycin resistent gemacht worden war (HL60/R). Statt nur ein Gen oder Protein nach dem anderen zu betrachten, nutzten sie zwei breite, sich ergänzende Ansätze. Die Proteomik erfasste Tausende verschiedener Proteine — die Arbeitspferde, die die meisten Aufgaben in der Zelle ausführen. Die Metabolomik maß Hunderte kleiner Moleküle des Zellstoffwechsels, darunter Fette, Zucker und Aminosäuren. Durch die Kombination dieser Omics-Ebenen erstellte das Team ein detailliertes Bild davon, wie resistente Zellen sich von ihren weiter sensitiven Gegenstücken unterscheiden.
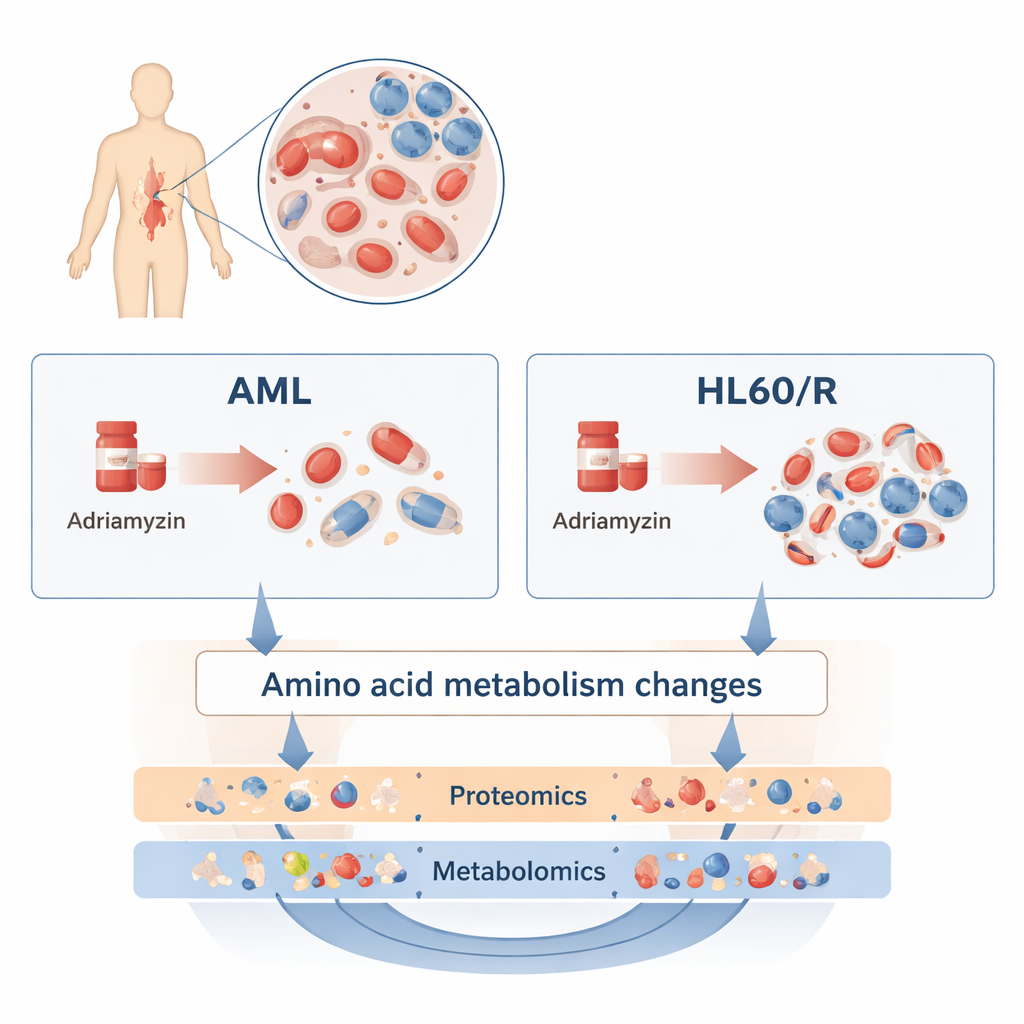
Umfangreiche Umprogrammierung der zellulären Maschinerie
Die Proteomik-Analyse zeigte weitreichende Veränderungen: Mehr als 3.200 Proteine waren in den adriamycinresistenten Zellen im Vergleich zu den normalen HL60-Zellen in höheren oder niedrigeren Mengen vorhanden. Viele dieser Proteine gruppierten sich in Signalwegen, die steuern, wie Zellen Energie nutzen und auf Stress reagieren. Insbesondere Proteine der cAMP-Signalkaskade, des HIF‑1-Wegs (der Zellen hilft, mit niedrigem Sauerstoff umzugehen) und der oxidativen Phosphorylierung (ein zentraler energieproduzierender Prozess in Mitochondrien) waren verändert. Diese Verschiebungen deuten darauf hin, dass resistente Leukämiezellen umprogrammieren, wie sie atmen, wachsen und miteinander kommunizieren, um Chemotherapie zu überstehen.
Stoffwechsel verschiebt sich hin zu Aminosäuren
Die Metabolomik lieferte eine ergänzende Erzählung. Von etwa 1.400 detektierten Metaboliten veränderten sich 260 signifikant in den resistenten Zellen. Statistische Modelle trennten resistente von nicht-resistenten Zellen klar, was auf ein konsistentes metabolisches Signaturmuster der Resistenz hinweist. Beim Abbilden der veränderten Metaboliten auf bekannte biochemische Wege traten mehrere Routen besonders hervor. Viele der stärksten Effekte betrafen Aminosäure-assoziierte Wege — die Bausteine der Proteine — insbesondere solche, die Alanin, Aspartat, Glutamat, Cystein, Methionin und Glutathion betreffen. Auch andere Netzwerke, wie Purin- und Pyrimidin-Stoffwechsel (wichtig für DNA und RNA) sowie die Verarbeitung bestimmter Lipide, waren gestört, was unterstreicht, dass Resistenz mit umfassender metabolischer Umgestaltung verbunden ist.
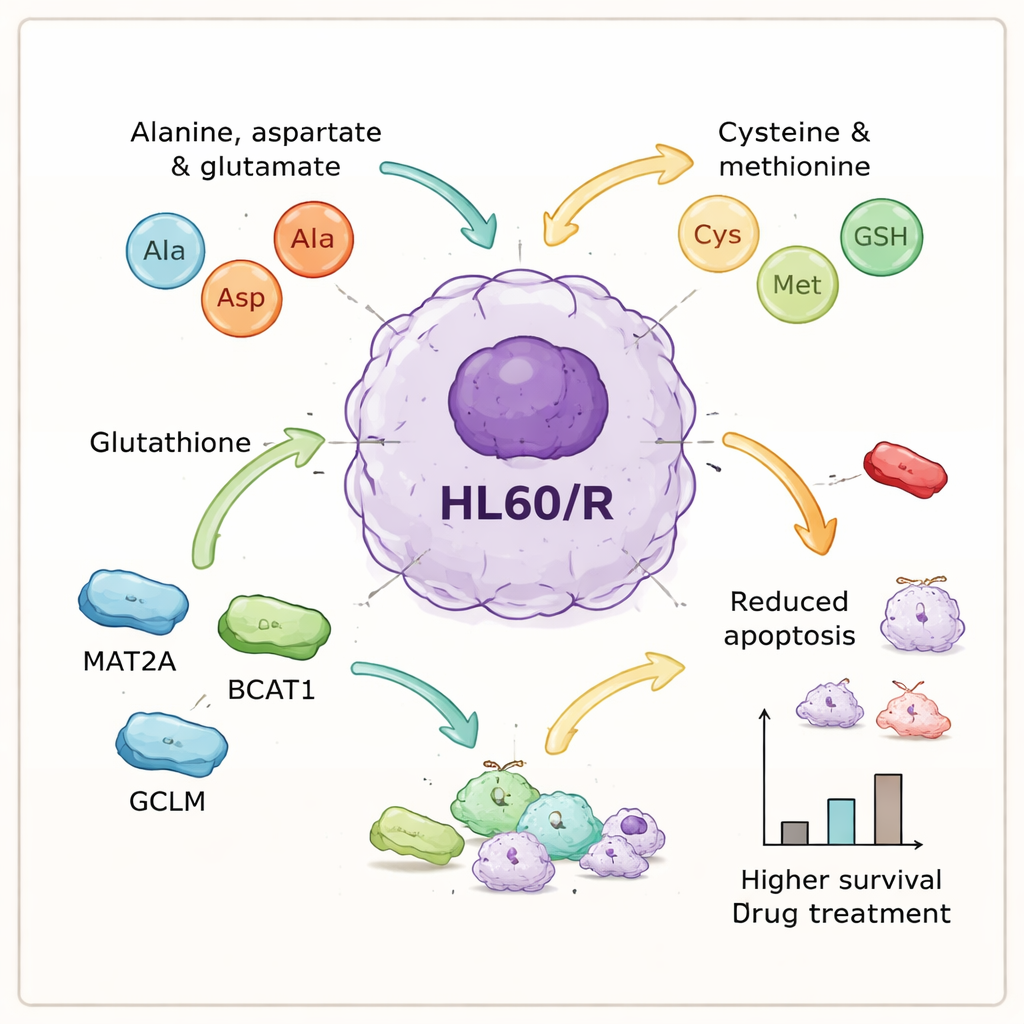
Wichtige molekulare Akteure, die Krebszellen das Überdauern ermöglichen
Durch die Integration der Protein- und Metabolitendaten konzentrierten sich die Autorinnen und Autoren auf eine Reihe aminosäurebezogener Prozesse, die zentral für die Resistenz zu sein scheinen. Sie wählten sechs Proteine, die mit diesen Pfaden verknüpft sind — GOT1, GPX1, AHCY, MAT2A, BCAT1 und GCLM — für eine genauere Untersuchung aus. Labortests bestätigten, dass fünf von ihnen in den resistenten Zellen häufiger vorkamen, was mit der Idee übereinstimmt, dass die Aminosäureverarbeitung hochgefahren ist, während ein antioxidatives Enzym, GPX1, reduziert war. Um Ursache und Wirkung zu prüfen, setzte das Team kleine interferierende RNAs ein, um drei der hochregulierten Proteine — MAT2A, BCAT1 und GCLM — in den resistenten Zellen herunterzufahren. Wurden diese Proteine herunterreguliert, zeigten die Zellen nach Behandlung deutlich mehr programmierte Zellsterblichkeit, das heißt, sie verloren einen großen Teil ihres hart erlangten Schutzes gegen Adriamycin.
Was das für künftige Therapien bedeutet
Zusammen genommen deuten diese Befunde darauf hin, dass adriamycinresistente AML-Zellen nicht nur wegen einzelner Mutationen überleben, sondern weil sie ihre interne Chemie umgestalten, wobei der Aminosäurestoffwechsel als zentrales Drehkreuz fungiert. Indem sie mehr Ressourcen in bestimmte Aminosäure- und Glutathionwege lenken, sind die Zellen offenbar besser in der Lage, Stress zu bewältigen, Schäden zu reparieren und dem Zelltod zu entgehen, wenn sie Chemotherapie ausgesetzt werden. Für Nichtfachleute ist die wichtigste Botschaft: Resistenz ist nicht zufällig, sondern folgt messbaren Mustern, die potenziell gezielt werden können. Langfristig könnten Wirkstoffe, die spezifische aminosäureverarbeitende Proteine wie MAT2A, BCAT1 oder GCLM hemmen, mit Adriamycin oder ähnlichen Mitteln kombiniert werden und Ärzten neue Optionen geben, Resistenz bei Patientinnen und Patienten mit akuter myeloischer Leukämie vorzubeugen oder zu überwinden.
Zitation: Li, C., Liang, X., Gong, S. et al. Integrative analysis of proteomics and metabolomics reveals amino acid metabolism disorder in adriamycin-resistant acute myeloid leukemia cells. Sci Rep 16, 4902 (2026). https://doi.org/10.1038/s41598-026-35675-3
Schlüsselwörter: akute myeloische Leukämie, Medikamentenresistenz, Adriamycin, Aminosäurestoffwechsel, Multi-Omics