Clear Sky Science · de
Ein funktionales und robustes zelluläres Modell für Hochdurchsatz-Screening von Piezo1-Modulatoren
Warum winzige Drucksensoren in unseren Zellen wichtig sind
Jedes Mal, wenn Blut durch unsere Gefäße strömt oder wir einfach durch einen Raum gehen, spüren unsere Zellen winzige mechanische Kräfte. Ein wichtiger "Drucksensor"-Protein namens Piezo1 hilft den Zellen, diese Kräfte in elektrische und chemische Signale umzuwandeln, die das Gewebe gesund halten. Da Piezo1 an Gefäßwachstum, Knochendichte, Immunfunktionen und seltenen genetischen Erkrankungen beteiligt ist, sind Arzneimittelentwickler daran interessiert, Moleküle zu finden, die seine Aktivität modulieren können. Die hier beschriebene Studie stellt eine neue, schnellere Methode vor, um solche Moleküle zu suchen, indem sie gentechnisch veränderte Zellen und lichtbasierte Messungen statt langsamer, arbeitsintensiver Techniken verwendet.
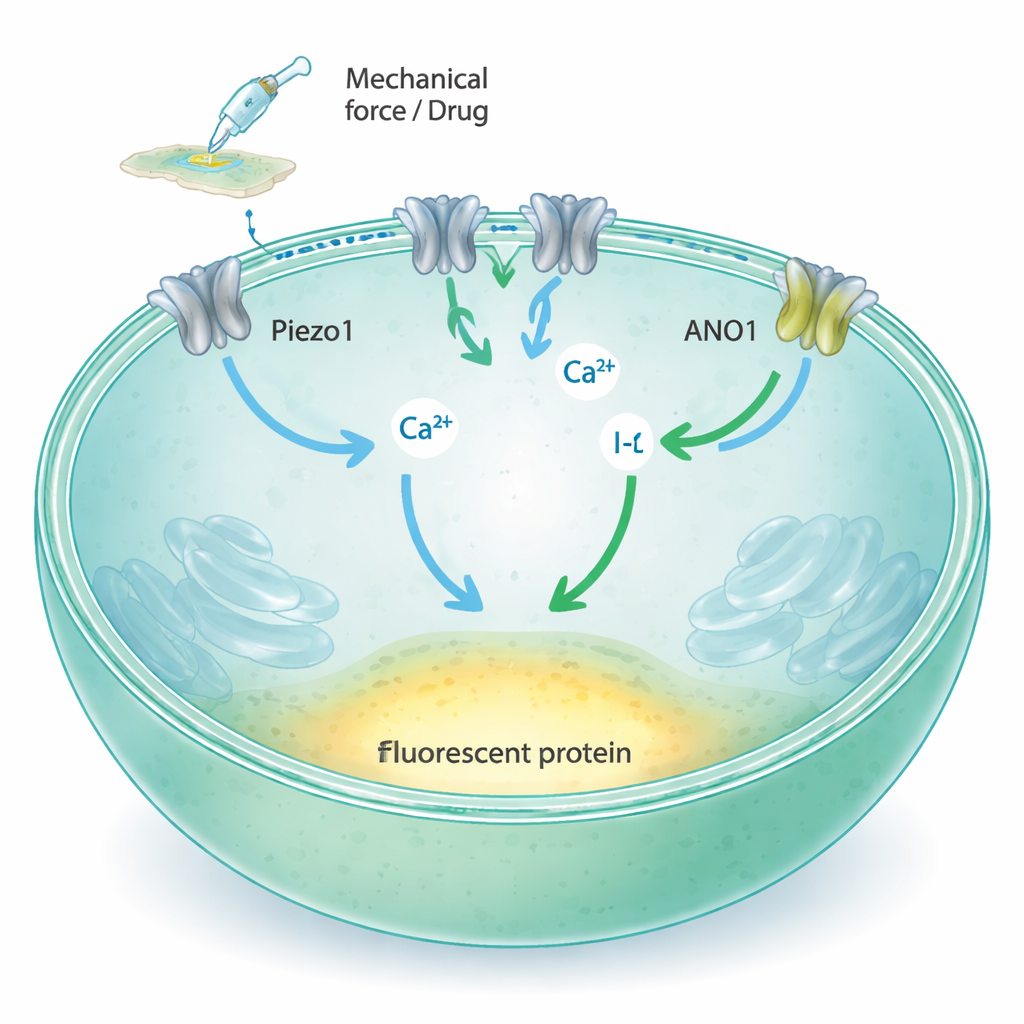
Wie Berührung in ein Lichtsignal umgewandelt wird
Piezo1 ist ein Kanal in der Zellmembran, der sich öffnet, wenn die Membran gedehnt oder gedrückt wird, und Calcium sowie andere geladene Teilchen in die Zelle strömen lässt. Traditionelle Methoden zur Untersuchung solcher Kanäle basieren auf feinen Glaselektroden oder speziellen fluoreszenten Reportern, die zwar leistungsfähig, aber schwer auf die Zehntausende von Tests skalierbar sind, die für moderne Wirkstoffsuche nötig sind. Die Autoren wollten Piezo1-Aktivität in eine einfache Lichtänderung übersetzen, die ein Plattenleser schnell über viele Proben hinweg messen kann. Ihre Idee war, Piezo1 mit zwei zusätzlichen Komponenten zu koppeln: ANO1, einem weiteren Ionenkanal, der auf Calcium reagiert, und einer modifizierten gelben fluoreszenten Proteinsorte, die bei Anwesenheit von Iodid ihre Leuchtkraft verliert.
Aufbau einer responsiven Testzelle
Die Forscher begannen mit Fischer-Ratten-Schilddrüsenzellen (FRT), die natürlich Piezo1 produzieren und gut auf Standard-Plastikplatten haften. Sie bestätigten, dass diese Zellen Piezo1, aber nicht den nahen Verwandten Piezo2 exprimieren, und zeigten, dass Piezo1 in diesen Zellen auf Flüssigkeitsströmung und mechanische Reize mit Calcium-Einstrom reagiert. Anschließend führten sie den ANO1-Kanal und das iodidsensitive Fluoreszenzprotein (YFP-H148Q/I152L) in die Zellen ein. Wenn der Calciumspiegel in der Zelle ansteigt, öffnet sich ANO1 und lässt Iodid eintreten; das Fluoreszenzprotein wird dann dunkler, sobald Iodid um es herum ansteigt. Mikroskopie, Durchflusszytometrie und elektrische Messungen zeigten, dass sowohl ANO1 als auch der Fluoreszenzsensor in hoher Menge vorhanden und funktionsfähig waren.
Vom Wirkmechanismus zu einem messbaren Leuchten
Mit diesem Drei-Komponenten-System bauten die Autoren eine einfache Ursache-Wirkungs-Kette auf: Aktiviert ein Testmolekül Piezo1, strömt Calcium ein, ANO1 öffnet sich, Iodid strömt nach innen und das Fluoreszenzsignal sinkt; blockiert ein Molekül Piezo1, bleibt das Signal hell. Sie validierten diese Logik mit bekannten Piezo1-Aktivatoren (Yoda1, Jedi1, Jedi2) und Blockern (Rutheniumrot, GsMTx4). Aktivatoren führten zu dosisabhängigen Abnahmen der Fluoreszenz, mit Empfindlichkeitswerten, die mit zuvor berichteten Daten übereinstimmen. Blocker erzeugten das umgekehrte Muster und verringerten die Antwort mit steigender Konzentration. Der Assay funktionierte nur, wenn sowohl Calcium als auch Iodid vorhanden waren, was unterstreicht, dass das Signal tatsächlich vom Piezo1-vermittelten Calciumeinstrom und dem anschließenden ANO1-vermittelten Iodideinstrom abhängt. Statistische Kennzahlen wie der Z-Faktor und das Signal-zu-Rausch-Verhältnis zeigten, dass die Methode stabil und zuverlässig genug für industrielle Screening-Anwendungen ist.
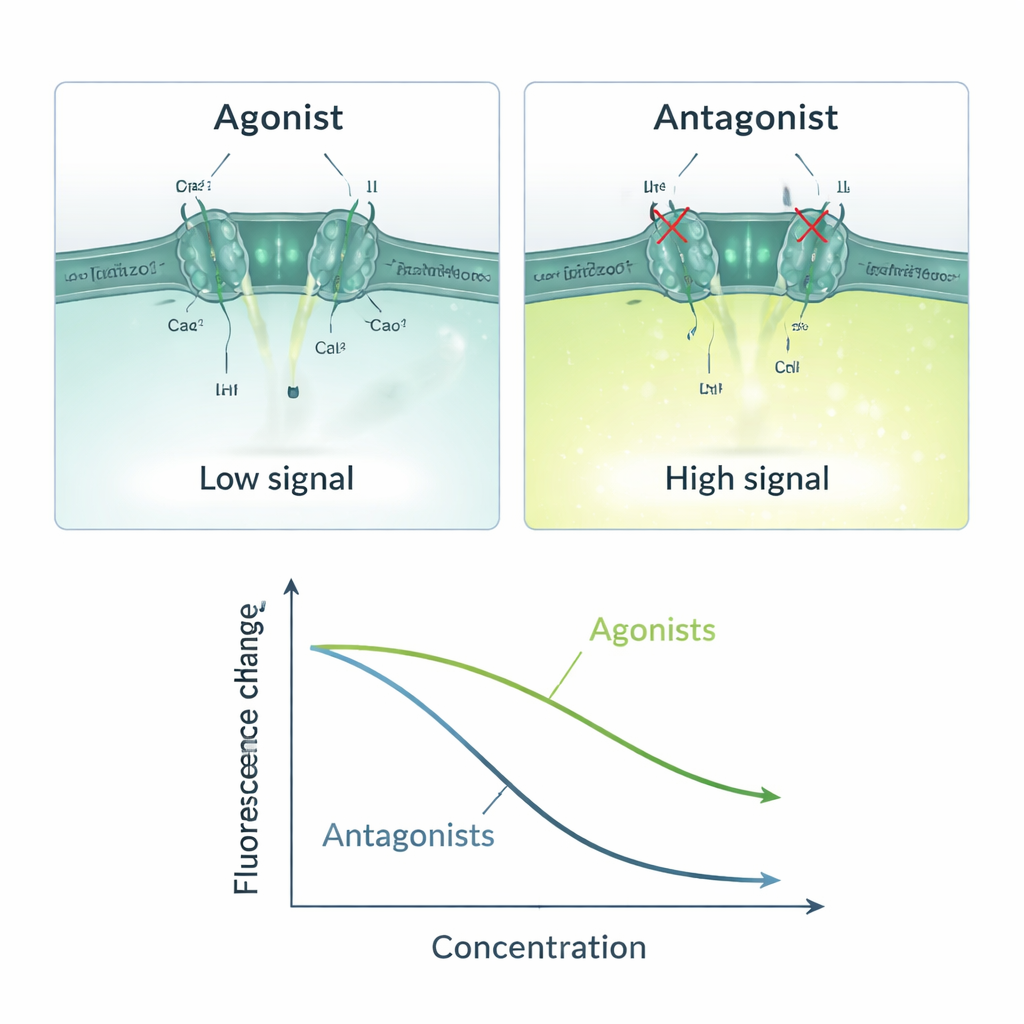
Schnelle, skalierbare Tests mit einigen Vorbehalten
Das neue Zellmodell kann eine Einzelmessung in einer Vertiefung in etwa 14 Sekunden abschließen und eine komplette 96-Well-Platte in ungefähr 22 Minuten scannen; es lässt sich zudem an Geräte anpassen, die Hunderte von Vertiefungen gleichzeitig auslesen. Die gentechnisch veränderten Zellen bleiben unter Antibiotikaselektion über viele Generationen stabil, was wiederholte Experimente über längere Zeiträume ermöglicht. Da die Messung optisch ist und Standard-Mikroplatten-Equipment verwendet, ist der Ansatz relativ kostengünstig und zugänglich. Die Autoren weisen jedoch darauf hin, dass ihr Test indirekt ist: Jede Verbindung, die Schritte vor oder nach Piezo1 in der Signalkette beeinflusst — etwa ANO1 selbst oder andere Calcium-regulierende Proteine — kann zu einem falsch-positiven Ergebnis führen. Aus diesem Grund müssen Treffer aus diesem Screen weiterhin mit direkteren Methoden wie Elektrophysiologie bestätigt werden.
Was das für zukünftige Therapien bedeutet
Alltäglich gesagt haben die Forscher einen Labor-"Rauchmelder" gebaut, der schwächer aufleuchtet, wann immer ein Stoff Piezo1 anstupst, und hell bleibt, wenn Piezo1 blockiert ist. Dieser "Alarm" ist empfindlich, schnell und leicht in großer Zahl zu betreiben, wodurch er sich gut als erster Schritt bei der Suche nach Wirkstoffen eignet, die die mechanischen Sensoren des Körpers modulieren. Während er detailliertere Nachtests nicht ersetzt, bietet dieses zelluläre Modell einen leistungsfähigen Ausgangspunkt, um Moleküle zu entdecken, die eines Tages helfen könnten, Gefäßerkrankungen, Knochenerkrankungen, Immunprobleme und andere Zustände zu behandeln, die mit der Art zusammenhängen, wie unsere Zellen physikalische Kräfte wahrnehmen und darauf reagieren.
Zitation: Liu, X., Zheng, K., Wang, Y. et al. A functional and robust cellular model for high-throughput screening of piezo1 modulators. Sci Rep 16, 6048 (2026). https://doi.org/10.1038/s41598-026-35673-5
Schlüsselwörter: Piezo1-Kanal, mechanosensitive Ionenkanäle, Hochdurchsatz-Screening, Zellbasierter Assay, Arzneimittelentdeckung