Clear Sky Science · de
Synthese, Charakterisierung, DFT-Analyse, molekulares Docking und krebshemmende Untersuchungen bei kolorektalem Karzinom eines neuartigen Pyrazol‑Hydrazon‑Zink(II)-Komplexes
Warum ein metallbasiertes Medikament Darmkrebs schonender bekämpfen könnte
Viele wirksame Krebsmedikamente basieren auf schweren Metallen wie Platin. Sie können effektiv sein, gehen aber oft mit starken Nebenwirkungen und mit der Zeit mit Resistenzbildung einher. Diese Studie verfolgt einen anderen Ansatz: ein neuer Wirkstoffkandidat, der auf Zink aufbaut — einem essenziellen Nährstoff, der bereits im Körper vorkommt — kombiniert mit einem organischen Gerüst, dem Pyrazol‑Hydrazon. Die Forschenden fragten, ob die Bindung von Zink an dieses Gerüst eine Verbindung schaffen könnte, die Darmkrebszellen stark trifft, dabei aber gesunde Zellen schont.
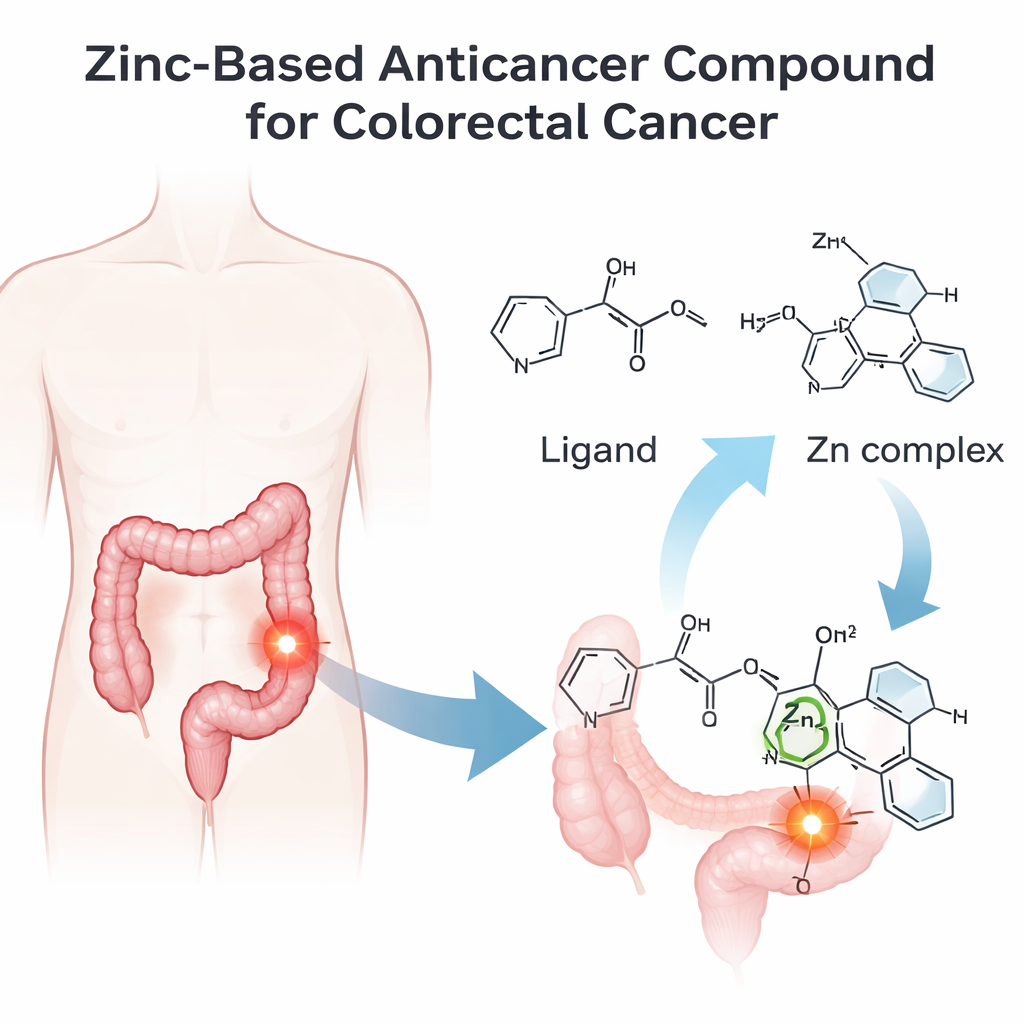
Bau eines intelligenteren zinkbasierten Moleküls
Das Team entwarf und synthetisierte zunächst ein neues organisches Molekül, bezeichnet als IMP, und koordinierte es anschließend an ein Zinkion, um den Zinkkomplex IMP‑Zn zu bilden. Sie bestätigten die genaue Struktur beider Verbindungen mit einer Reihe von Techniken, die Moleküle wie Fingerabdrücke charakterisieren: Infrarotspektroskopie zur Erkennung chemischer Bindungen, Kernspinresonanz zur Positionsbestimmung der Atome, Massenspektrometrie zur Verifizierung des Molekulargewichts und UV–Vis‑Spektroskopie zur Untersuchung der Lichtwechselwirkung. Diese Experimente zusammen mit Leitfähigkeitsmessungen zeigten, dass das Zink fest an drei Schlüsselsauerstoffe des IMP und zwei Chloridionen koordiniert ist und so einen einzelnen, klar definierten zinkzentrierten Komplex bildet.
Ein Blick ins Molekül mit virtueller Chemie
Als Ergänzung zu den Laborbefunden führten die Forschenden detaillierte Computersimulationen mittels Dichtefunktionaltheorie (DFT) durch. Diese Rechnungen ermöglichten Vorhersagen zur Elektronenverteilung in IMP und IMP‑Zn, zur Stabilität jeder Form und zur Reaktionsbereitschaft der Moleküle. Die Ergebnisse zeigten, dass sich nach der Zinkkoordination die Energielücke zwischen den „Frontier“-Orbitalen verkleinert, sodass sich Elektronen leichter im Gebilde bewegen können. Das geht in der Regel mit höherer chemischer Reaktivität einher. Der Zinkkomplex wies zudem einen erhöhten sogenannten Elektrophilie‑Index auf, was darauf hindeutet, dass er besser dazu geeignet ist, mit biologischen Zielstrukturen zu interagieren als der freie Ligand IMP allein.
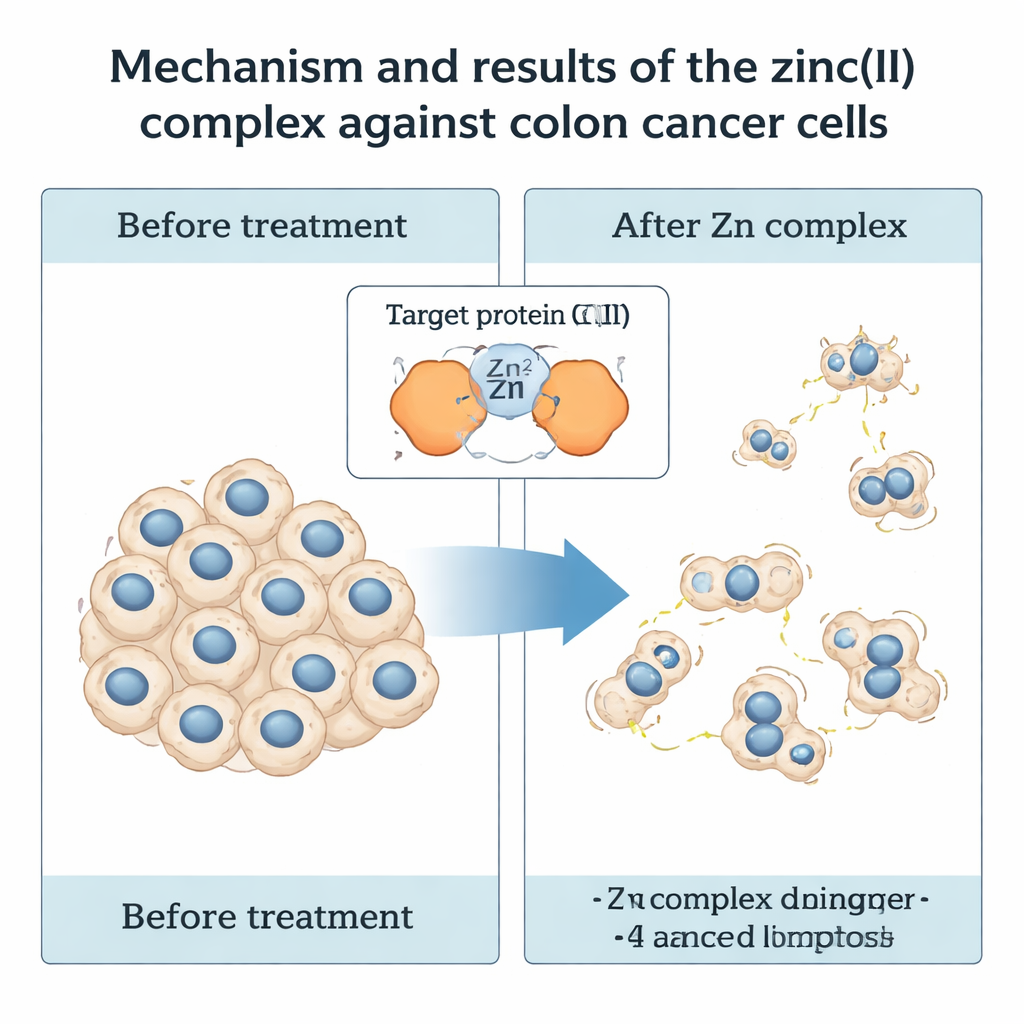
Wie der Zinkkomplex Darmkrebszellen angreift
Der eigentliche Test war biologisch. Die Forschenden behandelten menschliche kolorektale Krebszellen (HCT116) mit IMP und IMP‑Zn in unterschiedlichen Dosen und Zeiträumen und bestimmten anschließend die Überlebensrate der Zellen. Beide Verbindungen hemmten das Wachstum der Krebszellen, doch der Zinkkomplex war deutlich wirksamer: Nach 48 Stunden halbierte IMP‑Zn die Zellviabilität bei etwa 25 Mikromolar, während der Ligand allein eine deutlich höhere Dosis benötigte. Ebenso wichtig: Dieselben Konzentrationen von IMP‑Zn zeigten keine messbare Toxizität gegenüber einer normalen menschlichen Nierenzelllinie (HEK293), was auf eine gewisse Selektivität gegenüber Krebszellen hinweist. Beobachteten die Forschenden die behandelten Krebszellen über zwei Wochen, stellten sie fest, dass IMP‑Zn sowohl die Zahl als auch die Größe der Kolonien stark verringerte — ein Hinweis darauf, dass es die Fähigkeit zur langfristigen Proliferation beeinträchtigt.
Hinweise darauf, dass die Zellen in programmierenden Zelltod gedrängt werden
Um zu verstehen, wie der Zinkkomplex Krebszellen schädigt, untersuchten die Wissenschaftler den Zellzyklus — die Abfolge von Stadien, die Zellen beim Wachstum und bei der Teilung durchlaufen. Nach Exposition gegenüber IMP‑Zn verschob sich ein deutlich größerer Anteil der HCT116‑Zellen in die "SubG0"‑Phase, ein Kennzeichen für Zellen mit fragmentierter DNA. Dieses Muster ist häufig mit Apoptose assoziiert, einer kontrollierten Form des Zelltods, die viele Krebsmedikamente anstreben. Molekulare Docking‑Simulationen lieferten ein weiteres Puzzlestück: Die virtuellen Modelle legen nahe, dass IMP‑Zn stärker bindet als IMP an mehrere krebsrelevante Proteine, darunter eine Wachstumsfaktor‑Rezeptorkinase, eine an der Zellzyklusregulation beteiligte Kinase und ein Medikamenten‑metabolisierendes Enzym. Diese stärkeren Wechselwirkungen unterstützen die Idee, dass die Zinkkoordination dem Komplex hilft, an kritische zelluläre Maschinen zu binden und so das Überleben der Krebszellen zu stören.
Was das für künftige Behandlungen bedeuten könnte
Insgesamt zeigt die Studie, dass das „Dekorieren“ eines Pyrazol‑Hydrazon‑Gerüsts mit Zink mehr bewirkt als nur eine chemische Feinabstimmung: Es verwandelt IMP in einen reaktiveren, potenteren und offenbar selektiveren Wirkstoff gegen kolorektale Krebszellen. Zwar ist IMP‑Zn noch weit davon entfernt, ein fertig entwickeltes Medikament zu sein — es muss noch in Tiermodellen und am Menschen getestet werden —, doch seine Fähigkeit, das Wachstum von Darmkrebszellen deutlich zu verlangsamen, die Zellen in Richtung Apoptose zu treiben und normale Zellen zu verschonen, macht es zu einem vielversprechenden Vertreter einer wachsenden Klasse zinkbasierter Metallmedikamente. Die Arbeit legt nahe, dass sorgfältig gestaltete Zinkkomplexe künftig schonendere, gezielte Alternativen oder Ergänzungen zur traditionellen metallbasierten Chemotherapie bieten könnten.
Zitation: Mermer, A., Bayrak, A.M., Bolat, Z.B. et al. Synthesis, characterization, DFT analysis, molecular docking and anticancer investigations in colorectal carcinoma of a novel pyrazole-hydrazone zinc(II) complex. Sci Rep 16, 6391 (2026). https://doi.org/10.1038/s41598-026-35664-6
Schlüsselwörter: Zinkbasierte Wirkstoffe gegen Krebs, kolorektales Karzinom, Pyrazol‑Hydrazon‑Komplex, molekulares Docking, Apoptose