Clear Sky Science · de
Radiosensibilisierende Effekte von Silbernanopartikeln auf Angiogenese und Matrix-Metalloproteinase-Signalgebung in triple-negativen Brustkrebszelllinien
Wie man aggressive Brustkrebse verwundbarer macht
Triple-negativer Brustkrebs ist eine der schwersten Formen von Brustkrebs zu behandeln. Er wächst oft schnell, breitet sich früh aus und fehlt die üblichen molekularen „Griffe“, an denen viele moderne Medikamente ansetzen. Strahlentherapie ist häufig Teil der Behandlung, doch diese Tumoren können hartnäckig resistent sein. Die Studie stellt eine einfache, aber spannende Frage: Können winzige Silberpartikel die Wirkung von Strahlung verbessern und zugleich die Fähigkeit des Tumors einschränken, neue Blutgefäße zu bilden und sich auszubreiten?
Winzige Silberhelfer für die Strahlentherapie
Die Forschenden konzentrierten sich auf Silbernanopartikel – ultrakleine Silberkügelchen im Nanometerbereich. Da Silber eine hohe Dichte hat und stark mit Röntgenstrahlung wechselwirkt, können diese Partikel die Effekte der Strahlung genau dort konzentrieren, wo sie sich anreichern. Das Team arbeitete mit zwei weit verbreiteten Labor-Modellen des triple-negativen Brustkrebses und verglich sie mit einer nicht krebsartigen Brustzelllinie. Zunächst testeten sie die alleinige Toxizität der Silbernanopartikel und fanden, dass Krebszellen bei deutlich niedrigeren Dosen abgetötet wurden als normale Zellen, was auf ein günstiges therapeutisches Fenster hindeutet. Mithilfe mathematischer Analysen der Wechselwirkung zwischen Partikeln und Strahlung zeigten sie, dass die Kombination beider Behandlungen eine eindeutig stärkere krebsabtötende Wirkung erzielte als jede einzelne Behandlung für sich.
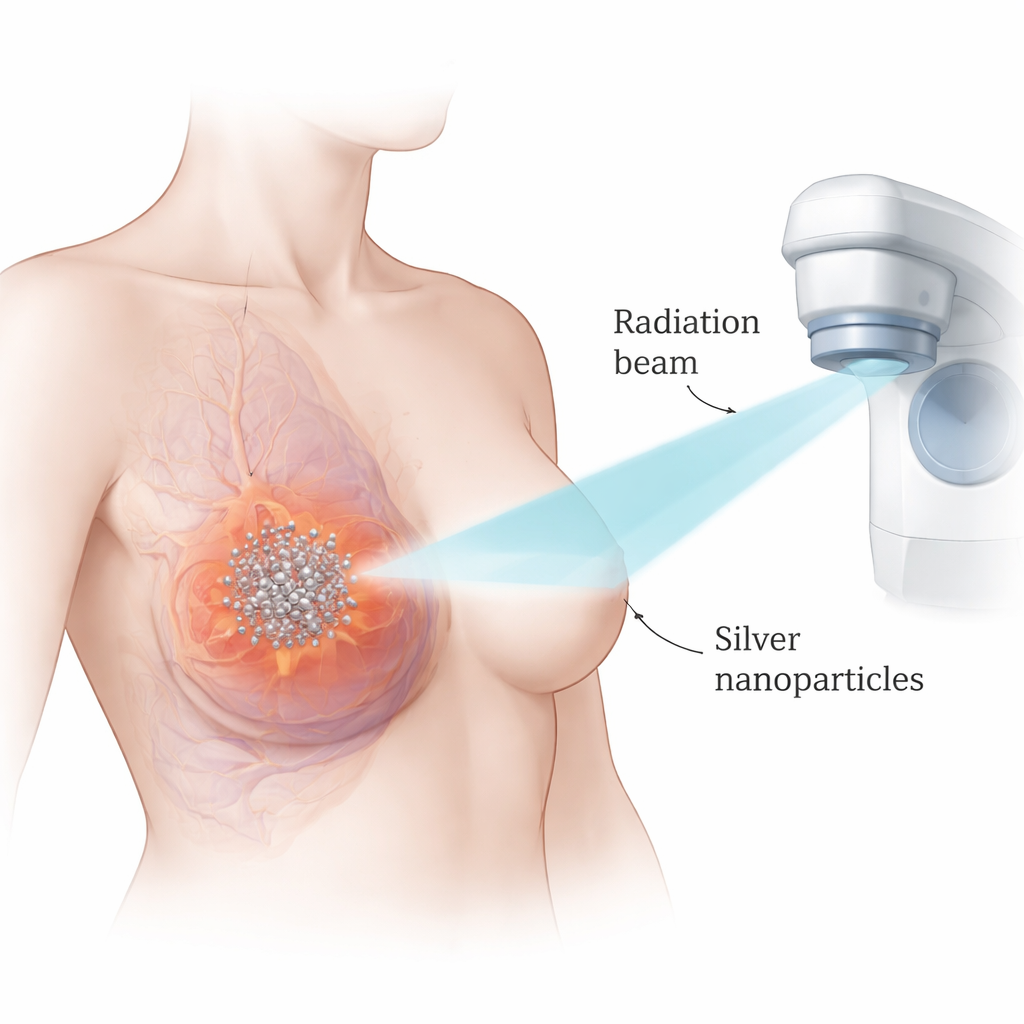
Krebszellen in den programmierten Zelltod treiben
Als Nächstes untersuchten die Wissenschaftler, wie die kombinierte Behandlung Zellen tötet. Sie maßen Apoptose, eine Form des programmierten Zelltods, und verfolgten die Anhäufung hochreaktiver Moleküle, bekannt als reaktive Sauerstoffspezies (ROS). Es ist bereits bekannt, dass Strahlung teilweise über die Erzeugung von ROS wirkt, die die DNA schädigen. In beiden triple-negativen Zelllinien erhöhten Silbernanopartikel allein Apoptose und ROS-Level, ebenso tat dies die Strahlung allein – doch die Kombination trieb beide Messwerte dramatisch nach oben. Das bedeutet, dass mehr Krebszellen in einen geordneten Selbstzerstörungsmodus gedrängt wurden, statt in einem beschädigten Zustand zu verharren, der manchmal Rückfälle oder Resistenz begünstigen kann.
Blutzufuhr abschneiden und Ausbreitung verlangsamen
Tumoren sind auf Blutgefäße angewiesen, die Sauerstoff und Nährstoffe liefern, und aggressiver Krebs kann sogar Blutgefäßfunktionen nachahmen. Das Team betrachtete zwei wichtige molekulare Schalter, die am Aufbau und der Stabilisierung von Tumorgefäßen beteiligt sind: VEGFR2 und Tie2. In beiden Zelllinien reduzierten Silbernanopartikel die Aktivität dieser Gene, und die Kombination mit Strahlung schaltete sie noch weiter herunter. Außerdem untersuchten sie zwei Enzyme, MMP-2 und MMP-9, die Krebszellen helfen, das umgebende Gewebe zu durchdringen und zu migrieren. In einem der Zellmodelle senkten sowohl Strahlung als auch Silbernanopartikel diese Enzyme, während die kombinierte Behandlung den stärksten Effekt zeigte. Als die Forschenden beobachteten, wie Krebszellen in eine künstliche „Kratzsonne“ in einer Schale einwanderten, und wie gut gefäßähnliche Röhrchen in einem Ko-Kultur-System entstanden, verlangsamte die Kombinationstherapie am deutlichsten Migration und Röhrenbildung.
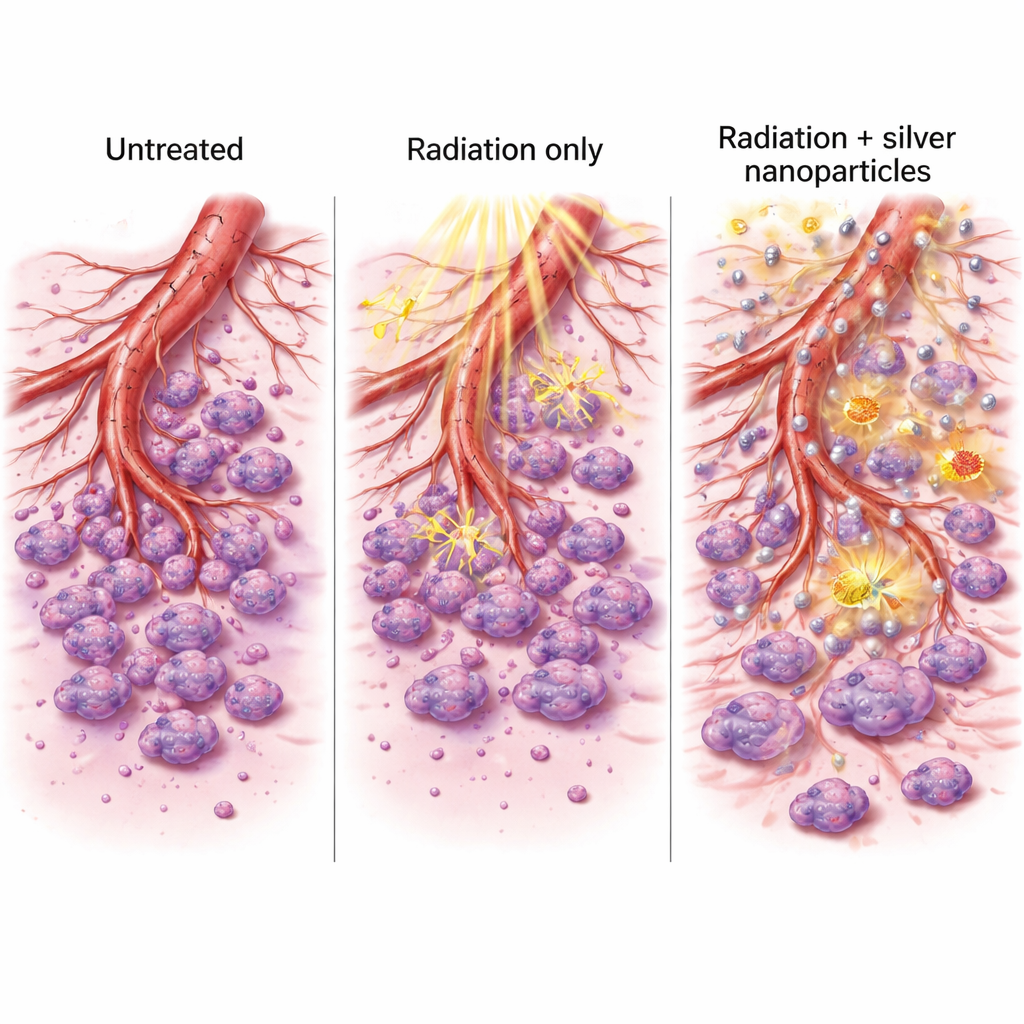
Warum diese Veränderungen wichtig sind
Indem Gene gedrosselt wurden, die neues Blutgefäßwachstum fördern, sowie Enzyme, die Zellen beim Eindringen unterstützen, bewirkte die Kombination aus Silber und Strahlung mehr als nur das Abtöten von Krebszellen. Sie störte auch die Unterstützungssysteme, die Tumoren zum Wachsen und zur Ausbreitung nutzen. Die behandelten Zellen konnten Wunden in Laborschalen schlechter verschließen und sich weniger gut zu verzweigten Netzwerken organisieren, die frühen Blutgefäßen ähneln. Zusammen mit dem starken Anstieg von Zelltod und ROS-Produktion deuten diese Effekte auf einen zweifachen Nutzen hin: ein stärkerer direkter Angriff auf den Tumor und eine Abschwächung der Werkzeuge für späteres Wachstum und Metastasierung.
Was das für Patientinnen und Patienten bedeuten könnte
Derzeit stammen diese Ergebnisse aus im Labor gezüchteten Krebszellen, nicht aus Patientenstudien. Dennoch zeichnen sie ein hoffnungsvolles Bild. Silbernanopartikel wirkten als Radiosensibilisierer und machten die Standardstrahlentherapie gegenüber triple-negativen Brustkrebszellen wirksamer. Gleichzeitig schienen sie die Fähigkeit des Tumors zu unterbinden, Blutversorgungsnetze aufzubauen und in umliegendes Gewebe einzudringen. Falls zukünftige Tier‑ und klinische Studien bestätigen, dass diese Partikel sicher und gezielt in Tumoren abgeliefert werden können, könnten sie Ärzten helfen, niedrigere Strahlendosen zu verwenden und gleichzeitig bessere Ergebnisse zu erzielen — und so einen neuen Weg bieten, eine der herausforderndsten Formen von Brustkrebs anzugehen.
Zitation: Montazersaheb, S., Farahzadi, R., Mansouri, E. et al. Radiosensitizing effects of silver nanoparticles targeting angiogenesis and matrix metalloproteinase signaling in triple negative breast cancer cell lines. Sci Rep 16, 6820 (2026). https://doi.org/10.1038/s41598-026-35662-8
Schlüsselwörter: triple-negativer Brustkrebs, Silbernanopartikel, Strahlentherapie, Angiogenese, Metastasierung