Clear Sky Science · de
Chlorierte Bis-4-hydroxycoumarine unterdrücken die Replikation von Flaviviren durch Hemmung der Translation und Replikation von Dengue‑Virus Typ 2
Neue Hoffnungen gegen von Mücken übertragene Viren
Dengue‑ und Zika‑Viren infizieren jedes Jahr Hunderte Millionen Menschen, häufig in Regionen mit begrenzten medizinischen Ressourcen. Impfstoffe bieten nur teilweisen Schutz, und es gibt noch kein breit eingesetztes antivirales Medikament, das Ärztinnen und Ärzte bei den ersten Symptomen verordnen können. Diese Studie untersucht eine Familie im Labor hergestellter Chemikalien, die von Pflanzenstoffen abgeleitet sind, und stellt eine einfache, aber dringliche Frage: Kann eine davon verlässlich die Vermehrung dieser Viren in menschlichen Zellen verlangsamen, ohne die Zellen selbst zu schädigen?
Pflanzeninspirierte Moleküle als Virenblocker
Die Forschenden konzentrierten sich auf Coumarine, eine Klasse natürlicher Verbindungen, die in vielen Pflanzen vorkommen und seit langem für ihr antimikrobielles und antivirales Potenzial bekannt sind. Sie testeten zwölf „Biscoumarin“-Derivate – also zwei gekoppelte Coumarin‑Einheiten – gegen Dengue‑Virus Typ 2 und Zika‑Virus in Zellkulturen. Durch Messung der produzierten infektiösen Partikel und der Zellgesundheit stellten sie fest, dass zwei chlorierte Varianten, bezeichnet als Verbindung 3 und Verbindung 4, besonders vielversprechend waren. In niedrigen Mikromolar‑Konzentrationen reduzierten diese chlorierten Bis‑4‑hydroxycoumarine die Virusproduktion um mehr als 90 % und schonten dabei den Großteil der Zellen.
Chemie feintunen für stärkeren Schutz
Nicht jede chemische Veränderung war gleichermaßen effektiv. Durch systematisches Abändern von Atomen rund um einen ringförmigen Bereich der Moleküle fanden die Forschenden heraus, dass das Anbringen von Chlor an bestimmten Positionen die beste antivirale Aktivität lieferte. Der Austausch von Chlor gegen andere Halogene wie Fluor oder Brom – oder das Hinzufügen anderer chemischer Gruppen – schwächte meist die Wirkung gegen Dengue und Zika. Mithilfe computergestützter Modelle verknüpften sie die antivirale Stärke mit einfachen molekularen Merkmalen wie der Ladungsverteilung im Molekül und der exponierten Oberfläche. Methoden des maschinellen Lernens erfassten diese Zusammenhänge deutlich besser als ältere statistische Werkzeuge, was darauf hindeutet, dass künstliche Intelligenz die Entwicklung verbesserter Anti‑Dengue‑Wirkstoffkandidaten leiten kann.
Wie die Verbindungen den Virenlebenszyklus stören
Einmal in der Zelle nutzt das Dengue‑Virus sein RNA‑Genom als Vorlage, um ein langes Polyprotein zu produzieren, das in funktionelle Teile geschnitten wird, und kopiert dann seine RNA, um neue Viren zu erzeugen. Die Studie zeigt, dass Verbindungen 3 und 4 hauptsächlich in diese Schritte der Translation und Replikation eingreifen. In infizierten Zellen fielen die Mengen eines wichtigen viralen Hüllproteins drastisch ab, wenn die Verbindungen vorhanden waren, und ein Reportersystem, das die virale RNA‑Replikation verfolgt, schwächte sich ebenfalls dosisabhängig ab. Biochemische Tests und Computerdocking deuteten auf ein virales Enzym, die NS5‑Methyltransferase, als direkten, wenn auch relativ schwachen Zielpunkt hin: Die Verbindungen konnten die RNA‑„Capping“‑Funktion hemmen, jedoch bei weitem nicht so stark wie ein bekannter Referenzinhibitor. Außerdem verlangsamten sie moderat die virale Protease, ein weiteres Enzym, das das virale Polyprotein zerschneidet.
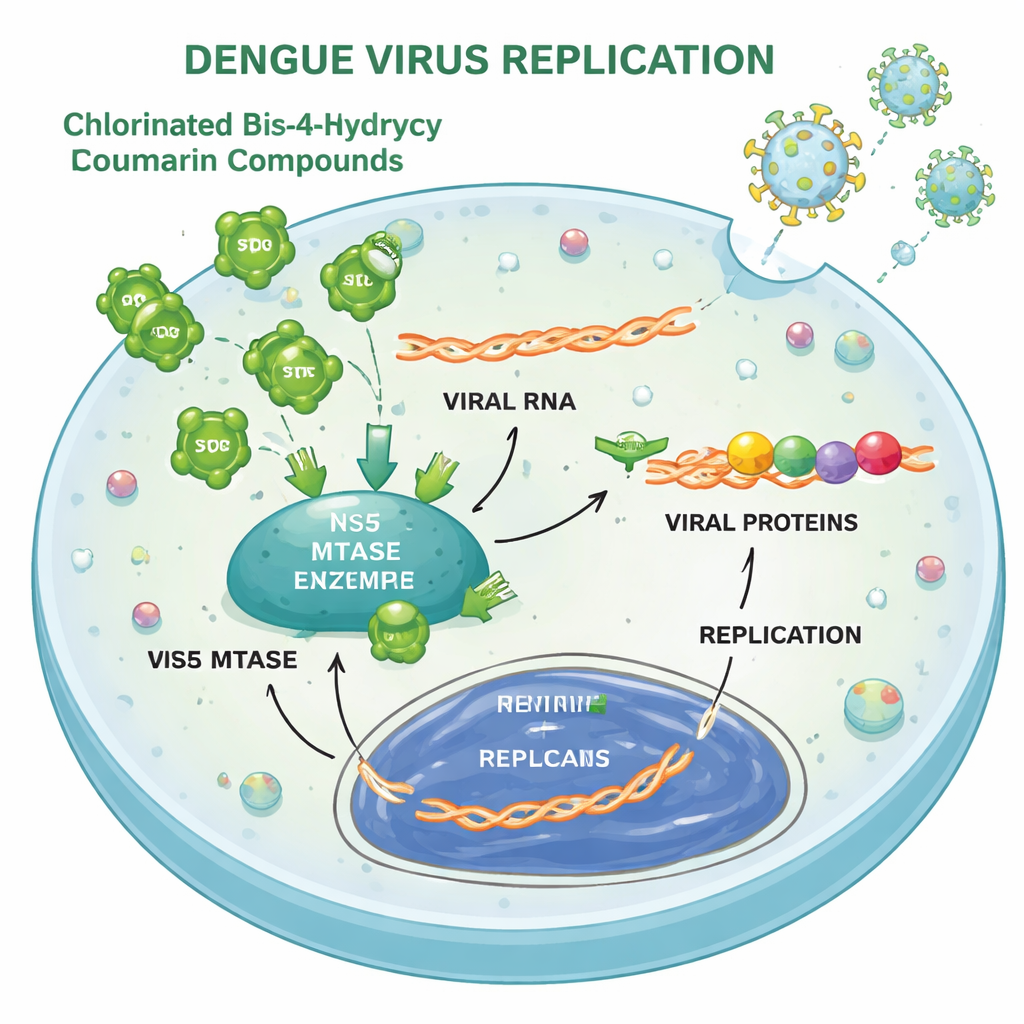
Viren tun sich schwer, sich anzupassen
Viren entkommen Medikamenten oft durch Mutationen. Um zu prüfen, ob das hier passieren könnte, züchtete das Team Dengue‑Virus wiederholt in Zellen, die über viele Infektionszyklen hinweg den neuen Verbindungen ausgesetzt waren. Tatsächlich traten mehrere Veränderungen in einem anderen viralen Protein, NS4B, auf, das dabei hilft, Zellmembranen in kleine Taschen zu biegen, in denen die Replikation stattfindet. Überraschenderweise waren diese mutierten Viren nicht weniger empfindlich gegenüber den Verbindungen als der ursprüngliche Stamm. Computervorhergesagte Strukturen legten nahe, dass die Gesamtform von NS4B weitgehend erhalten blieb. Dieses Muster deutet darauf hin, dass die Mutationen allgemeine Anpassungen an Stress waren, keine echte Resistenz. Es stützt auch die Idee, dass die Verbindungen an mehreren Stellen der Replikationsmaschinerie oder an Wirtsfaktoren wirken, die das Virus nur schwer umprogrammieren kann.
Warum diese Ergebnisse für zukünftige Behandlungen wichtig sind
Für Nicht‑Fachleute lautet die Kernaussage, dass die Forschenden ein neues chemisches „Gerüst“ gefunden haben, das Dengue‑ und Zika‑Viren an mehreren Punkten ihres Lebenszyklus verlangsamen kann, insbesondere bei der Translation ihrer Gene und der Kopie ihrer RNA in Zellen. Das vielversprechendste Molekül, Verbindung 3, wirkt in niedrigen Dosen, schadet den Zellen vergleichsweise wenig, trifft alle vier wichtigen Dengue‑Typen sowie Zika und treibt das Virus im Labor nicht schnell zu Resistenzen. Obwohl diese chlorierten Bis‑4‑hydroxycoumarine noch weit von Arzneimitteln entfernt sind, bieten sie einen soliden Ausgangspunkt für Chemiker und Virologen, um sie zu verfeinern, in Tierversuchen zu testen und schließlich mit anderen Medikamenten zu kombinieren – Schritte, die uns einem dringend benötigten antiviralen Wirkstoff gegen von Mücken übertragene Infektionen näherbringen könnten.
Zitation: Loeanurit, N., Phan, THT., Hengphasatporn, K. et al. Chlorinated bis-4-hydroxycoumarins suppress flavivirus replication by inhibiting dengue virus type 2 translation and replication. Sci Rep 16, 5300 (2026). https://doi.org/10.1038/s41598-026-35654-8
Schlüsselwörter: Dengue‑Virus, Zika‑Virus, antivirale Verbindungen, Coumarin‑Derivate, Virusreplikation