Clear Sky Science · de
DFT-Berechnung der Komplexierung von Ac3+ und Bi3+ mit dem hybriden Chelator 3p-C-DEPA für zielgerichtete Alphatherapie
Warum diese Forschung für die Krebsbehandlung wichtig ist
Die moderne Krebsmedizin setzt zunehmend auf radioaktive Wirkstoffe, die Tumoren Zelle für Zelle aufspüren können. Ein kraftvoller Ansatz, die zielgerichtete Alphatherapie, nutzt hochenergetische Partikel, die einzelne Krebszellen mit hoher Präzision abtöten können. Um diese Partikel sicher zu transportieren, muss das radioaktive Metall jedoch in einem winzigen molekularen „Käfig“ eingeschlossen werden, damit es nicht in gesundes Gewebe gelangt. Diese Studie untersucht ein neues Käfigmolekül, 3p‑C‑DEPA, das dafür entworfen wurde, besonders anspruchsvolle Metalle wie Actinium‑225 und Bismut‑213 zu binden, und stellt die Frage: Kann es diese Metalle stärker halten als der derzeit verbreitete Chelator DOTA?
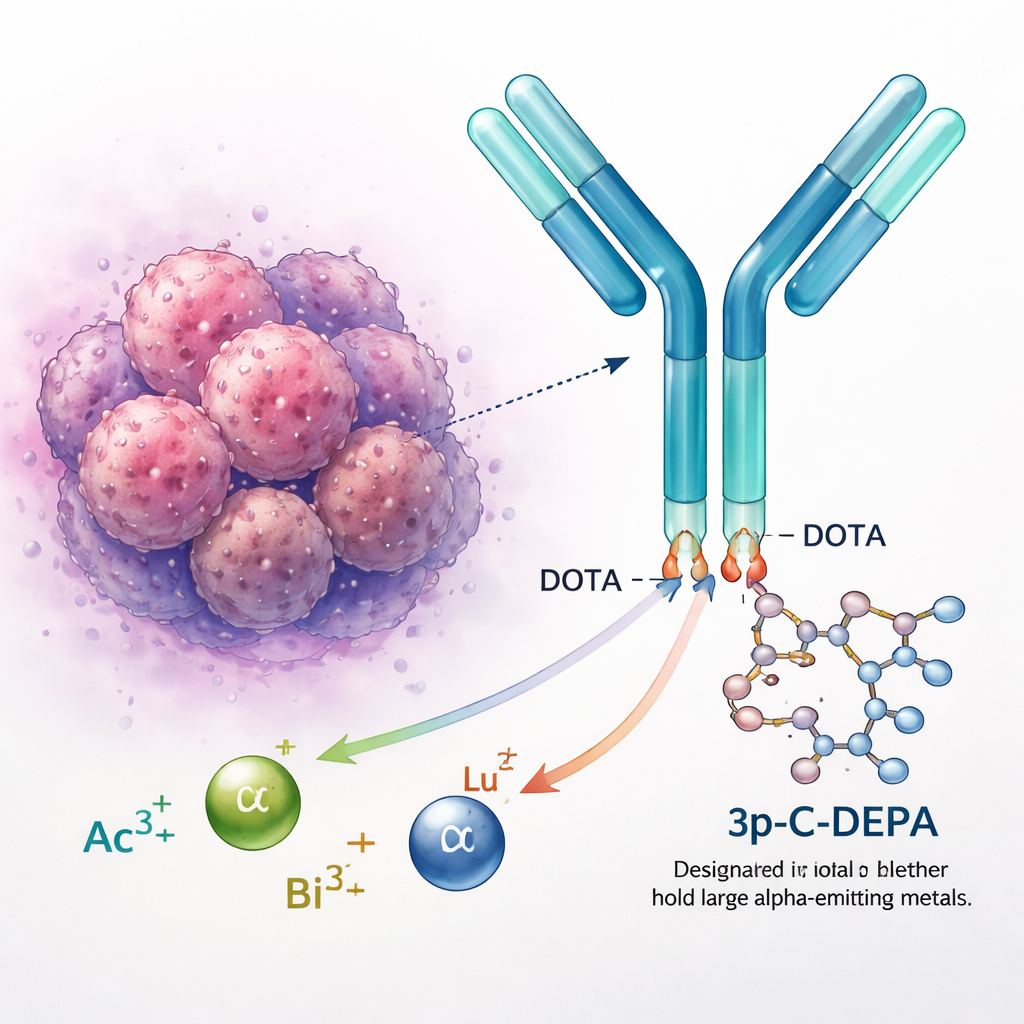
Radioaktive Metalle sicher fixieren
Radioaktive Metalle wie Actinium, Bismut und Lutetium werden zur Diagnose und Behandlung von Krebs eingesetzt. Allein stehend würden diese positiv geladenen Metallionen jedoch frei mit dem Körper interagieren und möglicherweise gesunde Organe schädigen. Chemiker befestigen sie daher an „Chelatoren“, ringförmigen Molekülen, die das Metall umschließen und an seinem Platz halten. Der Goldstandard Chelator DOTA wird in mehreren zugelassenen Wirkstoffen verwendet, hat aber bei größeren, weniger dicht ladungsverteilten Ionen wie Actinium‑225 Probleme. Diese Metalle können mit der Zeit ausbrechen, was Bedenken hinsichtlich der langfristigen Sicherheit aufwirft und die Verbreitung der zielgerichteten Alphatherapie einschränkt.
Ein hybrider Käfig für größere Atome
Der neue Chelator 3p‑C‑DEPA kombiniert Merkmale zweier etablierter Konstruktionen: das starre, ringförmige Gerüst von DOTA und die flexiblere, offenere Struktur eines anderen Chelators namens DTPA. Diese hybride Architektur verleiht 3p‑C‑DEPA zehn starke Bindungs„hände“ (Stickstoff‑ und Sauerstoffatome) gegenüber DOTAs acht und eine geräumigere Höhlung, die große Metallionen besser aufnehmen kann. Frühere Laborarbeiten deuteten darauf hin, dass 3p‑C‑DEPA Antikörper schnell bei milden Temperaturen markieren kann und Bismut‑basierte Radionuklide in Blutserum stabil hält. Die vorliegende Studie geht einen Schritt weiter und verwendet quantenmechanische Rechnungen, um systematisch zu vergleichen, wie gut 3p‑C‑DEPA und DOTA Lutetium‑177, Bismut‑213 und Actinium‑225 binden.
Einblick in den molekularen Händedruck
Da die direkte Arbeit mit kurzlebigen Alphastrahlern schwierig ist, nutzten die Forschenden die Dichtheitsfunktionaltheorie (DFT), eine leistungsfähige computergestützte Methode, die abschätzt, wie Elektronen in Molekülen verteilt sind und wie stark Atome einander anziehen. Sie modellierten jedes Metallion in Wasser, dann dessen Komplex mit entweder DOTA oder 3p‑C‑DEPA, und berechneten die freie Energieänderung, wenn das Metall vom Wasser in den Chelator‑Käfig übergeht. Diese Energieänderung wird in eine „Stabilitätskonstante“ übersetzt: Je höher der Wert, desto fester hält der Chelator das Metall. Zwei unterschiedliche DFT‑Ansätze und zwei Solvatationsmodelle wurden verwendet, um realistische Lösungsbedingungen nachzuahmen und sicherzustellen, dass die Trends robust sind und keine Artefakte eines einzelnen Rechenaufbaus darstellen.
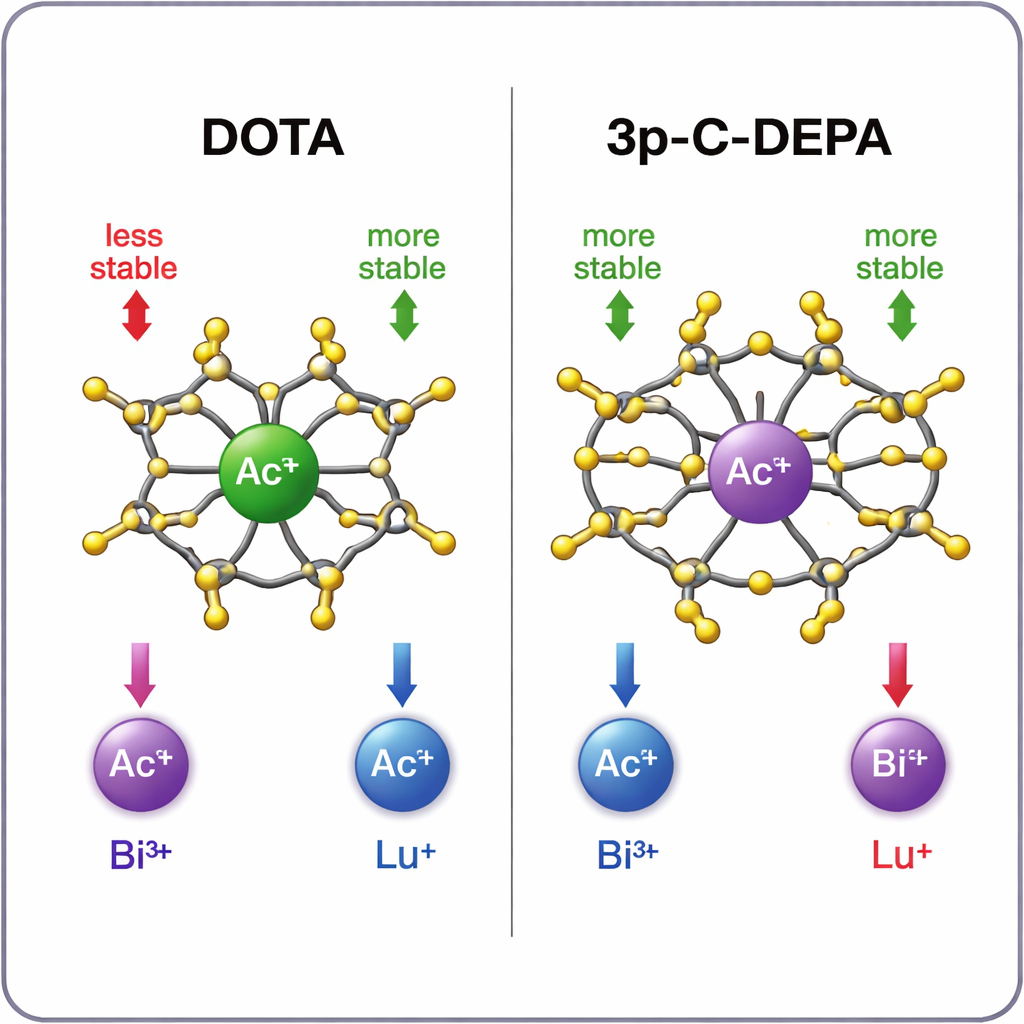
Welcher Käfig hält welches Metall am besten?
Die Simulationen zeigen ein klares Muster. Für das große Actinium‑Ion bildet 3p‑C‑DEPA einen deutlich stabileren Komplex als DOTA, was seiner größeren Höhlung und der größeren Anzahl an Sauerstoffdonoren zu verdanken ist, die das Metall greifen können. Auch Bismut‑213 wird von 3p‑C‑DEPA gut aufgenommen und profitiert sowohl von seiner Größe als auch von seiner elektronischen Aufnahmebereitschaft, die zu den elektronendonierenden Gruppen des Chelators passt. Im Gegensatz dazu passt das kleinere Lutetium‑177 besser in DOTAs dichtere, achthändige Umgebung. In 3p‑C‑DEPA führen überschüssige Donorgruppen um das kleine Ion herum zu abstoßenden Wechselwirkungen, die offenbar das Markieren verlangsamen und den Endkomplex leicht schwächen. Die berechneten Stabilitätstrends stimmen gut mit verfügbaren experimentellen Daten und Radiomarkierungserträgen überein, was den theoretischen Vorhersagen Glaubwürdigkeit verleiht.
Was das für künftige Krebstherapien bedeutet
Einfach gesagt legt die Studie nahe, dass DOTA kein Universalkäfig ist: Er funktioniert sehr gut für kleinere Metalle wie Lutetium, ist aber für voluminösere Alphastrahler wie Actinium‑225 suboptimal. 3p‑C‑DEPA hingegen verhält sich wie ein maßgeschneiderter Halter für diese größeren Ionen, greift sie fester und unter schonenderen Bedingungen, die empfindlichen Zielmolekülen wie Antikörpern entgegenkommen. Obwohl weitere experimentelle und klinische Arbeiten nötig sind, deuten die Berechnungen darauf hin, dass 3p‑C‑DEPA ein vielversprechendes Rückgrat für sicherere, effektivere zielgerichtete Alphatherapien sein könnte — und damit potenziell den Zugang zu sehr wirksamen Krebsbehandlungen erweitert, die Tumoren gezielt zerstören und gesundes Gewebe schonen.
Zitation: Ramdhani, D., Watabe, H., Ahenkorah, S. et al. DFT calculation of Ac3+ and Bi3+ complexation with hybrid chelator 3p-C-DEPA for targeted alpha therapy. Sci Rep 16, 6587 (2026). https://doi.org/10.1038/s41598-026-35633-z
Schlüsselwörter: zielgerichtete Alphatherapie, Radiopharmaka, Chelator‑Design, Actinium‑225, Dichtheitsfunktionaltheorie