Clear Sky Science · de
Experimentelle Untersuchung und thermodynamische Korrelation der Löslichkeit von Chlordiazepoxid in überkritischem CO₂
Warum es wichtig ist, ein bekanntes Medikament auf neue Weise aufzulösen
Viele moderne Arzneimittel wirken gut, lassen sich aber nur schwer effizient formulieren: Sie lösen sich möglicherweise nicht leicht, bauen sich während der Herstellung ab oder erfordern große Mengen organischer Lösungsmittel. Diese Studie beschäftigt sich mit Chlordiazepoxid, einem langjährig eingesetzten Medikament gegen Angststörungen, und stellt eine praktische Frage mit weitreichender Bedeutung: Wie gut löst es sich in überkritischem Kohlendioxid, einem saubereren, einstellbaren Lösungsmittel, das helfen könnte, sicherere und wirkungsvollere Arzneimittelpartikel herzustellen?
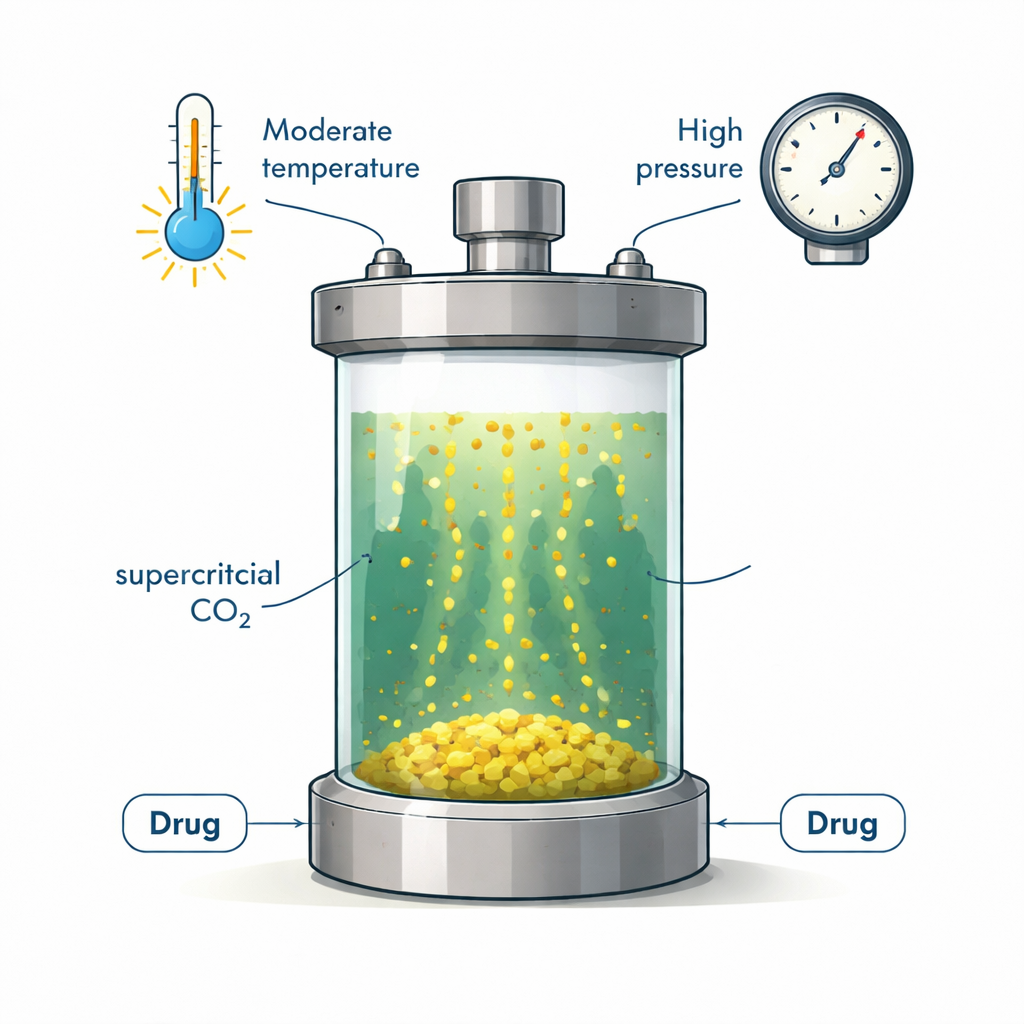
Ein grünes Fluid, das sich wie Gas und Flüssigkeit verhält
Überkritisches Kohlendioxid entsteht, wenn CO₂ über einen bestimmten Druck und eine bestimmte Temperatur hinausgebracht wird, sodass es weder ein typisches Gas noch eine normale Flüssigkeit ist. In diesem Zustand strömt es wie ein Gas, hat aber eine flüssigkeitsähnliche Dichte, die viele Substanzen lösen kann. Die Industrie nutzt es bereits zum Entkoffeinieren von Kaffee und zum Extrahieren von Aromen und Ölen. Für die Pharmazie ist überkritisches CO₂ attraktiv, weil es ungiftig ist, von Aufsichtsbehörden akzeptiert wird, kostengünstig und leicht zu recyceln ist. Es kann helfen, winzige, gleichförmige Arzneimittelpartikel zu erzeugen und den Einsatz harscher organischer Lösungsmittel zu reduzieren — sofern, und nur sofern, sich das Arzneimittel tatsächlich in ausreichendem Maße darin löst.
Messungen, wie sich ein Angstmedikament unter Druck verhält
Die Autoren wollten zum ersten Mal messen, wie viel Chlordiazepoxid sich in reinem überkritischem CO₂ innerhalb eines praktisch relevanten Verarbeitungsbereichs löst. Sie brachten festes Arzneipulver in einer Hochdruckzelle unter und leiteten CO₂ bei Drücken zwischen 12 und 30 Megapascal und Temperaturen zwischen 308 und 338 Kelvin (etwa 35–65 °C) hindurch. Nachdem das System das Gleichgewicht erreicht hatte, entnahmen sie die CO₂‑Phase, dehnten sie schnell in ein Lösungsmittel aus und bestimmten mittels UV‑sichtbarer Absorption, wie viel Wirkstoff gelöst war. Die Gesamtlöslichkeit lag im Bereich von etwa 20 bis 576 Teilen pro Million, entsprechend Molbruchteilen zwischen 0,0198×10⁻³ und 0,576×10⁻³ — Werte, die mit vielen anderen mäßig löslichen Arzneistoffen in überkritischem CO₂ übereinstimmen.
Wie Druck und Temperatur die Löslichkeit prägen
Die Messungen zeigten klare, einleuchtende Muster. Bei konstanter Temperatur erhöhte eine Drucksteigerung stets die Löslichkeit. Höherer Druck bringt CO₂‑Moleküle näher zusammen, macht die überkritische Phase dichter und besser darin, Arzneimittelmoleküle zu umgeben und zu transportieren. Die Temperatur hatte einen subtileren Effekt. Bei niedrigeren Drücken führte Erwärmung tendenziell zu geringerer Löslichkeit, weil das CO₂ verdünnt wurde und seine Lösungskraft abnahm. Oberhalb eines Umschlagdrucks von rund 19 Megapascal kehrte sich der Trend um: Höhere Temperatur erhöhte die Löslichkeit, weil sie die Tendenz des Wirkstoffs verstärkte, aus dem festen Zustand in die Phase überzugehen. Dieses Gleichgewicht zwischen Fluiddichte und der eigenen Flüchtigkeit des Arzneimittels ist kennzeichnend für überkritische Systeme und wichtig für die Wahl praktischer Betriebsbedingungen.
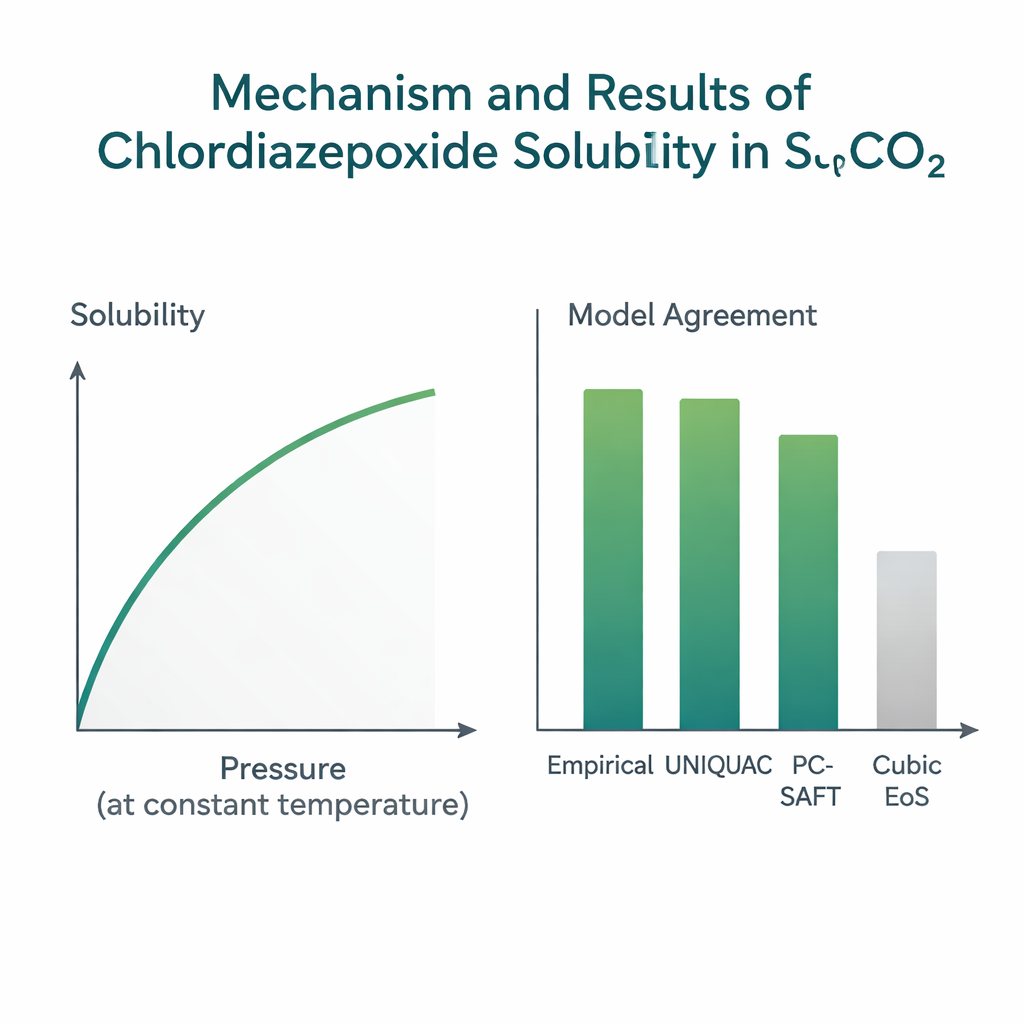
Modelle lehren, vorherzusagen, was das Labor zeigt
Da Hochdruckexperimente zeitaufwändig und teuer sind, verlassen sich Ingenieure auf mathematische Modelle, um die Löslichkeit unter neuen Bedingungen oder für verwandte Wirkstoffe vorherzusagen. Das Team prüfte mehrere Modellfamilien mit ihrem neuen Datensatz. Einfache, "dichtebasierte" empirische Formeln, die Löslichkeit direkt mit CO₂‑Dichte und Temperatur über nur wenige Anpassungsparameter verknüpfen, lieferten die besten Ergebnisse. Insbesondere die lang etablierte Chrastil‑Korrelation passte mit einer durchschnittlichen Abweichung von etwa 5 % sehr gut, und andere ähnliche Formeln schnitten ebenfalls gut ab. Ein physikalisch detaillierterer "expanded‑liquid"‑Ansatz namens UNIQUAC, der Molekülgröße, Form und Wechselwirkungsenergien berücksichtigt, erreichte vergleichbare Genauigkeit von rund 6 % Abweichung. Dagegen zeigten gebräuchliche kubische Zustandsgleichungen — allgemeine Formeln für das Verhalten von Fluiden — Abweichungen nahe 20 % und verfehlten feinere Details der spezifischen Wechselwirkung dieses Arzneistoffs mit CO₂.
Was das für die zukünftige Arzneimittelherstellung bedeutet
Kurz gesagt zeigt die Studie, dass sich Chlordiazepoxid unter technologisch relevanten Bedingungen in überkritischem CO₂ löst und dass sein Verhalten mit relativ einfachen, gut gewählten Modellen sehr gut erfasst werden kann. Das liefert eine verlässliche Karte zur Auslegung umweltfreundlicherer Prozesse zur Herstellung neuer Feststoffformen oder Nanopartikel des Wirkstoffs, was Stabilität oder Bioverfügbarkeit verbessern kann. Breiter betrachtet liefert die Arbeit einen seltenen, sorgfältig gemessenen Datensatz für ein weit verbreitetes Medikament und zeigt, welche Modellierungswerkzeuge beim Planen von überkritischen CO₂‑Prozessen am vertrauenswürdigsten sind — Informationen, die eine sauberere und effizientere Herstellung vieler anderer Arzneimittel unterstützen können.
Zitation: Saadati Ardestani, N., Noubigh, A., Esfandiari, N. et al. Experimental investigation and thermodynamic correlation of chlordiazepoxide solubility in supercritical CO₂. Sci Rep 16, 6552 (2026). https://doi.org/10.1038/s41598-026-35623-1
Schlüsselwörter: überkritisches Kohlendioxid, Arzneimittellöslichkeit, Chlordiazepoxid, grüne pharmazeutische Verarbeitung, thermodynamische Modellierung