Clear Sky Science · de
Ein Proteomik- und Redox-Proteomik-Ansatz zum Verständnis der Heterogenität von ARDS
Warum das für Intensivpatienten wichtig ist
Das akute Respiratorische Distress-Syndrom (ARDS) ist eine lebensbedrohliche Form des Lungenversagens, die bei Menschen mit schweren Infektionen, Traumata oder anderen kritischen Erkrankungen auftreten kann. Viele Patienten mit ARDS erscheinen am Krankenbett ähnlich, doch während sich einige erholen, versterben andere, und kein Medikament hat sich bislang als gezielte Therapie zur Umkehr des Syndroms bewährt. Diese Studie stellt eine einfache, aber bedeutende Frage: Wenn wir Proteine und chemische Reaktionen in Lunge und Blut von ARDS-Patienten genau untersuchen, lassen sich dann versteckte biologische "Typen" der Erkrankung finden, die erklären, warum Patienten so unterschiedlich verlaufen?
In die Lunge schauen, nicht nur in den Blutkreislauf
Um das zu untersuchen, begleiteten die Forschenden 16 Erwachsene auf einer Intensivstation mit ARDS, die beatmet wurden. Innerhalb der ersten drei Tage nach Diagnose entnahmen sie Blut und eine spezielle Probe, die bronchoalveoläre Lavage (BAL), eine schonende Spülung der Lungenbläschen. Wann immer möglich wiederholten sie die Probenentnahmen über mehrere Tage. Mit hochauflösender Massenspektrometrie bestimmten sie Hunderte von Proteinen in jeder Probe (Proteomik) und untersuchten entscheidend auch, in welchem Oxidationszustand einige dieser Proteine vorlagen (Redox-Proteomik). Das gibt Aufschluss darüber, wie stark sie durch reaktive Sauerstoffspezies – aggressive chemische Nebenprodukte der Entzündung – geschädigt oder reguliert sind.
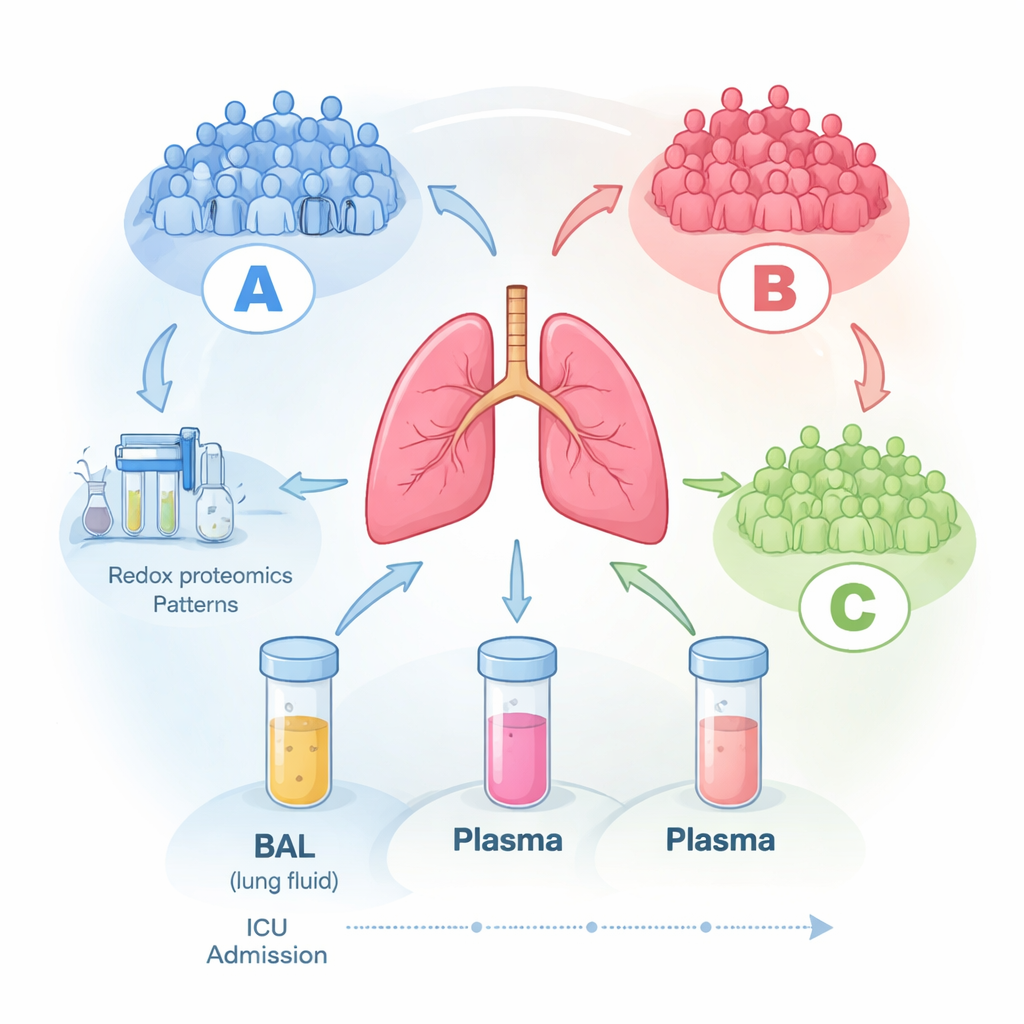
Drei versteckte Patientengruppen treten zutage
Als das Team die Daten ohne Vorgaben selbst gruppieren ließ, zeigte sich in den Proben aus der Lungenspülflüssigkeit ein klares Muster: drei unterschiedliche molekulare Gruppen, bezeichnet A, B und C. Patienten in Gruppe A waren bei Einschluss tendenziell schwerer erkrankt, während Gruppen B und C eine mildere Erkrankung aufwiesen. Auffällig war, dass diese molekularen Signaturen über einen Zeitraum von bis zu sechs Tagen auf der Intensivstation weitgehend stabil blieben, was darauf hindeutet, dass jeder Patient einem relativ konsistenten biologischen Muster folgt und nicht zufällig von Tag zu Tag wechselt. Übliche klinische Messgrößen – etwa Sauerstoffwerte, Aufenthaltsdauer oder allgemeine Schweregrad-Scores – korrespondierten nur schlecht mit diesen molekularen Gruppierungen. Das deutet darauf hin, dass die gängigen klinischen Werkzeuge wichtige Vorgänge in der Lunge übersehen.
Oxidativer Stress und körpereigene Abwehrmechanismen
Ein zentrales Thema in den Daten war das Gleichgewicht zwischen schädigenden reaktiven Sauerstoffspezies und den antioxidativen Abwehrsystemen des Körpers. In Gruppe A, der schwersten Gruppe, waren viele Lungenproteine, die an Energieproduktion und zellulären Aufräumprozessen beteiligt sind, in geringerer Menge vorhanden. Noch aussagekräftiger war, dass wichtige antioxidative Enzyme wie Peroxiredoxine, glutathionbezogene Proteine, Thioredoxin und Katalase deutlich vermindert waren. Im Gegensatz dazu wiesen Gruppen B und insbesondere C höhere Mengen dieser Schutzproteine auf, was darauf schließen lässt, dass ihre Lungen besser gerüstet waren, schädliche Oxidantien zu entgiften und Kollateralschäden durch Entzündung zu begrenzen. Unterschiede im Oxidationszustand von Proteinen legten eine weitere Ebene offen: verschiedene Untergruppen oxidierter Proteine waren in den schwersten und den mildesten Gruppen unterschiedlich stark vertreten.
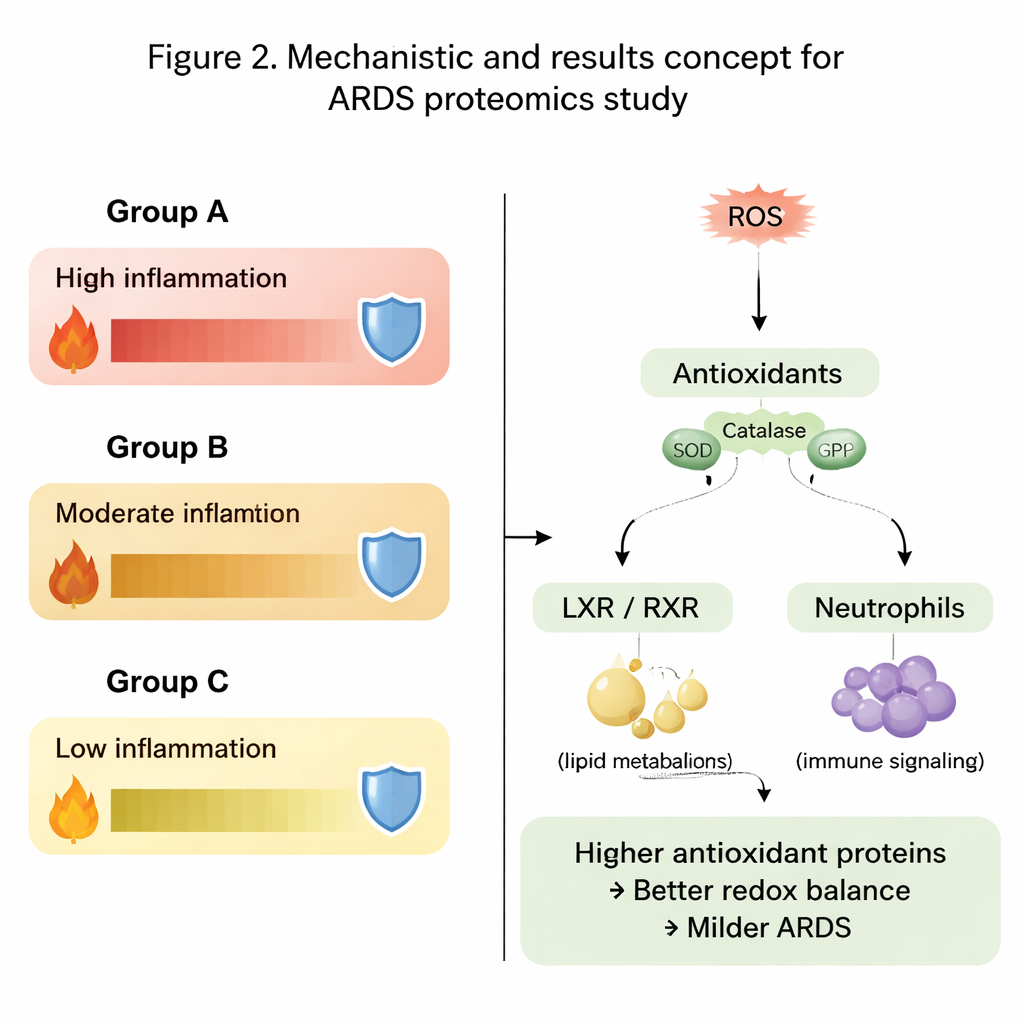
Signalwege, die die Entzündung formen
Über einzelne Proteine hinaus untersuchten die Autor*innen komplette biologische Signalwege. Sie stellten fest, dass Wege, die mit Entzündung, Cholesterin- und Fettstoffwechsel sowie der Aktivität von Immunzellen verknüpft sind, zwischen den drei Gruppen unterschiedlich agierten. Besonders auffällig waren Signale, die mit dem LXR/RXR-Signalweg (Liver X Receptor–Retinoid X Receptor) und dem Enzym DHCR24 zusammenhängen, die gemeinsam sowohl den Lipidstoffwechsel als auch Immunantworten regulieren. In der schwersten Gruppe wurden diese Wege als stärker aktiviert vorhergesagt, einhergehend mit reduzierter Signalgebung des Immunbotenstoffs Interleukin-12. Zugleich zeigten Wege, die reaktive Sauerstoffspezies, deren Entgiftung und Aktivität von Neutrophilen betreffen, kontrastierende Muster zwischen Lungenspülflüssigkeit und Blut, was unterstreicht, dass lokale Vorgänge in der Lunge vom Geschehen im Kreislauf abweichen können.
Was das für die künftige Versorgung bedeuten könnte
Diese kleine, explorative Studie verändert die Behandlung heute nicht; ihre Ergebnisse müssen in deutlich größeren Patientengruppen bestätigt werden. Sie zeigt jedoch, dass man durch detaillierte Profilierung von Proteinen und ihrem Redox-Zustand direkt in der Lungenspülflüssigkeit – statt sich nur auf Bluttests oder klinische Scores zu verlassen – biologisch sinnvolle Subtypen des ARDS unterscheiden kann. Diese Subtypen unterscheiden sich hinsichtlich oxidativem Stress, antioxidativer Kapazität, Stoffwechsel und Immun-Signalgebung und bleiben in den ersten kritischen Krankheitstagen relativ stabil. Zukünftig könnten solche molekularen Fingerabdrücke Ärzten helfen, ARDS-Patienten präziser zuzuordnen, gezielte Therapien entsprechend dem jeweiligen Muster auszuwählen und klügere klinische Studien zu entwerfen, die eine größere Chance haben, wirksame Behandlungen zu finden.
Zitation: Forshaw, T.E., Shukla, K., Wu, H. et al. A proteomics and redox proteomics approach to understanding ARDS heterogeneity. Sci Rep 16, 6034 (2026). https://doi.org/10.1038/s41598-026-35606-2
Schlüsselwörter: akutes Respiratorisches Distress-Syndrom, Proteomik, oxidativer Stress, bronchoalveoläre Lavage, Intensivmedizin