Clear Sky Science · de
Immunoassays zum Nachweis und zur Differenzierung von Paenibacillus larvae, dem Erreger der Amerikanischen Faulbrut (AFB) bei Honigbienen
Warum die Brutkrankheit der Bienen uns alle betrifft
Honigbienen leisten weit mehr als nur die Honigproduktion. Durch die Bestäubung von Nutz- und Wildpflanzen sichern sie unsere Nahrungsmittelversorgung und erhalten das Funktionieren von Ökosystemen. Eine der zerstörerischsten Bedrohungen für Bienenvölker ist eine bakterielle Erkrankung der Jungen, die Amerikanische Faulbrut genannt wird. Hat sie sich in einem Volk ausgebreitet, kann sie eine gesamte Kolonie auslöschen und sich schnell auf Nachbarvölker ausbreiten. Diese Studie beschreibt neue Schnelltests, die das frühe Erkennen der Krankheit und die Bestimmung des beteiligten Bakterientyps erleichtern und Imkern sowie Tierärzten bessere Chancen geben, Ausbrüche zu stoppen, bevor sie außer Kontrolle geraten.
Eine tödliche Kinderkrankheit der Bienen
Die Amerikanische Faulbrut trifft die Larven der Honigbiene, die heranwachsende Brut, aus der Arbeiterinnen und Königinnen werden. Der Erreger ist ein sporenbildendes Bakterium, Paenibacillus larvae. Seine Sporen können jahrelang in altem Wabenwerk und getrockneten Larvenresten überdauern, und schon wenige verschluckte Sporen reichen aus, um eine junge Larve zu infizieren. Sobald sich die Bakterien vermehren, fällt die Larve zu einer klebrigen Masse zusammen, die später zu einer dunklen Kruste austrocknet und dicht an der Zelle haftet. Diese Krusten sind mit Millionen von Sporen gefüllt und fungieren als langlebige Infektionsreservoire, die von Sammelbienen und Imkern unabsichtlich zwischen Völkern und Standorten verbreitet werden können.
Zwei Varianten desselben Killers
Nicht alle P.-larvae-Stämme sind auf die gleiche Weise gefährlich. Weltweit sind zwei Hauptgenotypen, bekannt als ERIC I und ERIC II, für nahezu alle aktuellen Ausbrüche verantwortlich. Beide sind tödlich, nutzen jedoch unterschiedliche Mechanismen, um die Larvengut-Barriere zu überwinden und in den Körper einzudringen. Alle virulenten Stämme sezernieren ein starkes chitinabbauendes Enzym namens PlCBP49, das ihnen hilft, die schützende Auskleidung des Darms aufzubrechen. ERIC-I-Stämme produzieren zusätzlich klassische Toxine, die Darmschleimhautzellen direkt schädigen, während ERIC-II-Stämme stattdessen auf ein Oberflächenprotein namens SplA setzen, das ihnen beim Anhaften hilft und anschließend die Darmbarriere auf einem noch nicht vollständig geklärten Weg zerstört. Da sich ERIC I und ERIC II in der Geschwindigkeit, mit der sie Larven töten, und im Verlauf eines Ausbruchs unterscheiden, kann die Kenntnis des vorliegenden Typs Einfluss auf Bekämpfungsmaßnahmen haben.
Bakterielle Waffen als diagnostische Zielmoleküle nutzen
Die Autorinnen und Autoren erkannten, dass sich diese Virulenzfaktoren – PlCBP49 und SplA – als hochspezifische Marker eignen könnten. Würde ein Test PlCBP49 nachweisen, würde er eine Infektion durch jeden gefährlichen P.-larvae-Stamm anzeigen. Würde er zusätzlich SplA erkennen, würde das spezifisch auf den ERIC-II-Typ hinweisen. Zu diesem Zweck stellten die Forschenden gereinigte Versionen beider Proteine her und nutzten sie, um monoklonale Antikörper zu erzeugen: im Labor hergestellte Proteine, die nur an ein einzelnes Molekül binden. Diese Antikörper wurden sorgfältig mittels Dot‑Blot und Western‑Blot gegen mehrere ERIC-I- und ERIC-II-Stämme sowie gegen mehr als 20 andere in Honig und Wabengewebe häufig vorkommende Bakterienarten getestet. Ein Antikörper gegen PlCBP49 und einer gegen SplA erwiesen sich als besonders selektiv, da sie alle relevanten P.-larvae‑Stämme erkannten, aber ähnlich aussehende Bakterien aus der Bienenumgebung ignorierten.
Von Laborplatten zum Teststreifen am Bienenstock
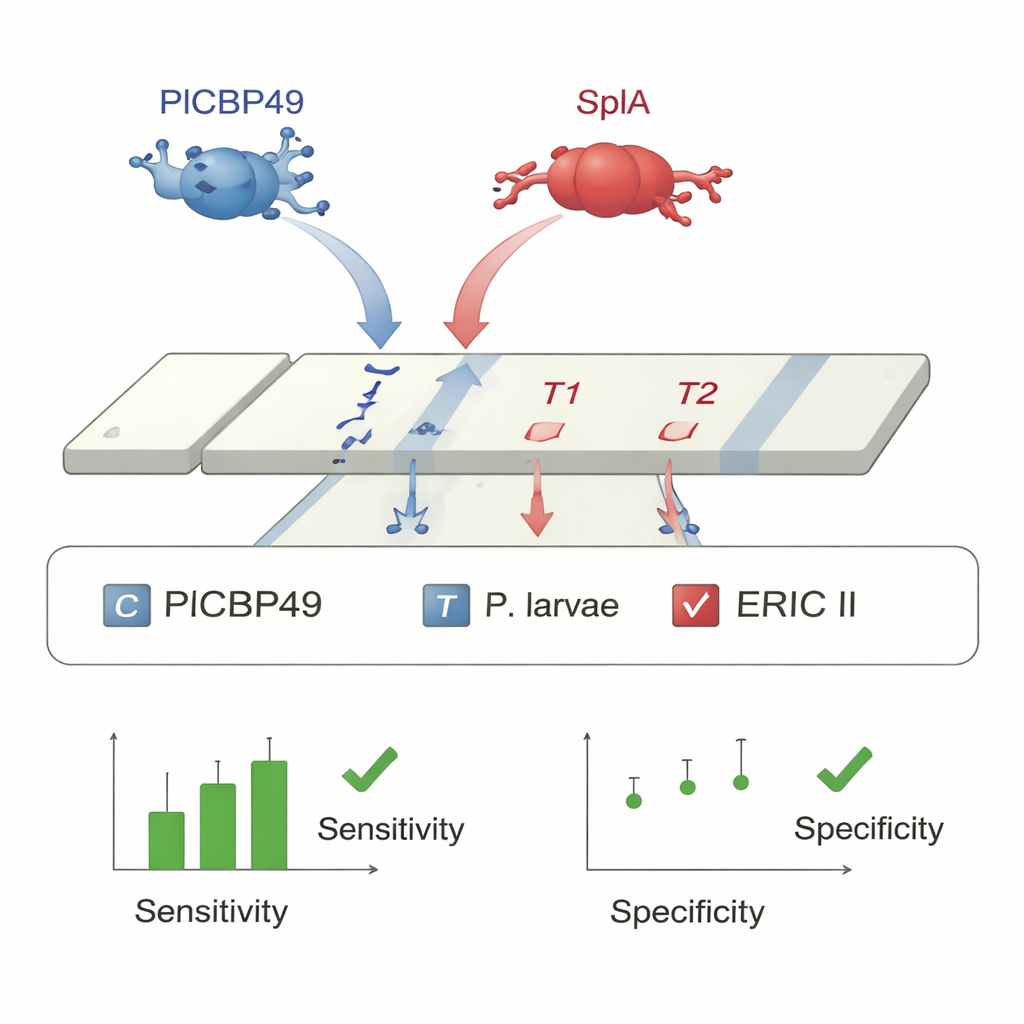
Mit geeigneten Antikörpern entwickelten die Forschenden zwei laborbasierte Sandwich‑ELISA‑Kits und einen streifenförmigen Lateral‑Flow‑Assay, ähnlich dem Konzept eines Schwangerschafts- oder COVID‑19‑Heimtests. In den ELISAs fängt ein Antikörper das Zielprotein aus einer homogenisierten Larve ein, und ein zweiter markierter Antikörper macht dessen Anwesenheit als Farbumschlag in einer Kunststoff‑Mikroplatte sichtbar. Tests an experimentell infizierten Larven zeigten, dass der PlCBP49‑ELISA 89 % der infizierten Individuen mit keinen falsch positiven Ergebnissen nachweisen konnte, während der SplA‑ELISA 94 % der ERIC‑II‑infizierten Larven detektierte und ERIC II mit 97 % Genauigkeit von ERIC I unterschied. Auf Grundlage derselben Antikörperpaare entwarf das Team einen duplexen Lateral‑Flow‑Streifen mit zwei Testlinien: eine für PlCBP49 (alle P. larvae) und eine für SplA (nur ERIC II). Als Larvenproben aus Laborinfektionen und realen Ausbrüchen über die Streifen getestet wurden, identifizierte der Test P. larvae in 95–99 % der infizierten Larven korrekt und zeigte eine Spezifität von 96–100 %, wobei etwa 9 von 10 Genotypbestimmungen (ERIC I versus ERIC II) richtig klassifiziert wurden.
Was das für Bienen und Imker bedeutet
Heute erfordert die Bestätigung der Amerikanischen Faulbrut oft das Einschicken verdächtiger Waben oder Larven an ein spezialisiertes Labor zur Kultur oder DNA‑Analyse, ein Prozess, der Tage bis Wochen dauern kann, während sich die Krankheit weiter ausbreitet. Die neuen ELISA‑Kits bieten Laboren eine schnellere, automationsfähige Möglichkeit, viele Proben zu sichten, während der duplexe Lateral‑Flow‑Streifen direkt am Bienenstock als Point‑of‑Care‑Test eingesetzt werden kann. Ein Imker oder Inspektor kann einige verdächtige Larven entnehmen, den Test in Minuten durchführen und nicht nur feststellen, ob P. larvae vorhanden ist, sondern auch, ob der schneller wirkende ERIC‑II‑Typ beteiligt ist. Diese Kombination aus Geschwindigkeit, Genauigkeit und Einsatzfähigkeit vor Ort kann die Bekämpfung der Faulbrut grundlegend verändern: Früherer Nachweis ermöglicht frühere Eingriffe, weniger verlorene Völker und besseren Schutz der Bestäubungsleistungen, von denen Landwirtschaft und natürliche Ökosysteme abhängen.
Zitation: Reinecke, A., Göbel, J. & Genersch, E. Immunoassays for the detection and differentiation of Paenibacillus larvae, the etiological agent of American foulbrood (AFB) in honey bees. Sci Rep 16, 2635 (2026). https://doi.org/10.1038/s41598-026-35590-7
Schlüsselwörter: Bienenkrankheit, Amerikanische Faulbrut, Paenibacillus larvae, schneller Diagnosetest, Lateral-Flow-Assay