Clear Sky Science · de
Antikörper-funktionalisierte Gold-Nanosphären für multimodale Bildgebung
Scharfere Sicht auf verborgene Tumore
Die Früherkennung von Krebs hängt oft davon ab, wie klar Ärztinnen und Ärzte das Geschehen im Körper sehen können. Diese Studie stellt winzige goldbasierte Partikel vor, die Tumore auf mehreren Wegen zugleich zum Leuchten bringen und so sowohl eine präzise Karte der Lage eines Kopf‑ und Hals‑Tumors liefern als auch Hinweise auf das Verhalten des Gewebes. Die Arbeit weist den Weg zu künftigen Untersuchungen und Operationen, die schneller, genauer und weniger anfällig dafür sind, gefährliche Zellen zu übersehen.
Warum bessere Bildgebung wichtig ist
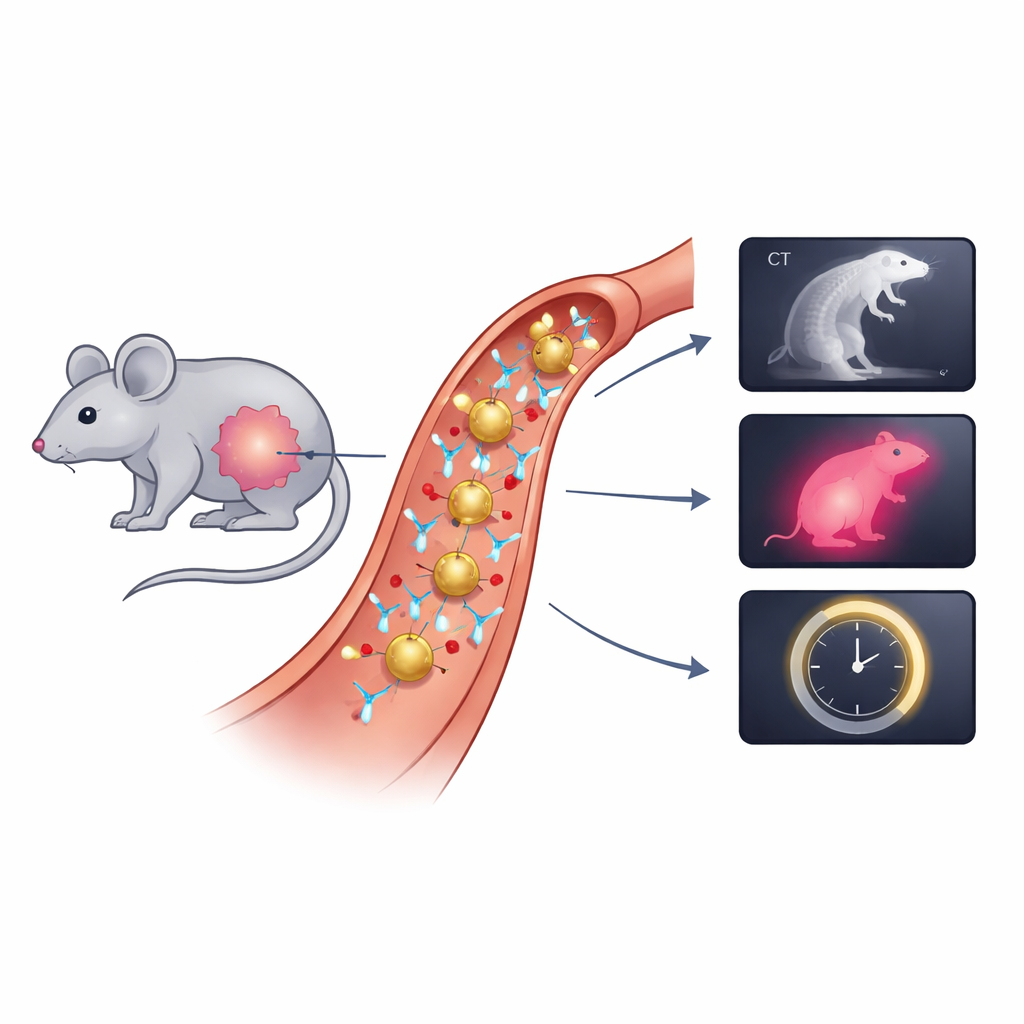
Kopf‑ und Halskrebserkrankungen entstehen in Bereichen wie Mund, Rachen und Kehlkopf, wo Operationen abwägen müssen, wie das gesamte Tumorgewebe entfernt werden kann, ohne Sprache und Schlucken unnötig zu beeinträchtigen. Chirurgen verlassen sich zunehmend auf fluoreszierende Farbstoffe, die Tumore unter speziellen Kameras zum Glühen bringen und so helfen, die tatsächlichen Ränder einer Masse nachzuzeichnen. Viele nahinfrarote Farbstoffe, die bevorzugt werden, weil sie tiefer ins Gewebe vordringen und weniger Hintergrundstörung zeigen, leuchten jedoch im Körper zu schwach. Computertomographie (CT) liefert dagegen scharfe anatomische Bilder, sagt aber wenig über die Biologie des Tumors aus. Die Autorinnen und Autoren wollten diese Lücke mit einem einzigen Werkzeug überbrücken, das sowohl für CT als auch für fortgeschrittene lichtbasierte Bildgebung nutzbar ist.
Entwurf eines winzigen goldenen Leuchtfeuers
Das Team baute ein „Gold‑Nanodye“, ausgehend von sehr kleinen Goldkugeln von etwa 25 Nanometern Durchmesser – tausendfach dünner als ein menschliches Haar. Sie überzogen das Gold mit flexiblen Polymerkettchen, um die Partikel im Blut stabil zu halten, und setzten dann zwei zentrale Komponenten auf: einen weitverbreiteten nahinfraroten Farbstoff (IRDye 800) und Antikörper, die ein Protein namens EGFR erkennen, das auf Kopf‑ und Halskrebszellen häufig in hoher Konzentration vorkommt. Dieses kombinierte Partikel, Anti‑AuND genannt, soll über die Antikörper gezielt Tumore ansteuern, die Helligkeit des Farbstoffs durch Wechselwirkungen mit der Goldoberfläche verstärken und Röntgenstrahlen stark abschwächen, sodass es auch im CT sichtbar ist. Labortests bestätigten, dass die Partikel die erwartete Größe, Ladung und Struktur aufwiesen und von Krebszellen gut aufgenommen wurden.
Wie sich die Partikel bei Mäusen verhalten
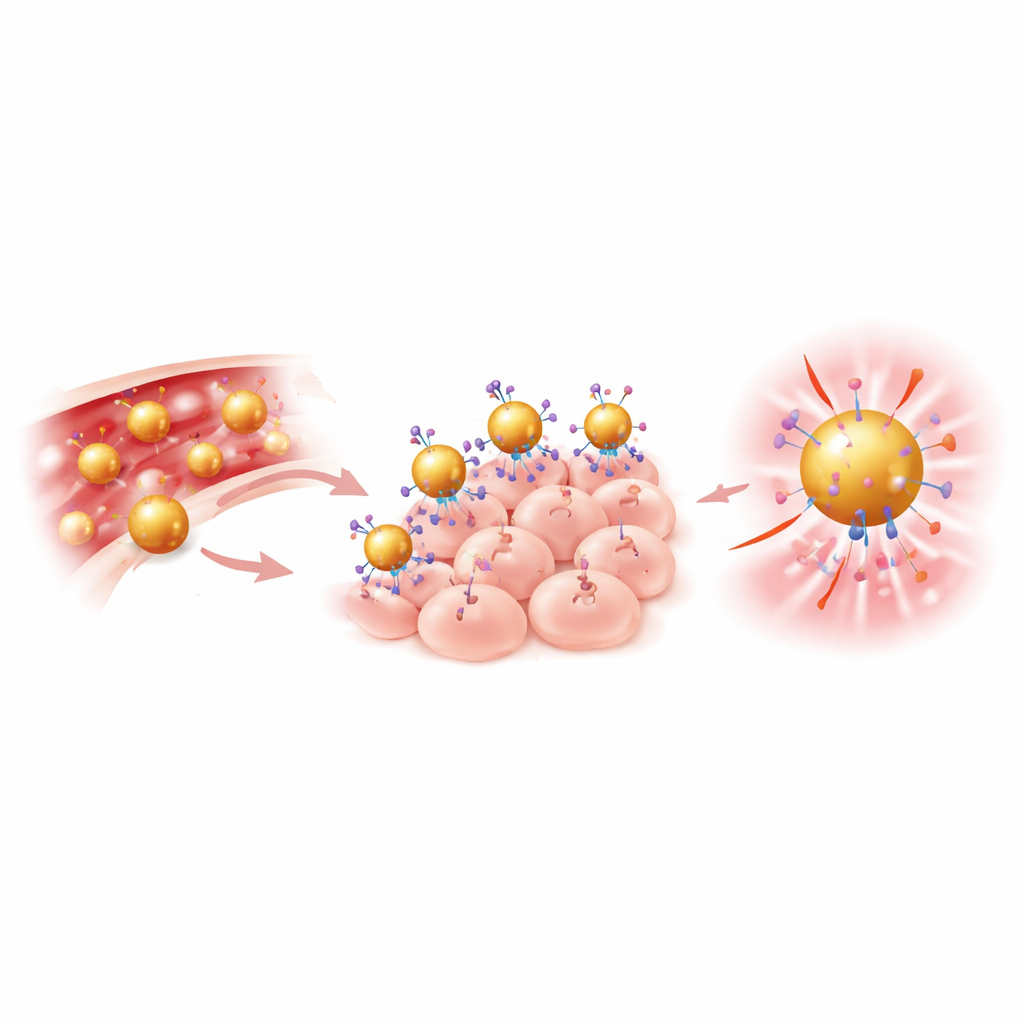
Um die neuen Sonden in lebenden Systemen zu testen, setzten die Forschenden humane Kopf‑ und Halskrebszellen unter die Haut von Mäusen ein. Nachdem die Tumore gewachsen waren, erhielten die Tiere Anti‑AuND über eine Vene. Mit hochauflösender Mikro‑CT sah das Team deutlich stärkere Signale in den Tumoren der mit zielgerichteten Goldpartikeln behandelten Mäuse als bei unbehandelten Tieren, was zeigt, dass aktives Targeting passive Anreicherung übertraf. Anschließend nutzten sie nahinfrarote Kameras, um zu prüfen, wie hell die Tumore leuchteten. Im Vergleich zum freien Farbstoff allein erzeugte Anti‑AuND etwa zehnmal höhere Fluoreszenz, schuf einen klaren Kontrast zwischen Tumor und gesundem Gewebe und zeichnete die Tumorränder auf der Hautoberfläche scharf nach.
Eine neue Dimension durch Lebensdauer‑Signale
Über die Helligkeit hinaus maßen die Forschenden, wie lange der Farbstoff nach der Anregung im angeregten Zustand verbleibt — eine Eigenschaft, die als Fluoreszenzlebensdauer bezeichnet wird. Diese Lebensdauer ist empfindlich gegenüber der Umgebung, etwa lokalen Ionenwerten, Proteinen und Sauerstoff. Die Anti‑AuND‑Partikel zeigten eine moderate Lebensdaueränderung, wenn sie an Gold gebunden waren, aber einen deutlich größeren Anstieg, wenn sie sich im Tumorgewebe gegenüber normalem Mausgewebe befanden. Diese Verschiebung deutet darauf hin, dass die Lebensdauerbildgebung nicht nur offenbart, wo sich die Partikel befinden, sondern auch, dass sie in einer tumorähnlichen Umgebung lokalisiert sind, und liefert damit Informationen, die weniger von der Farbstoffkonzentration abhängen und stärker an die Tumorchemie gebunden sind.
Was das für die künftige Versorgung bedeuten könnte
Zusammen liefern CT‑, Fluoreszenz‑Intensitäts‑ und Lebensdauer‑Messungen ein reichhaltigeres Bild von Kopf‑ und Hals‑Tumoren als jede einzelne Bildgebungsmethode für sich. Das Gold‑Nanodye fungiert als doppelt nutzbares Leuchtfeuer, das nahinfrarote Signale aufhellt, zugleich als starker CT‑Kontrastmitteldarsteller dient und als empfindliche Sonde für das Tumormikromilieu fungiert. Obwohl weitere Arbeiten nötig sind, um Langzeitsicherheit und Ausscheidung zu verfolgen, könnte dieser multimodale Ansatz letztlich Ärztinnen und Ärzten helfen, kleinere Tumore früher zu entdecken, Chirurgen zu saubereren Schnitträndern zu verhelfen und mit demselben injizierten Wirkstoff zu überwachen, wie Tumore auf Therapien ansprechen.
Zitation: Chacko, N., Motiei, M., Rotbaum, R. et al. Antibody-functionalized gold nanospheres for multimodal imaging. Sci Rep 16, 8608 (2026). https://doi.org/10.1038/s41598-026-35561-y
Schlüsselwörter: Goldnanopartikel, nahinfrarote Bildgebung, Kopf- und Halskrebs, Fluoreszenzlebensdauer, multimodale Bildgebung