Clear Sky Science · de
Bevacizumab erhöht das Gesamtüberleben bei neu diagnostizierten Glioblastom-Patienten mit hoher COX-2-Expression
Warum diese Studie zu Hirntumoren wichtig ist
Das Glioblastom gehört zu den tödlichsten Hirntumoren; selbst mit Operation, Bestrahlung und Chemotherapie überleben die meisten Patientinnen und Patienten weniger als zwei Jahre. Ein Medikament namens Bevacizumab kann Tumoren verkleinern und Hirnschwellungen lindern, doch große Studien deuteten darauf hin, dass es im Durchschnitt nicht die Lebenszeit verlängert. Diese Studie stellt eine präzisere Frage: Kann ein einfacher Labortest am Tumor eine Untergruppe von Patientinnen und Patienten identifizieren, die durch Bevacizumab tatsächlich länger leben?
Ein genauerer Blick auf einen hartnäckigen Hirntumor
Glioblastome wachsen schnell und sind dicht mit abnormalen Blutgefäßen durchzogen, die den Tumor versorgen. Die Standardbehandlung, oft als Stupp-Protokoll bezeichnet, kombiniert eine Operation zur maximalen Tumorresektion mit anschließender Bestrahlung und dem oralen Chemotherapeutikum Temozolomid. Bevacizumab ist ein Antikörper, der ein Wachstumsignal blockiert, das für die Bildung neuer Blutgefäße genutzt wird. Es ist in vielen Ländern für rezidivierende Glioblastome zugelassen und kann in Japan auch von Beginn an eingesetzt werden. Da frühere große Studien jedoch zeigten, dass die Zugabe von Bevacizumab zur Erstbehandlung das Gesamtüberleben der durchschnittlichen Patientenschaft nicht verlängerte, waren Ärztinnen und Ärzte unsicher, wann oder ob es frühzeitig eingesetzt werden sollte.
Ein möglicher „Schalter“, der aggressivere Tumoren kennzeichnet
Die Forschenden konzentrierten sich auf ein Molekül namens COX-2, ein Enzym, das an Entzündungsprozessen beteiligt ist und Krebszellen außerdem beim Aufbau neuer Blutgefäße, bei der Ausbreitung und bei der Resistenz gegen Medikamente hilft. Hohe COX-2-Werte im Glioblastom werden seit langem mit schlechterem Überleben in Verbindung gebracht und gelten damit als Marker einer besonders aggressiven Erkrankung. Das Team fragte sich, ob diese schnell wachsenden, stark vaskularisierten Tumoren möglicherweise am ehesten von einem anti-angiogenen Medikament wie Bevacizumab profitieren. Um das zu prüfen, untersuchten sie Tumorproben von 50 erwachsenen, neu diagnostizierten Glioblastom-Patientinnen und -Patienten, die zwischen 2012 und 2023 an einem einzigen japanischen Krankenhaus behandelt wurden. Alle erhielten die Standardbehandlung aus Operation, Bestrahlung und Temozolomid; einige bekamen zusätzlich von Anfang an Bevacizumab.
Aufteilung der Patientinnen und Patienten anhand eines Tumor-Labortests
Pathologinnen und Pathologen bestimmten COX-2 in jedem Tumor mittels einer Färbemethode unter dem Mikroskop und vergaben einen „Immunreaktivitäts‑Score“ basierend auf der Färbeintensität und dem Anteil positiver Zellen. Unter Verwendung des Medians als Grenzwert wurden Tumoren entweder als „hohe COX-2“ oder „niedrige COX-2“ klassifiziert. In einer Teilmenge der Proben bestimmten sie zudem die COX-2-Genaktivität und fanden, dass Tumoren mit starker Färbung generell auch höhere Genaktivität aufwiesen, was die Zuverlässigkeit des Tests stützte. Die Patientengruppen wurden anschließend nach COX-2-Level und danach, ob sie nur Temozolomid oder Temozolomid plus Bevacizumab erhalten hatten, eingeteilt; verglichen wurden das Zeitintervall bis zum Tumorrezidiv und das Gesamtüberleben.
Wer profitiert wirklich von Bevacizumab?
Betrachtete man alle 50 Patientinnen und Patienten zusammengenommen, verzögerte die Zugabe von Bevacizumab zwar das Tumorwachstum, verlängerte aber nicht eindeutig das Leben – ein Ergebnis, das frühere große Studien widerspiegelt. Das Bild änderte sich jedoch deutlich, als die Patienten nach COX-2-Level getrennt wurden. Unter denen mit hoher COX-2-Expression lebten die mit Bevacizumab behandelten Patientinnen und Patienten median 25 Monate, verglichen mit 18 Monaten bei denen ohne Bevacizumab, und auch die Zeit bis zur Krankheitsprogression war länger. Statistische Modelle, die Alter, funktionellen Status und das Ausmaß der Tumorentfernung berücksichtigten, zeigten weiterhin, dass Bevacizumab in dieser Hoch‑COX‑2‑Gruppe unabhängig mit besseren Ergebnissen assoziiert war. Im Gegensatz dazu brachte die Zugabe von Bevacizumab bei Patientinnen und Patienten mit niedriger COX-2-Expression weder eine Verbesserung der Zeit bis zum Rezidiv noch des Gesamtüberlebens.
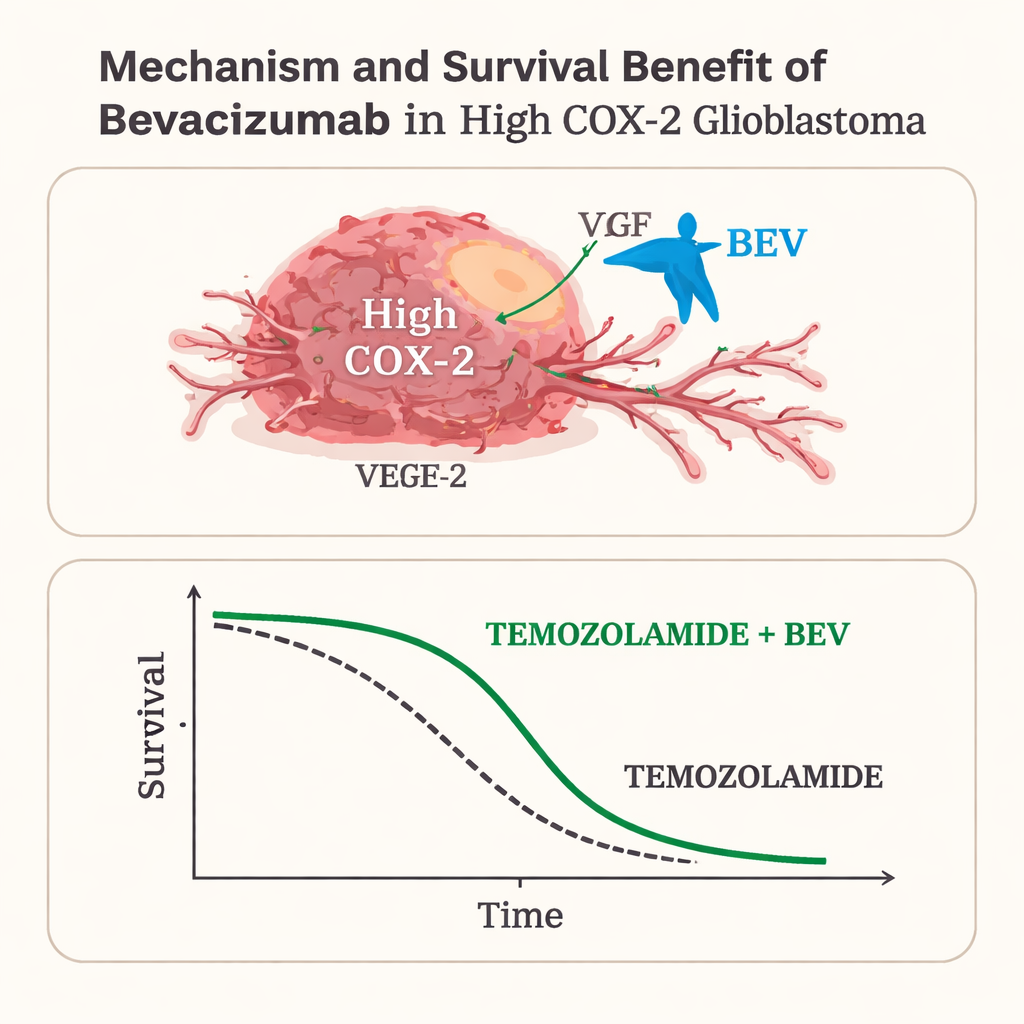
Was das für Patientinnen, Patienten und Gesundheitssysteme bedeutet
Für Patientinnen und Patienten mit hoher COX-2-Expression schien Bevacizumab den Überlebensnachteil, der üblicherweise mit dieser aggressiven Tumorbiologie einhergeht, auszugleichen und ihre Lebenserwartung der von Personen mit niedriger COX-2-Expression anzugleichen. Für jene mit niedriger COX-2 brachte das Medikament dagegen Kosten und mögliche Nebenwirkungen ohne klaren Nutzen. Da es sich um eine relativ kleine, retrospektive Studie eines einzelnen Zentrums handelt, müssen die Ergebnisse in größeren, prospektiven Studien bestätigt werden. Dennoch deutet die Arbeit darauf hin, dass ein unkomplizierter Labortest am Tumorgewebe Ärztinnen und Ärzten helfen könnte, Bevacizumab gezielt denjenigen Patientinnen und Patienten anzubieten, die am ehesten profitieren, und andere vor einer teuren und belastenden Behandlung zu bewahren, die ihr Leben möglicherweise nicht verlängert.
Zitation: Kesumayadi, I., Kambe, A., Kanda, H. et al. Bevacizumab enhances overall survival in newly diagnosed glioblastoma patients with high COX-2 expression. Sci Rep 16, 4974 (2026). https://doi.org/10.1038/s41598-026-35550-1
Schlüsselwörter: Glioblastom, Bevacizumab, COX-2, Behandlung von Hirntumoren, personalisierte Medizin