Clear Sky Science · de
Co3O4-Nadeln auf Graphenoxid als effizienter Elektrokatalysator für hybride Wasserelektrolyse durch alternative anodische Oxidationsreaktionen
Aus Fruchtabfall wird Treibstoff der Zukunft
Wasserstoff gilt oft als sauberer Kraftstoff der Zukunft, aber seine Herstellung erfordert meist sehr viel Strom. Diese Studie zeigt, wie etwas Alltägliches wie weggeworfene Orangenschalen das ändern kann. Indem die Forscher diesen Abfall in ein spezielles Kohlenstoffmaterial umwandeln und mit einer cobaltbasierten Verbindung kombinieren, erzeugten sie einen kostengünstigen Katalysator, der Wasserstoff mit deutlich weniger Energieaufwand herstellen kann als konventionelle Wasserspaltung. Gleichzeitig ersetzen sie einen ineffizienten Schritt der Wasserelektrolyse durch schonendere Reaktionen, die problematische Chemikalien in harmlose Gase umwandeln.
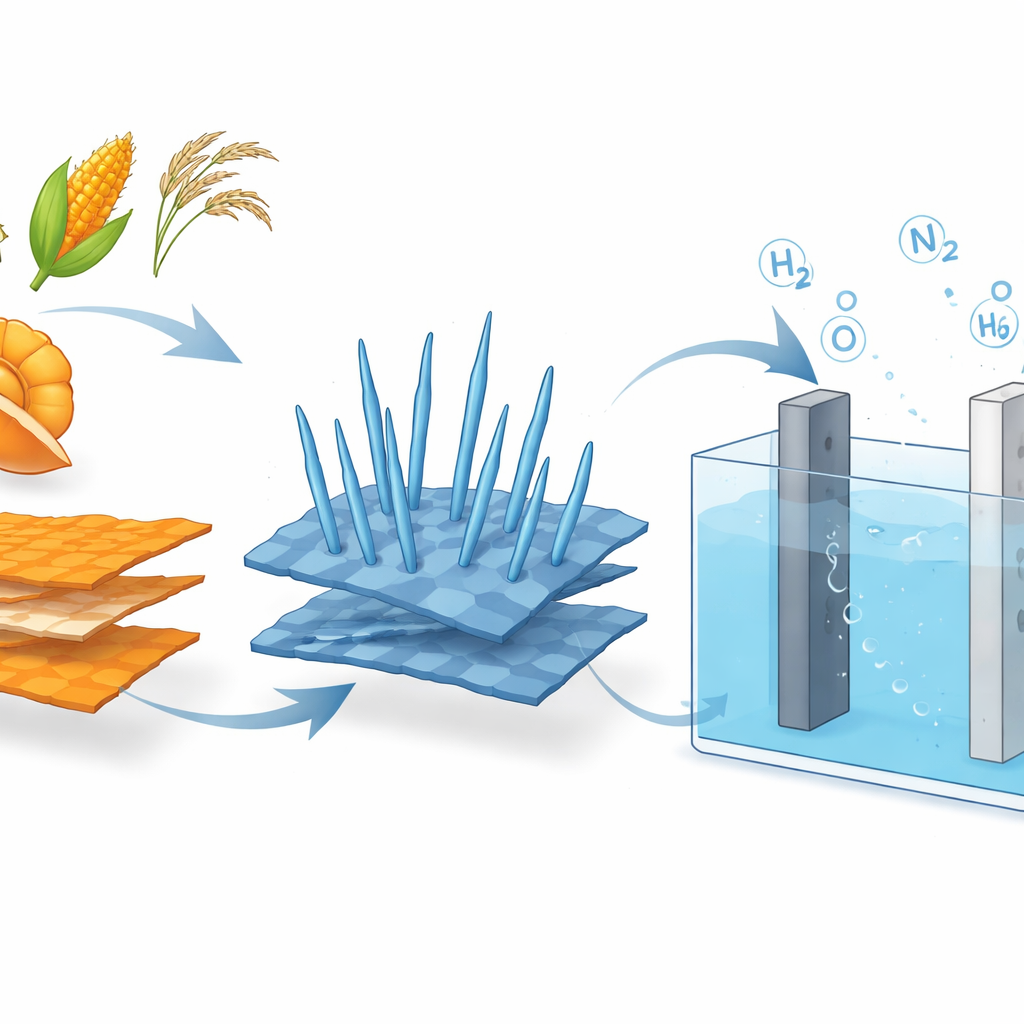
Warum traditionelle Wasserspaltung Energie verschwendet
Um Wasser in Wasserstoff und Sauerstoff zu spalten, leitet ein Elektrolyseur Strom durch Wasser, dem ein gelöstes Salz oder eine Lauge beigemischt ist. An einer Elektrode bildet sich Wasserstoff relativ leicht. An der anderen Elektrode wird Sauerstoff erzeugt — eine langsame und energieintensive Reaktion, weil dabei vier Elektronen in mehreren wohlabgestimmten Schritten bewegt werden müssen. Dieser sauerstoffbildende Schritt, die anodische Reaktion, zwingt die Ingenieure dazu, die Spannung zu erhöhen, was die Energiekosten in die Höhe treibt. Schlimmer noch: Der entstehende Sauerstoff wird oft einfach abgeführt und nicht weiter genutzt, sodass ein großer Teil der zugeführten elektrischen Energie wenig praktischen Nutzen liefert.
Einen Energiefresser gegen schonendere Reaktionen austauschen
Das Team ging dieses Nadelöhr an, indem es das Geschehen an der energieaufwendigen Seite der Zelle neu konzipierte. Statt aus Wasser Sauerstoff zu erzeugen, fragten sie: Was wäre, wenn das System andere, leichter zu handhabende Chemikalien oxidiert, während am gegenüberliegenden Pol weiterhin Wasserstoff entsteht? Sie wählten zwei stickstoffreiche Verbindungen, Harnstoff und Hydrazin, die in Abwässern und industriellen Prozessen häufig vorkommen. Wenn diese Moleküle in alkalischer Lösung oxidiert werden, zerfallen sie zu Stickstoffgas, Wasser und im Fall von Harnstoff zu Kohlendioxid. Entscheidend ist, dass diese Reaktionen bei deutlich geringeren Spannungen beginnen als die Sauerstoffbildung, sodass bei gleicher Wasserstoffmenge weit weniger elektrische Energie benötigt wird.
Von Orangenschalen zu intelligenten Elektroden
Um diesen Ansatz praktisch umzusetzen, benötigten die Forscher einen Katalysator, der billig, robust und aktiv für drei verschiedene Aufgaben ist: klassische Sauerstoffbildung, Harnstoffoxidation und Hydrazinoxidation. Sie begannen damit, getrocknete Orangenschalen in Graphenoxid umzuwandeln — ein dünnes, leitfähiges Kohlenstoffmaterial — durch ein einfaches Erhitzungsverfahren statt durch aggressive chemische Behandlungen. Auf diesen Blättern züchteten sie in einem Druckgefäß winzige „Nanoneedles“ aus Cobaltoxid. Das resultierende Hybridmaterial — Cobaltoxid-Nadeln auf Graphenoxid — bildet eine raue, schwammartige Oberfläche mit vielen freiliegenden Reaktionsstellen und einem leicht zugänglichen Elektronenweg. Messungen zeigten, dass die Graphenunterlage verhindert, dass Cobaltpartikel verklumpen, und die effektive Oberfläche sowie die elektrische Leitfähigkeit deutlich erhöht.
Wie der neue Katalysator die Stromrechnung senkt
In alkalischer Lösung getestet erreichte Elektrode bei einem standardisierten Stromdichte-Benchmark deutlich niedrigere Spannungen als reines Cobaltoxid. Für die herkömmliche Sauerstoffbildung war die Leistung vergleichbar mit einigen kommerziellen Edelmetallkatalysatoren. Sobald Harnstoff zugesetzt wurde, sank die benötigte Spannung weiter, und bei Hydrazin war die Verbesserung auffällig: Die Elektrode benötigte nur einen sehr kleinen zusätzlichen Antrieb über das natürliche Referenzpotenzial, um denselben Strom aufrechtzuerhalten. In einer vollständigen Zwei-Elektroden-Zelle, gekoppelt mit einer üblichen platinbasierten Wasserstoffbildungselektrode, erzeugte die Hydrazin-unterstützte Elektrolyse Wasserstoff bereits bei nur 0,33 Volt — etwa 1,3 Volt weniger als die traditionelle Wasserspaltung unter den gleichen Bedingungen. Das System blieb zudem über viele Stunden stabil, wobei Struktur und Zusammensetzung des Katalysators praktisch unverändert blieben.
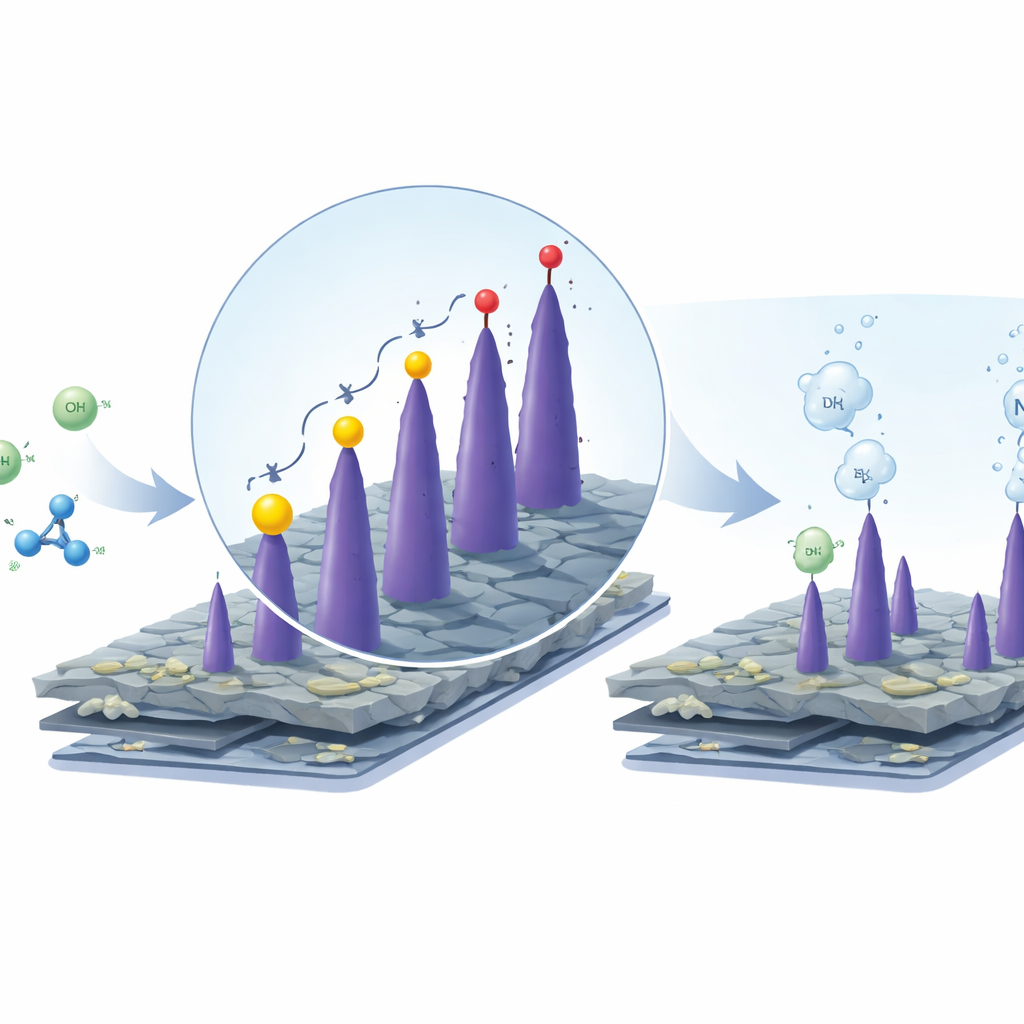
Was das für sauberen Wasserstoff bedeutet
Für den nicht spezialisierten Leser ist die Botschaft klar: Indem sowohl das Elektrodenmaterial als auch die an ihm ablaufende Reaktion neu gedacht werden, zeigen die Forscher, dass Wasserstoff mit deutlich weniger Strom und aus preisgünstigen Zutaten hergestellt werden kann. Fruchtabfälle werden zu leistungsfähigen Kohlenstoffgerüsten; Cobaltoxid-Nanoneedles liefern die aktiven Stellen; und der Ersatz der Sauerstoffbildung durch die Oxidation von Harnstoff oder Hydrazin senkt die benötigte Spannung drastisch. Im Fall von Hydrazin sind die Nebenprodukte hauptsächlich Stickstoff und Wasser, wodurch zusätzliche CO2-Emissionen vermieden werden. Zwar ist weitere Arbeit nötig, um chemische Versorgung und Sicherheit im großtechnischen Maßstab zu gewährleisten, doch diese hybride Elektrolyse-Strategie weist den Weg zu saubererem, günstigerem Wasserstoff, der zugleich Abfallströme und erneuerbare Biomasse aufwertet.
Zitation: Rahamathulla, N., Murthy, A.P. Co3O4 nanoneedles grown on graphene oxide as an efficient electrocatalyst for hybrid water electrolysis through alternative anodic oxidation reactions. Sci Rep 16, 8452 (2026). https://doi.org/10.1038/s41598-026-35522-5
Schlüsselwörter: Wasserstoffproduktion, Wasserelektrolyse, Graphenoxid, Hydrazinoxidation, Katalysatoren aus Biomasse