Clear Sky Science · de
Vergleichende Genomik von kolistin‑nicht‑empfindlichen multiresistenten Pseudomonas aeruginosa zeigt neu auftretende Liniensysteme in Thailand
Warum dieses Krankenhauskeim für alle wichtig ist
Pseudomonas aeruginosa ist ein Krankenhauskeim, der Menschen in ihrer verwundbarsten Phase befällt – nach Operationen, an Beatmungsgeräten oder bei schweren Verbrennungen oder Lungenerkrankungen. Seit Jahren verlassen sich Ärztinnen und Ärzte auf ein starkes „letztes Mittel“, das Antibiotikum Kolistin, wenn andere Wirkstoffe versagen. Diese Studie untersucht Stämme von Pseudomonas aus Krankenhäusern in ganz Thailand, die nicht mehr auf Kolistin oder viele andere Antibiotika ansprechen. Durch das vollständige Auslesen der DNA dieser Bakterien zeigen die Forschenden, wie neue, stark medikamentenresistente Liniensysteme sich ausbreiten und warum das Patienten, Klinikerinnen und Gesundheitssysteme weltweit beunruhigen sollte.
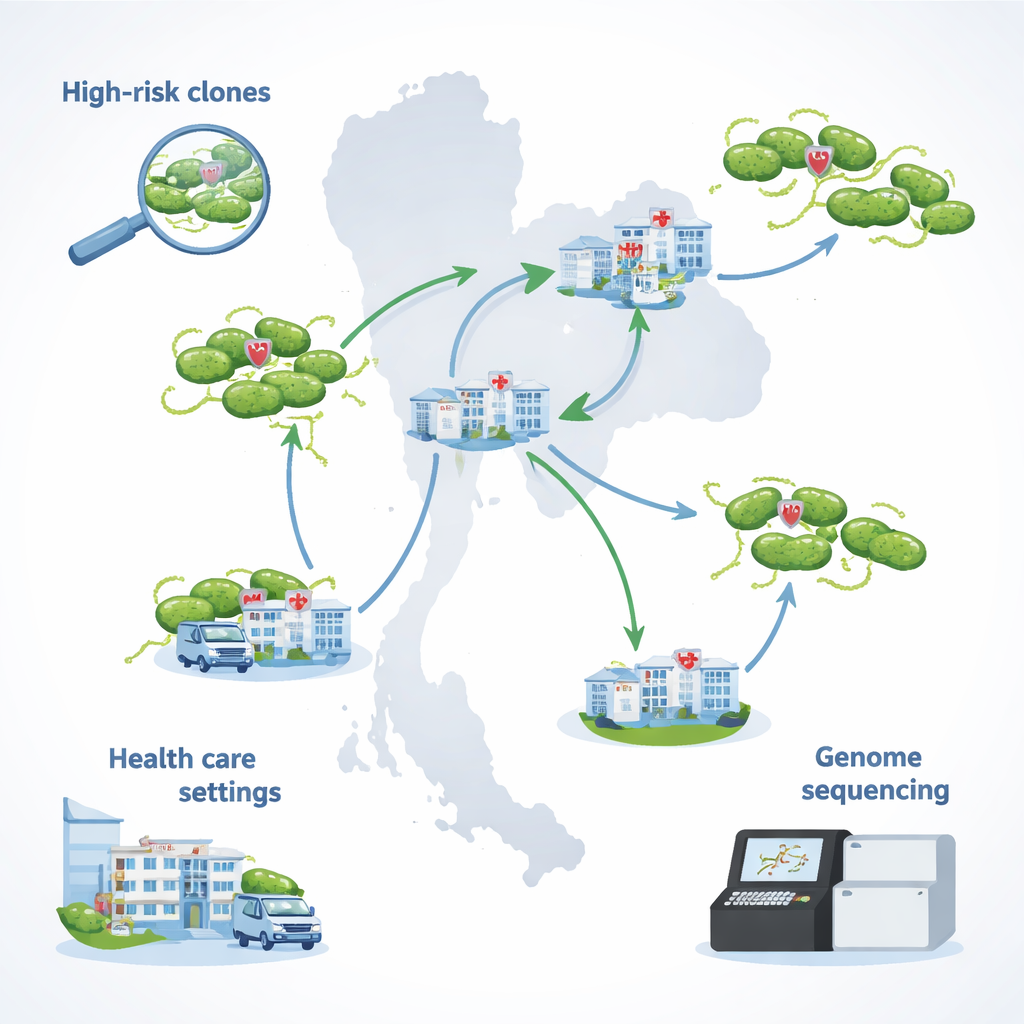
Ein schwer zu behandelnder Erreger in ganz Thailand verfolgen
Das Team konzentrierte sich auf 29 Stämme von Pseudomonas aeruginosa, die 2021–2022 in Krankenhäusern gesammelt wurden, die am nationalen Überwachungsprogramm für Antibiotikaresistenzen in Thailand teilnehmen. Alle diese Stämme waren multiresistent: Sie widerstanden mehreren wichtigen Antibiotikaklassen, einschließlich Wirkstoffen, die üblicherweise bei schweren Infektionen eingesetzt werden. Entscheidend ist, dass sie auch nicht vollständig gegenüber Kolistin empfindlich waren, dem Medikament, das oft für lebensbedrohliche Fälle zurückgehalten wird. Die meisten Proben stammten aus Urin, andere kamen aus Blut, Sputum, Eiter und Operationsdrainagen – ein Spiegel der vielfältigen Infektionstypen, die dieser Keim bei hospitalisierten Patientinnen und Patienten verursachen kann.
Die genetischen „Fingerabdrücke“ der Bakterien lesen
Mithilfe einer Kombination aus Kurz‑ und Langlese‑DNA‑Sequenzierung stellten die Forschenden für jeden Stamm hochwertige Genome zusammen. Anschließend verglichen sie diese Genome, um die Bakterien in genetische Familien einzuordnen, sogenannte Sequenztypen. Neun verschiedene Sequenztypen wurden entdeckt, was auf eine erhebliche Diversität hinweist. Einer davon, bezeichnet als ST5340, wurde zuvor noch nicht beschrieben. Er erwies sich als nah verwandt mit einem bekannten internationalen Hochrisiko‑Klon namens ST357 und unterschied sich in nur einem von sieben standardmäßig betrachteten Hauskeeping‑Genen. Trotz dieser engen Verwandtschaft fiel ST5340 dadurch auf, dass alle seine Isolate gegen alle getesteten Antibiotika resistent waren, was ihn als besonders besorgniserregende Linie kennzeichnet.
Aufkommende Hochrisiko‑Linien und ihre Ausbreitung
Indem sie winzige DNA‑Unterschiede, sogenannte Einzel‑Nukleotid‑Polymorphismen, über 108 thailändische Pseudomonas‑Genome (die 29 neuen plus 79 aus öffentlichen Datenbanken) hinweg ausrichteten, bauten die Forschenden einen Stammbaum der im Land zirkulierenden Stämme. Diese Analyse hob mehrere dominante Cluster hervor, die um ST5340, ST357, ST654 und ST235 zentriert waren – Linien, die bereits als oder nun zunehmend als „Hochrisiko“ gelten, weil sie häufig multidrug‑resistent sind und Krankenhausausbrüche verursachen. ST5340 trat dabei in mehreren Provinzen und Regionen auf, was darauf hindeutet, dass er sich weit verbreitet und nicht auf ein einzelnes Krankenhaus beschränkt ist. Auch andere global bedeutsame Klone wie ST654 und ST235 waren vorhanden, während einige weltweit wichtige Linien wie ST244 fehlten, vermutlich weil die Studie nur kolistin‑nicht‑empfindliche Stämme einschloss.
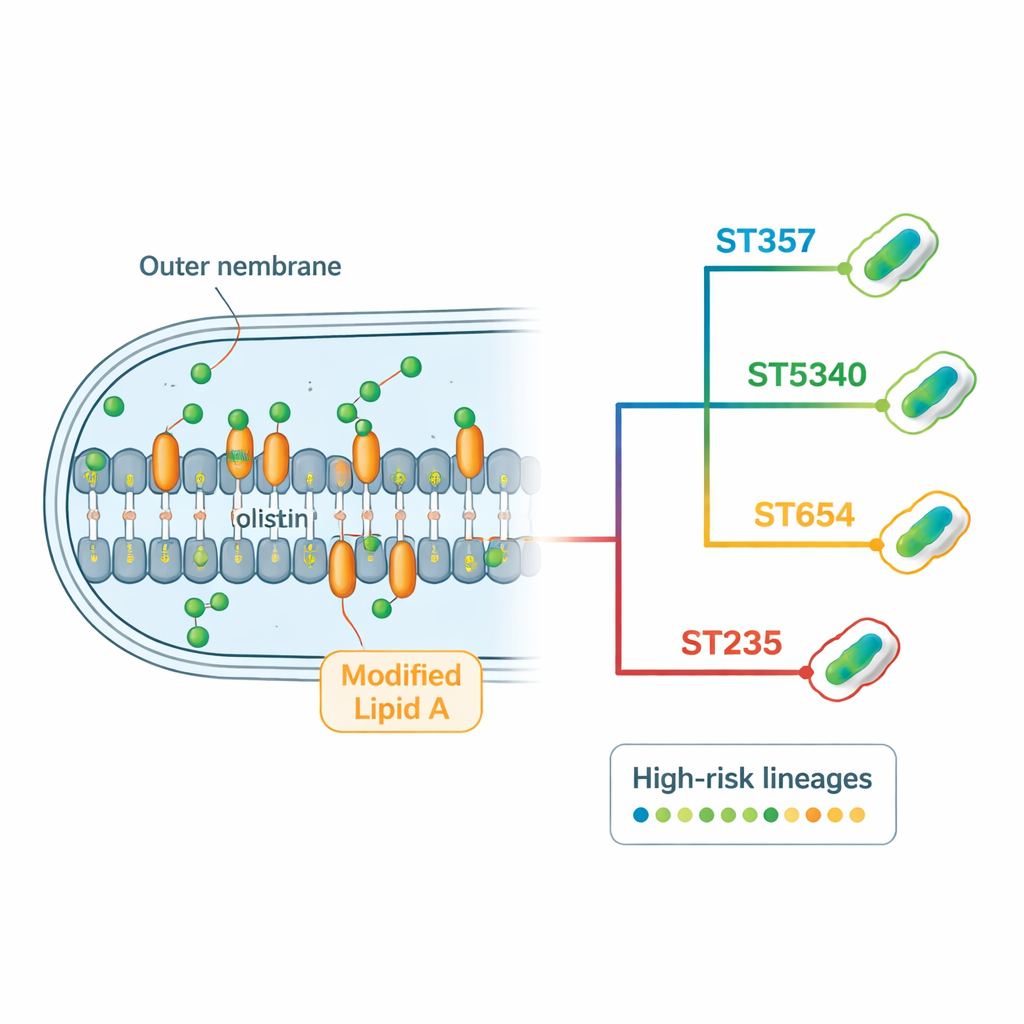
Wie diese Bakterien Antibiotika überlisten
Die genomische Analyse machte ein umfangreiches „Resistom“ sichtbar – das vollständige Set an Resistenzgenen und Mutationen, die jeder Stamm trägt. Viele Isolate kodierten mehrere Arten von Beta‑Laktamasen, Enzymen, die gängige Antibiotika wie Penicilline, Cephalosporine und Carbapeneme zerstören. Das Carbapenemase‑Gen blaNDM‑1, das mit Resistenz gegen einige der stärksten Klinikmedikamente assoziiert ist, tauchte in nahezu allen Stämmen auf, teilweise in mehrfacher Kopie. Die Bakterien trugen außerdem Gene, die Aminoglykosid‑Antibiotika chemisch modifizieren, sowie leistungsfähige Efflux‑Pumpen, die wie molekulare Pumpen Wirkstoffe aus der Zelle herausbefördern. Für Kolistin fanden die Forschenden keine mobil übertragbaren Resistenzgene, sondern wiederkehrende Veränderungen in chromosomalen Genen, die an der äußeren Zellmembran und deren Regulation beteiligt sind. Bestimmte Mutationen in Regulationsproteinen und in Enzymen zum Aufbau von Lipid A standen in starker Verbindung mit Kolistinresistenz, besonders in den dominanten Liniensystemen ST357 und ST5340.
Was das für Patientinnen, Patienten und Krankenhäuser bedeutet
Durch die Kombination nationaler Überwachung mit moderner Genomsequenzierung zeigt diese Studie, dass thailändische Krankenhäuser einer wachsenden Bedrohung durch einen neu erkannten Hochrisiko‑Klon, ST5340, neben etablierten globalen Problemstämmen gegenüberstehen. Diese Bakterien sind nicht nur gegenüber Kolistin resistent, sondern auch gegenüber vielen anderen wichtigen Wirkstoffen, was die Behandlungsmöglichkeiten bei schweren Infektionen drastisch einschränkt. Für Laien ist die Botschaft klar: Antibiotikaresistenz ist kein abstraktes Zukunftsrisiko, sondern eine gegenwärtige Realität, die den Ausgang von Operationen, Intensivbehandlungen und Krebstherapien direkt beeinflussen kann. Die Autorinnen und Autoren plädieren dafür, die genomische Überwachung fortzusetzen, die Infektionskontrolle zu verschärfen und Antibiotika sorgfältig einzusetzen, um zu verhindern, dass sich diese hochresistenten Liniensysteme noch weiter ausbreiten und schwerer zu kontrollieren werden.
Zitation: Wankaew, N., Arigul, T., Kruasuwan, W. et al. Comparative genomics of colistin-nonsusceptible multidrug-resistant Pseudomonas aeruginosa reveals emerging lineages in Thailand. Sci Rep 16, 5968 (2026). https://doi.org/10.1038/s41598-026-35520-7
Schlüsselwörter: Pseudomonas aeruginosa, antibiotikaresistenz, kolistin, genomische Überwachung, Krankenhausinfektionen