Clear Sky Science · de
Plasmatische exosomale hsa-miR-339-5p steht in Verbindung mit NOD-like receptor family CARD domain-containing 5 bei Herzinsuffizienz mit reduzierter Ejektionsfraktion
Warum winzige Moleküle im Blut auf ein geschwächtes Herz hinweisen können
Die Herzinsuffizienz mit reduzierter Ejektionsfraktion (HFrEF) ist ein häufiges Krankheitsbild, bei dem das Herz nicht mehr genügend Blut pumpt, um den Bedarf des Körpers zu decken. Ärztinnen und Ärzte erkennen sie meist erst, wenn bereits erheblicher Schaden entstanden ist. Diese Studie untersucht, ob mikroskopische Botschaften, die im Blut zirkulieren — kleine RNA‑Moleküle, verpackt in winzigen Bläschen namens Exosomen — frühzeitig auf Probleme hinweisen und Aufschluss darüber geben können, wie das Herz im Laufe der Zeit steifer wird und Narben bildet.
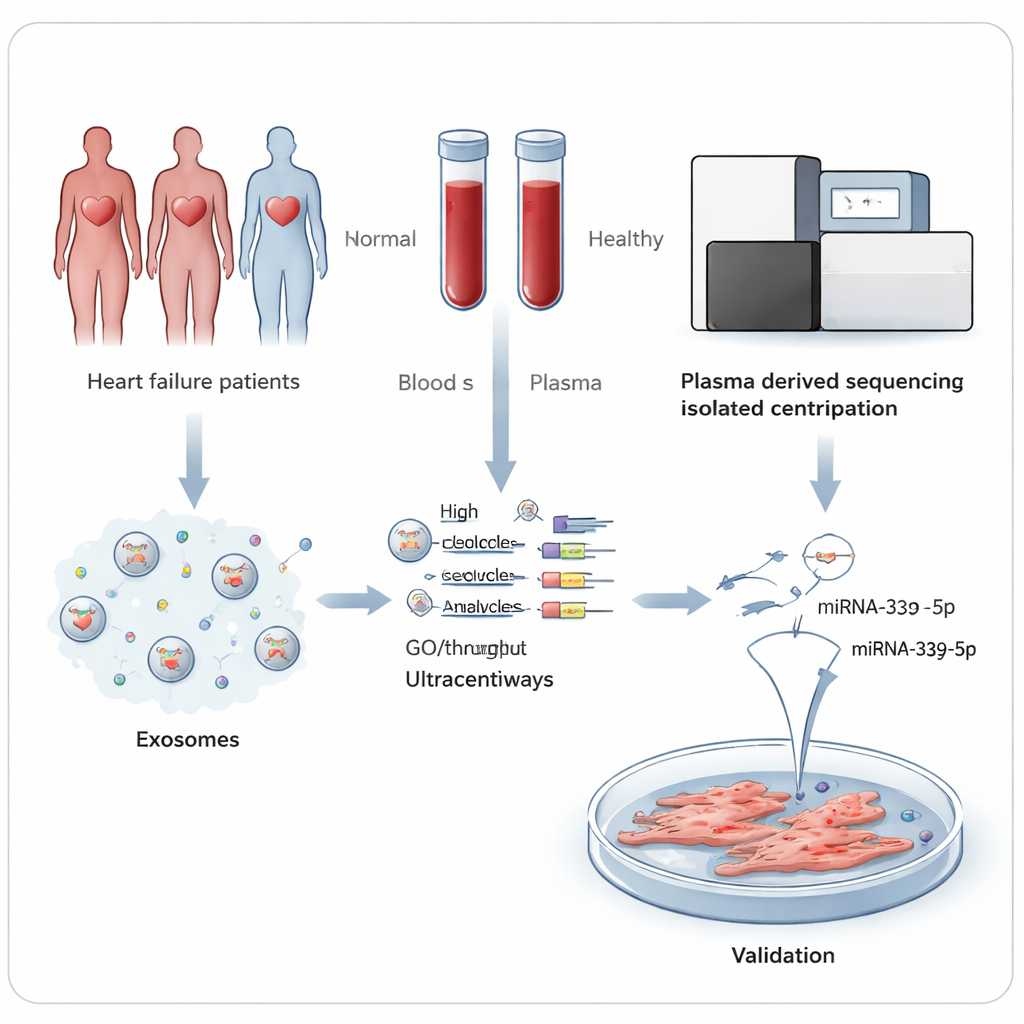
Versteckte Botschaften im Blutkreislauf
Unser Blut transportiert unzählige Exosomen, nanoskalige Säckchen, die von Zellen abgesondert werden und Proteine sowie genetisches Material zwischen Zellen transportieren. Zu ihrer Ladung gehören microRNAs, kurze Stränge, die fein steuern, welche Gene an- oder abgeschaltet werden. Da Exosomen diese microRNAs vor dem Abbau schützen, lassen sie sich in einer einfachen Blutprobe zuverlässig messen. Die Forscherinnen und Forscher vermuteten, dass das versagende Herz oder verwandte Gewebe eine andere Mischung an microRNAs freisetzen als ein gesundes Herz und dass diese Muster sowohl als Frühwarnzeichen dienen als auch Prozesse offenlegen könnten, die der Erkrankung zugrunde liegen.
Vergleich von Patienten mit geschwächtem Herzen und gesunden Freiwilligen
Das Team sammelte Blut von 45 Personen mit HFrEF und 45 vergleichbaren, aber gesunden Freiwilligen in einem Krankenhaus in Hefei, China. Aus dem Blutplasma isolierten sie sorgfältig Exosomen und bestätigten deren Größe und Form mittels Elektronenmikroskopie und Partikel‑Tracking‑Messungen. In einem ersten Schritt sequenzierten sie die kleinen RNAs in Exosomen aus einer Untergruppe von fünf Patienten und fünf Kontrollen. Dieser Hochdurchsatzansatz detektierte hunderte bekannte microRNAs und hob 27 hervor, die zwischen beiden Gruppen deutlich unterschiedlich vorkamen — 10 erhöht und 17 erniedrigt bei Personen mit Herzinsuffizienz.
Fokussierung auf ein herausragendes Signal
Um zu prüfen, welche dieser Veränderungen am verlässlichsten sind, verwendeten die Wissenschaftlerinnen und Wissenschaftler anschließend eine hochempfindliche PCR‑Methode, um sechs vielversprechende microRNAs in allen übrigen 40 Patienten und 40 Kontrollen zu messen. Mehrere Signale zeigten sich robust, doch ein einziges — hsa‑miR‑339‑5p — hob sich deutlich ab. Es war bei Patienten mit HFrEF konsequent erhöht und unterschied diese in der diagnostischen Analyse am besten von gesunden Personen. Computergestützte Pathway‑Analysen deuteten darauf hin, dass diese microRNA auf ein Gen namens NLRC5 einwirken könnte, das wiederum eine zentrale Wachstums‑ und Überlebensachse in der Zelle, den PI3K/Akt‑Signalweg, beeinflusst — ein Weg, der zuvor mit Herzhypertrophie und Vernarbung in Verbindung gebracht wurde.
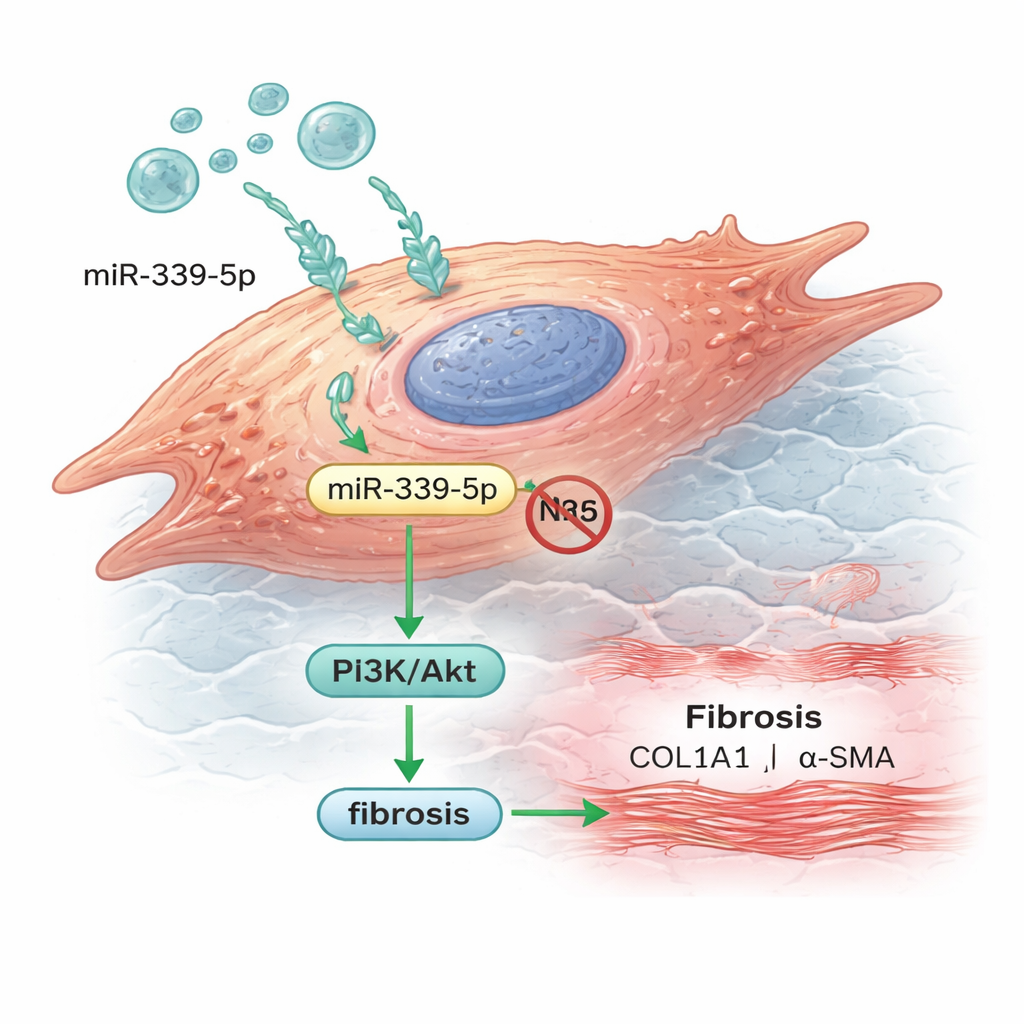
Vom Blutmarker zum Treiber der Vernarbung
Die Forscherinnen und Forscher gingen dann zu herzähnlichen Zellen im Labor über, um zu untersuchen, wie sich diese microRNA im Gewebe verhält. Sie zeigten, dass Exosomen von Patienten von menschlichen Kardiomyozyten problemlos aufgenommen wurden und miR‑339‑5p in die Zellen ablieferten. Wenn sie miR‑339‑5p künstlich erhöhten, sanken die NLRC5‑Spiegel und der PI3K/Akt‑Signalweg wurde aktiver. Gleichzeitig produzierten die Zellen mehr Kollagen und ein Protein namens alpha‑glatte Muskelaktin — beides Kennzeichen von fibrotischem, steifem Gewebe statt flexiblem, gesundem Muskel. Wurde miR‑339‑5p blockiert, kehrten diese Veränderungen um, was darauf hindeutet, dass diese einzelne microRNA Herz‑Zellen in einen narbenbildenden Zustand treiben kann.
Was das für Patientinnen und Patienten und die zukünftige Versorgung bedeutet
Indem die Studie diese Ereigniskette abbildet — von erhöhtem miR‑339‑5p in Blutexosomen über vermindertes NLRC5, aktivierten PI3K/Akt‑Signalen bis zu erhöhten Narbenproteinen — verknüpft sie einen messbaren Blutmarker mit einem plausiblen Mechanismus für Schäden im Herzen. Für Patientinnen und Patienten eröffnet sich die Möglichkeit, dass ein routinemäßiger Bluttest eines Tages schadhafte Umbaumaßnahmen früher erkennen könnte als heutige Bild- und Laborverfahren. Gleichzeitig wird angedeutet, dass Medikamente, die miR‑339‑5p dämpfen oder NLRC5‑Aktivität wiederherstellen, das Fortschreiten der Versteifung und Vernarbung verlangsamen könnten, die die Herzinsuffizienz verschlimmern. Obwohl größere und längerfristige Studien noch nötig sind, könnten diese winzigen RNA‑Boten sowohl eine Warnleuchte im Armaturenbrett als auch ein neues Ziel unter der Motorhaube bieten.
Zitation: Cheng, D., Hu, J., Zhao, M. et al. Plasma exosomal hsa-miR-339-5p is associated with NOD-like receptor family CARD domain-containing 5 in heart failure with reduced ejection fraction. Sci Rep 16, 5690 (2026). https://doi.org/10.1038/s41598-026-35519-0
Schlüsselwörter: Herzinsuffizienz, Exosomen, microRNA, Fibrose, Biomarker