Clear Sky Science · de
Strukturelle und rechnergestützte Entwicklung von 2,5-disubstituierten-1,3,4‑Oxadiazol‑Analoga als aktive LOX-, Urease‑ und α‑Glucosidase‑Hemmer
Neue chemische Werkzeuge zur Bekämpfung verbreiteter Krankheiten
Viele alltägliche Gesundheitsprobleme – von Geschwüren und Nierensteinen bis hin zu Diabetes und chronischen Entzündungen – werden durch überaktive Enzyme im Körper begünstigt. In dieser Studie wird eine Familie neu entworfener kleinmolekularer Verbindungen untersucht, die wie winzige Bremsen für drei solche Enzyme wirken. Durch gezielte Strukturvariation und Tests im Labor sowie am Rechner wollen die Forschenden die Grundlage für künftig wirksamere und sicherere Medikamente legen. 
Warum diese Enzyme wichtig sind
Das Team konzentrierte sich auf drei Enzymziele, die sehr unterschiedliche, aber gleichermaßen bedeutende Rollen für die Gesundheit spielen. Urease hilft beim Abbau von Harnstoff; wenn sie in bestimmten Bakterien oder Geweben überaktiv ist, kann das zu Magen‑ und Harnwegsulzera, Nierensteinen und sogar erhöhtem Blutdruck beitragen. Alpha‑Glucosidase sitzt an der Oberfläche von Darmzellen und spaltet komplexe Kohlenhydrate in Glukose; ihre Hemmung ist ein etabliertes Mittel zur Blutzuckerregulierung bei Typ‑2‑Diabetes. Lipoxygenase (LOX) wandelt Fette in Signalmoleküle um, die Entzündungen, Asthma und manche krebsbezogene Prozesse antreiben. Arzneistoffe, die diese Enzyme dämpfen, ohne andere Systeme zu schädigen, sind daher sehr gefragt.
Aufbau einer Bibliothek möglicher Wirkstoffe
Um solche Wirkstoffe zu finden, synthetisierten die Forschenden eine Reihe von 15 verwandten Verbindungen, basierend auf einem Ringsystem namens 1,3,4‑Oxadiazol, das mit einer Piperidin‑Einheit verbunden ist. Dieses chemische Gerüst kommt bereits in mehreren modernen Medikamenten vor und interagiert gut mit biologischen Zielstrukturen. Das Team variierte die „Dekorationen“ am Kern – kleine Gruppen wie Methyl, Ethyl, Methoxy, Benzyl und Cyclohexyl – an verschiedenen Positionen und erzeugte so eine kleine Kandidatenbibliothek mit den Bezeichnungen 7a bis 7o. Die Struktur jeder Verbindung wurde mit gängigen analytischen Methoden wie Infrarot‑ und Kernspinresonanzspektroskopie bestätigt, um sicherzustellen, dass die Synthesen den Entwürfen entsprachen.
Prüfung der hemmenden Wirkung auf Enzyme
Jede Verbindung wurde anschließend gegen gereinigte LOX, Urease und Alpha‑Glucosidase getestet, um zu ermitteln, wie stark sie die enzymatische Aktivität dämpfen kann. Mehrere Moleküle stachen hervor. Gegen Alpha‑Glucosidase erwiesen sich die Verbindungen 7a und 7n als besonders wirksam und übertrafen in den Labortests das Standarddiabetesmedikament Acarbose, indem sie bei niedrigen Mikromolar‑Konzentrationen hohe Hemmungsraten erreichten. Für LOX zeigten 7a, 7h und 7n sehr starke Aktivität, in einigen Fällen besser als der natürliche Referenzinhibitor Quercetin. In den Urease‑Assays rivalisierten 7a und insbesondere 7l mit dem Standardinhibitor Thiourea oder übertrafen ihn leicht, was darauf hindeutet, dass sie eines Tages als Ausgangspunkte für Anti‑Ulzera‑ oder Anti‑Stein‑Therapien dienen könnten. 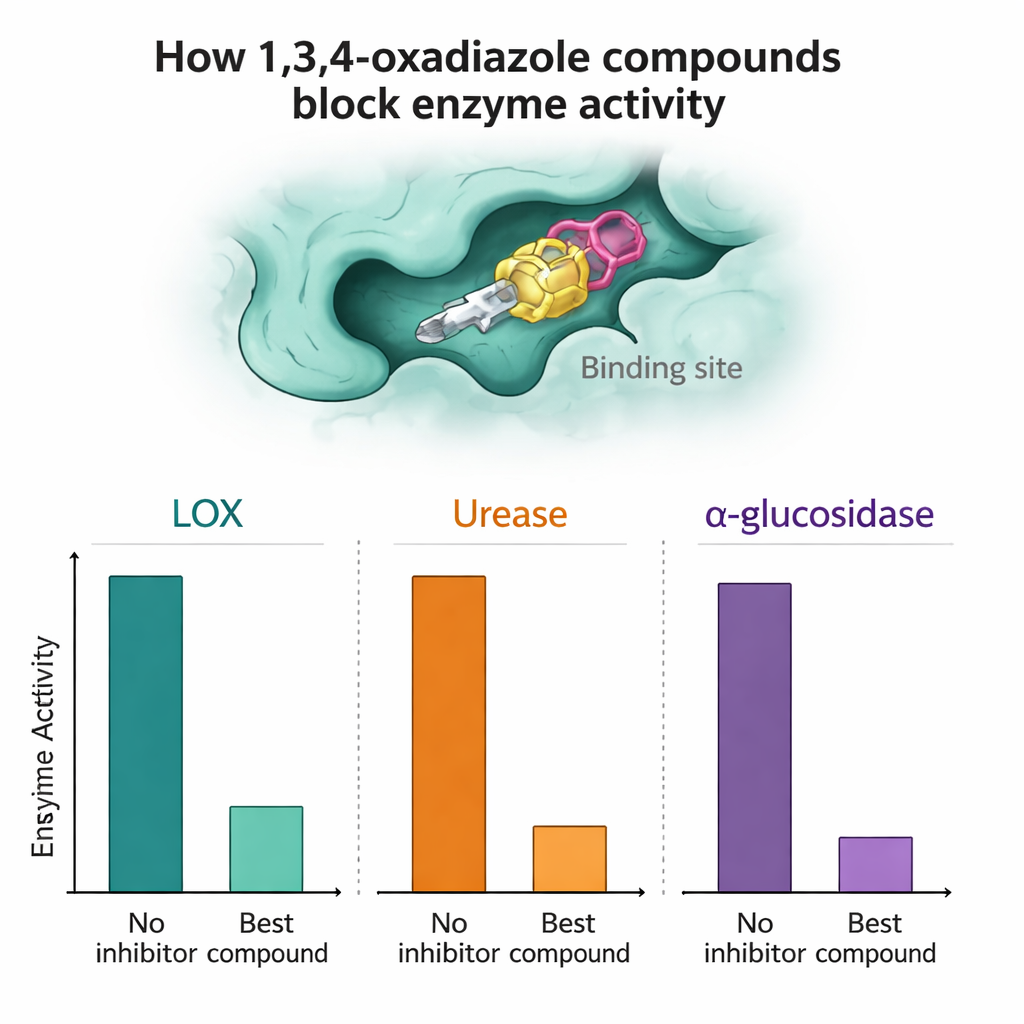
Verknüpfung von Struktur und Wirksamkeit
Da sich die Verbindungen 7a–7o nur durch kleine Änderungen am Kernringsystem unterscheiden, konnten die Forschenden einfache Struktur‑Wirksamkeits‑Beziehungen skizzieren. Beispielsweise verstärkte die Einführung kleiner, kohlenstoffreicher Gruppen an bestimmten „ortho“‑Positionen eines angehängten Rings häufig die Fähigkeit, Alpha‑Glucosidase oder LOX zu hemmen. Andere Substituenten, etwa bestimmte Methoxy‑ oder Estergruppen an weniger günstigen Positionen, schwächten dagegen die Aktivität. Um die Gründe dafür zu verstehen, nutzte das Team Computersimulationen. Quantenchemische Berechnungen zeigten, dass alle Moleküle thermodynamisch stabil und flexibel genug sind, um sich an Enzymtaschen anzupassen. Docking‑Studien – die virtuelle Einpassung jedes Moleküls in dreidimensionale Modelle der Enzyme – zeigten, dass die am stärksten aktiven Verbindungen durch eine Mischung aus Wasserstoffbrücken und hydrophoben (ölig‑artigen) Wechselwirkungen an Schlüsselstellen der aktiven Zentren engeren Kontakt herstellten, während schwächere Kandidaten weniger passgenau saßen oder kritische Kontaktpunkte verfehlten.
Was das für zukünftige Medikamente bedeutet
Vereinfacht gesagt identifiziert die Studie eine Handvoll vielversprechender „Schlüssel“, die gut in drei krankheitsbezogene „Schlösser“ passen, und beginnt zu erklären, auf atomarer Ebene, warum manche Schlüssel besser drehen als andere. Keine dieser Verbindungen ist noch reif für ein Medikament – es sind noch Sicherheitsprüfungen, Optimierungen des pharmakokinetischen Verhaltens sowie Tierversuche und klinische Studien erforderlich. Die Arbeit zeigt jedoch, dass das 1,3,4‑Oxadiazol‑Piperidin‑Gerüst ein fruchtbarer Ausgangspunkt für künftige Behandlungen von Diabetes, entzündlichen Erkrankungen und ureasebedingten Störungen ist. Die Kombination aus sorgfältigen Laborbefunden und detaillierter Computermodellierung liefert eine Roadmap, um diese Kandidaten zu präziseren und wirksameren Wirkstoffen zu verfeinern.
Zitation: Javid, J., Aziz-ur-Rehman, Iqbal, J. et al. Structural and computational supported development of 2,5-disubstituted-1,3,4-oxadiazole analogues as active LOX, urease, and α-glucosidase inhibitors. Sci Rep 16, 5866 (2026). https://doi.org/10.1038/s41598-026-35499-1
Schlüsselwörter: Enzymhemmer, Wirkstoffforschung, Oxadiazol‑Verbindungen, Diabetes und Entzündungen, Urease und Lipoxygenase