Clear Sky Science · de
SHP2 fördert Osteosarkom durch Regulation des STAT3/TET3/HOXB2‑Signalwegs
Warum diese Knochenkrebs‑Studie wichtig ist
Osteosarkom ist die häufigste primäre Knochentumorerkrankung bei Kindern und Jugendlichen. Trotz moderner Chemotherapie und Operationen hat sich das Überleben von Patientinnen und Patienten mit fortgeschrittener oder rezidivierender Erkrankung über Jahrzehnte kaum verbessert. Diese Studie geht den inneren Schaltkreisen von Osteosarkomzellen nach, um herauszufinden, welche Moleküle als „Hauptschalter“ fungieren und Tumoren Wachstum, Ausbreitung und Therapie‑Resistenz verleihen. Indem sie einen zentralen Regelweg um das Protein SHP2 aufdeckt, weist die Arbeit auf neue Wirkstoffziele, die künftig dazu beitragen könnten, Osteosarkomtherapien wirksamer und präziser zu machen.
Denen folgen, die die Tumorgenaktivität verraten
Die Forschenden begannen, Osteosarkom als Datenproblem zu behandeln. Sie durchsuchten öffentliche Genexpressionsdatensätze, in denen Tumorproben mit normalem Knochengewebe verglichen wurden, und nutzten statistische Werkzeuge, um Gene zu finden, die in Krebs konsequent hoch- oder herunterreguliert sind. Hunderte Gene unterschieden sich, viele davon gruppierten sich in bekannten Krebswegen, die Zellwachstum, Überleben und Bewegung antreiben. Unter diesen stach ein Protein hervor: SHP2, das als Knoten stark mit mehreren anderen verknüpft war – dem Signalfaktor STAT3, dem DNA‑modifizierenden Enzym TET3 und dem Entwicklungsregulator HOXB2. Das deutete darauf hin, dass diese Moleküle eine verknüpfte Kette bilden könnten, die aggressives Verhalten von Osteosarkomzellen fördert. 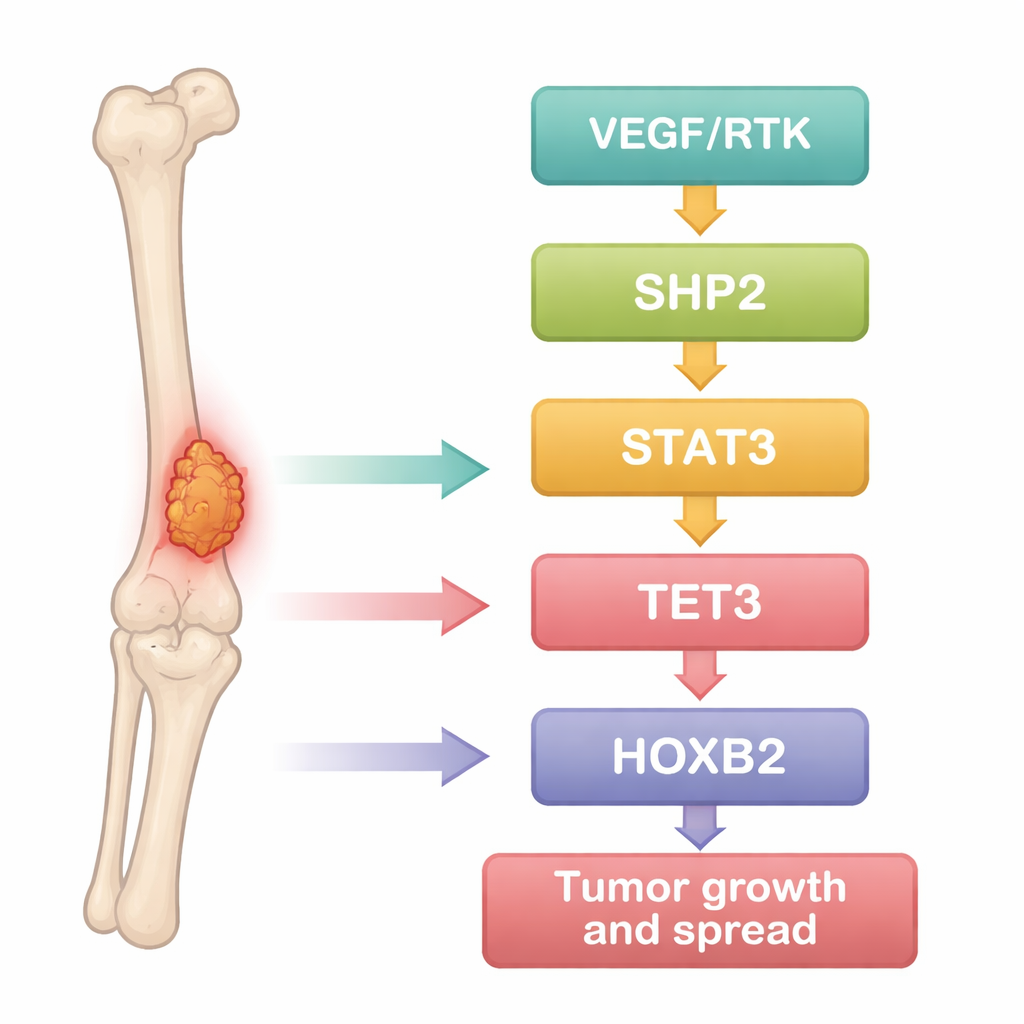
Überprüfung der Rolle von SHP2 in Krebszellen
Um über bloße Korrelationen hinauszukommen, erzeugte das Team menschliche Osteosarkomzelllinien (143B und MG63), in denen SHP2 entweder reduziert oder erhöht wurde. Bei Herunterregulierung von SHP2 nahmen die Fähigkeiten der Zellen, sich zu vermehren, über eine Oberfläche zu wandern und durch eine Membran zu invasieren, deutlich ab. Auch die Mengen an STAT3‑, TET3‑ und HOXB2‑Proteinen sowie krebsassoziierten Markern wie c‑Myc, NANOG und NUSAP1 sanken. Durch Reaktivierung von STAT3 oder Überexpression von HOXB2 wurden viele dieser Effekte rückgängig gemacht, was darauf hinweist, dass SHP2 stromaufwärts in einer Kaskade sitzt, die letztlich Gene beeinflusst, die Zellteilung, stamzellähnliche Eigenschaften und die Apparatur der Zellteilung steuern.
Aufbau eines schrittweisen Krebsweges
Aus den Experimenten entwerfen die Autorinnen und Autoren ein stufenweises Modell. Im Tumormilieu stimulieren hohe Konzentrationen des vaskulären endothelialen Wachstumsfaktors (VEGF) Rezeptortyrosinkinasen (RTKs) an der Zelloberfläche. Diese aktivieren wiederum SHP2 innerhalb der Zelle. Aktives SHP2 schaltet STAT3 an, einen Transkriptionsfaktor, der in den Zellkern wandert und die Produktion von TET3 erhöht. TET3 bearbeitet dann chemische Markierungen auf der DNA, indem es Methylgruppen in der HOXB2‑Genregion entfernt. Diese Demethylierung wirkt wie das Lösen einer Bremse und erlaubt eine stärkere Expression von HOXB2. HOXB2, ein Gen, das normalerweise die Entwicklung lenkt, steigert nun die Aktivität von c‑Myc, NANOG und NUSAP1, die zusammen unablässiges Tumorwachstum antreiben, invasives Verhalten verstärken und Merkmale unterstützen, die mit Metastasierung verbunden sind.
Vom Petrischälchen zum lebenden Tier
Um zu prüfen, ob dieser Weg in Tumoren im lebenden Organismus relevant ist, setzten die Wissenschaftlerinnen und Wissenschaftler veränderte Osteosarkomzellen unter die Haut von Mäusen. Tumoren, die aus Zellen mit erhöhter SHP2‑Expression entstanden, wuchsen größer und waren schwerer als Kontrolltumoren. Wurde TET3 in diesen SHP2‑reichen Zellen ausgeschaltet, verlangsamte sich das Tumorwachstum und die HOXB2‑Spiegel sanken, obwohl SHP2 und STAT3 weiterhin aktiv blieben. Die Wiedereinführung von HOXB2 stellte die Tumoraggressivität wieder her. Messungen der Proteinspiegel in Tumorgewebe spiegelten die früheren Zellkulturbefunde wider und untermauerten die Vorstellung, dass SHP2, STAT3, TET3 und HOXB2 als Achse wirken, die das Osteosarkom in Richtung eines maligneren Verhaltens treibt. 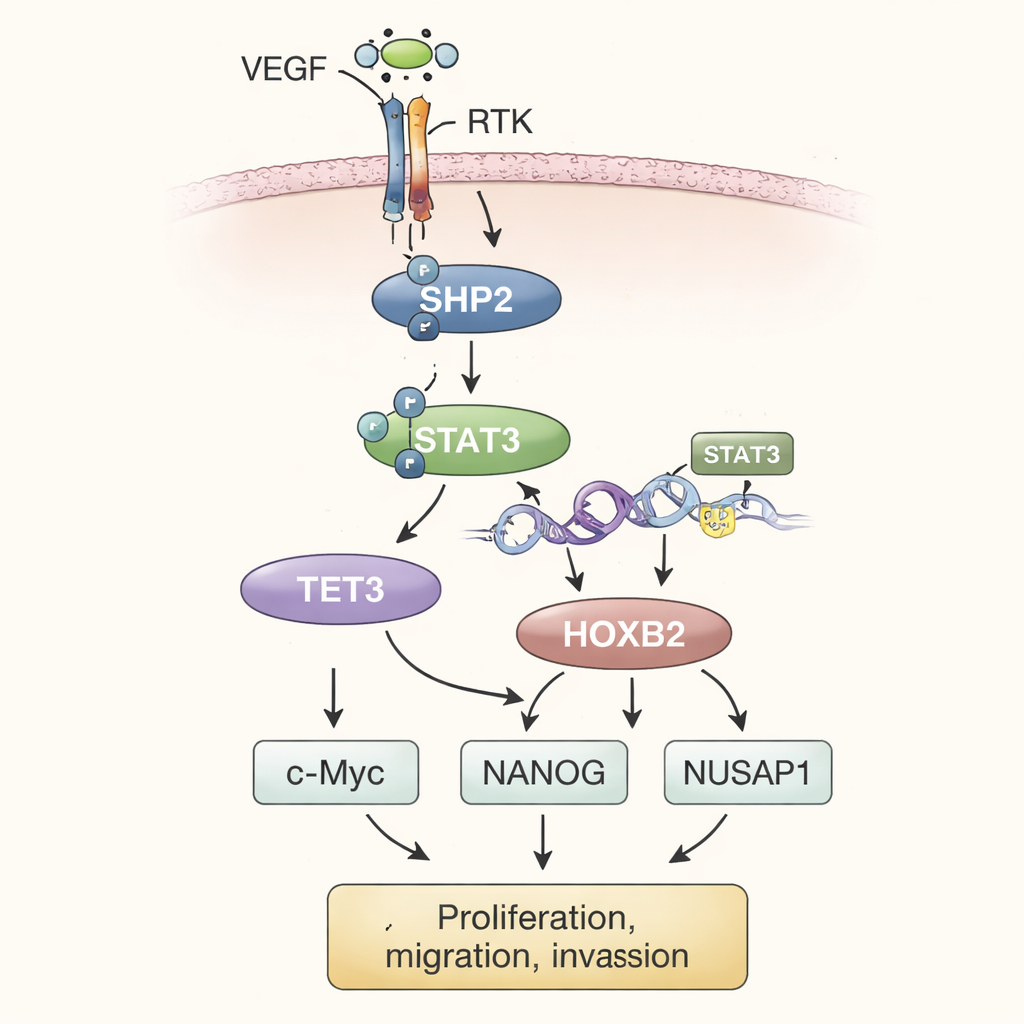
Was das für zukünftige Behandlungen bedeutet
Für nichtfachliche Leserinnen und Leser lautet die zentrale Botschaft: Die Forschenden haben eine klare Signalkette nachvollzogen – von VEGF und seinen Oberflächenrezeptoren über SHP2 und STAT3 bis hin zu TET3, HOXB2 und mehreren starken Wachstumsgenen –, die erklärt, warum Osteosarkom schnell wachsen und früh metastasieren kann. Da SHP2 und STAT3 Enzyme sind, die prinzipiell durch niedermolekulare Hemmstoffe blockiert werden könnten, und TET3 sowie HOXB2 spätere Schritte in derselben Route markieren, bietet dieser Weg mehrere Ansatzpunkte, an denen künftige Therapien eingreifen könnten. Obwohl die Studie in Zelllinien und Mäusen durchgeführt wurde, liefert sie eine detaillierte Karte, die Arzneimittelentwicklern helfen kann, Kombinationsbehandlungen zu entwerfen, die die zentralen Steuerschalter des Tumors abschalten, statt nur seine Endeffekte anzugreifen.
Zitation: Yang, H., Ji, J. SHP2 promotes osteosarcoma via regulating STAT3/TET3/HOXB2 signaling. Sci Rep 16, 6158 (2026). https://doi.org/10.1038/s41598-026-35493-7
Schlüsselwörter: Osteosarkom, SHP2, STAT3‑Signalweg, Tumorsignalgebung, gezielte Therapie