Clear Sky Science · de
Nichtinvasive PET‑Bildgebung von LPS‑induziertem oxidativem Stress in der Skelettmuskulatur mit einem auf ROS zielenden Radiotracer
Warum gestresste Muskeln wichtig sind
Im Alter, bei Infektionen oder längerer Immobilität im Krankenhaus können Muskeln schrumpfen und an Kraft verlieren. Viel von diesem verborgenen Schaden beginnt lange bevor sich die Muskelgröße sichtbar verändert und wird von instabilen Molekülen, den sogenannten reaktiven Sauerstoffspezies (ROS), angetrieben. Diese Studie untersucht eine neue Methode, um diesen unsichtbaren chemischen Stress in Muskeln mittels einer medizinischen Aufnahme namens PET sichtbar zu machen. Das könnte Ärzten ermöglichen, Probleme frühzeitig zu erkennen — bevor Muskelverlust schwer umkehrbar wird. 
Ein genauerer Blick auf unsichtbaren Muskelstress
Der Skelettmuskelschwund ist der schrittweise Verlust von Muskelmasse und -kraft, der mit Alterung, schweren Erkrankungen, Inaktivität oder Behandlungen wie Chemotherapie einhergehen kann. Klassisch greifen Ärztinnen und Ärzte auf Werkzeuge wie Biopsien, MRT oder CT zurück, um den Zustand der Muskeln zu beurteilen. Diese Verfahren zeigen Veränderungen in Größe und Struktur, können aber nicht die frühen chemischen Signale darstellen, die den Schaden in Gang setzen. Eines der frühesten und wichtigsten dieser Signale ist oxidativer Stress — eine Überladung mit ROS, die das chemische Gleichgewicht der Zelle stört und Signalwege aktiviert, welche die Muskelproteine abbauen. Die Fähigkeit, diesen Stress direkt in lebendem Muskelgewebe zu messen, könnte helfen, Risikopersonen zu identifizieren und zu verfolgen, ob Maßnahmen zum Schutz der Muskeln wirken.
Ein Tracer, der schädliche Moleküle sichtbar macht
Die Forschenden konzentrierten sich auf einen spezialisierten PET‑Bildgebungstracer namens [18F]ROStrace, der so entwickelt wurde, dass er Superoxid — eine wichtige Form von ROS — anvisiert. Nachdem bestätigt worden war, dass der Tracer zuverlässig hergestellt werden kann und über mehrere Stunden stabil bleibt, überprüften sie, ob er tatsächlich auf oxidativen Stress in im Labor gezüchteten Muskelzellen reagiert. Mäuse‑Muskelzellen (C2C12‑Myotuben), die dem bakteriellen Toxin LPS ausgesetzt wurden, welches Entzündung und ROS auslöst, nahmen im Zeitverlauf mehr [18F]ROStrace auf als unbehandelte Zellen. Wurden die Zellen mit einem Antioxidans geschützt, sank die Traceraufnahme; wurden die ROS mit einer anderen Verbindung verstärkt, stieg die Aufnahme. Diese Muster zeigten, dass das Signal des Tracers mit den ROS‑Spiegeln zunahm und abnahm und nicht mit allgemeinen Veränderungen in Zellform oder Stoffwechsel zusammenhing. 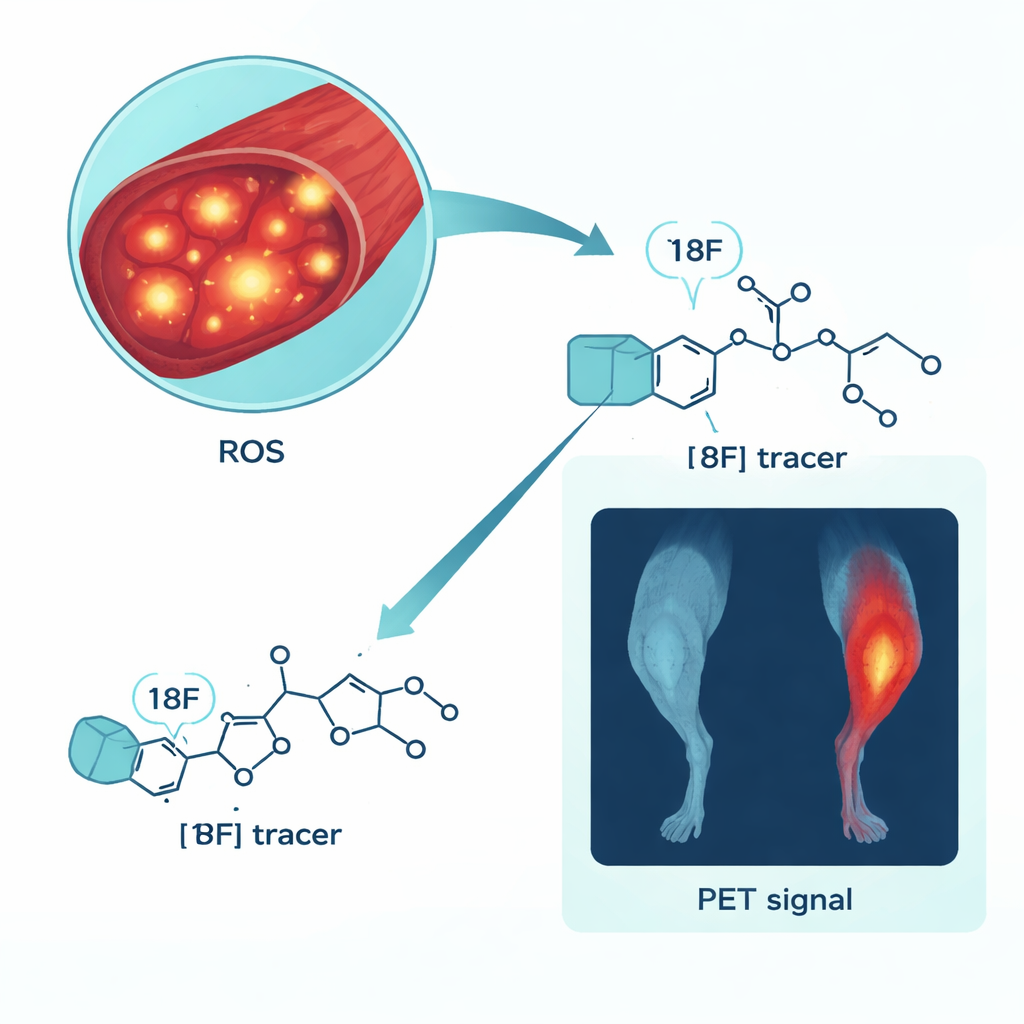
Vom Reagenzglas zu lebenden Muskeln
Als Nächstes prüfte das Team an Mäusen, ob [18F]ROStrace oxidativen Stress in echtem Muskelgewebe aufdecken kann. Mäusen wurde LPS injiziert, um einen systemischen Entzündungszustand zu erzeugen, der frühe Anzeichen von Muskelschwund verursacht. Mit PET/CT scannten die Wissenschaftler die Tiere etwa einen Tag später und maßen die Traceraufnahme in den Hinterbeinmuskeln. Im Vergleich zu gesunden Kontrollmäusen zeigte die LPS‑behandelte Gruppe etwa doppelt so starke PET‑Signale in diesen Muskeln, was auf eine deutlich höhere oxidative Belastung hinweist. Zeitverlaufsscans zeigten, dass die Tracerwerte im Muskel etwa eine Stunde nach Injektion ein stabiles Plateau erreichten und damit ein praktisches Bildfenster für zukünftige Studien und mögliche klinische Anwendungen definierten.
Biologische Hinweise hinter dem starken Signal
Um zu bestätigen, dass die PET‑Bilder wirklich schädliche chemische Vorgänge und nicht Blutfluss oder andere unspezifische Effekte widerspiegeln, analysierten die Forschenden dieselben Muskeln mit mehreren etablierten Labormethoden. Unter dem Mikroskop erschienen LPS‑behandelte Muskeln und kultivierte Myotuben dünner, und einzelne Fasern hatten eine geringere Querschnittsfläche — Merkmale, die mit frühen Stadien des Muskelschwunds übereinstimmen. Die Mitochondrien, die Kraftwerke der Zelle, zeigten ein reduziertes Membranpotenzial, ein Zeichen für gestörtes inneres Gleichgewicht unter oxidativem Stress. Schlüsselgene, die den Muskelabbau antreiben, MuRF‑1 und Atrogin‑1, waren in LPS‑behandelten Zellen und Geweben stark erhöht. Schließlich bestätigte eine Anfärbung mit einem fluoreszierenden Farbstoff, der der Chemie von [18F]ROStrace eng verwandt ist, dass die ROS‑Spiegel tatsächlich in den Muskeln erhöht waren, die stärkere PET‑Signale zeigten — sowohl in Zellkulturen als auch in lebenden Mäusen.
Was das für Patientinnen und Patienten bedeuten könnte
Insgesamt zeigen die Ergebnisse, dass [18F]ROStrace‑PET nichtinvasiv Bereiche mit oxidativem Stress in der Skelettmuskulatur sichtbar machen kann und dass die Intensität des Signals mit anderen Kennzeichen frühen Muskelschadens korreliert. Für Patientinnen und Patienten könnte dieser Ansatz eines Tages ermöglichen, Muskelstress zu erkennen, bevor erheblicher Schwund eintritt, zu überwachen, wie gut neue Medikamente oder Trainingsprogramme schädliche chemische Prozesse beruhigen, und das Verständnis von Zuständen wie sepsisbedingter Schwäche bis hin zur altersbedingten Gebrechlichkeit zu verbessern. Obwohl weitere Langzeit‑ und Studien am Menschen nötig sind, öffnet dieses auf ROS ausgerichtete Bildgebungswerkzeug ein neues Fenster dafür, wann und wie Muskeln zu versagen beginnen — und wie man früher eingreifen könnte.
Zitation: Park, J.Y., Park, S.M., Lee, T.S. et al. Noninvasive PET imaging of LPS-induced oxidative stress in skeletal muscle using a ROS-targeting radiotracer. Sci Rep 16, 4917 (2026). https://doi.org/10.1038/s41598-026-35489-3
Schlüsselwörter: Muskelschwund, oxidativer Stress, PET‑Bildgebung, reaktive Sauerstoffspezies, [18F]ROStrace