Clear Sky Science · de
Neubewertung des Verlaufs von Typ‑1‑Diabetes in der nicht‑adipösen diabetischen Maus
Warum kleine Maus‑Pankreata für die menschliche Gesundheit wichtig sind
Typ‑1‑Diabetes wird häufig erst diagnostiziert, wenn die meisten insulinproduzierenden Zellen in der Bauchspeicheldrüse bereits verloren sind. Um die Krankheit zu verhindern oder zu verzögern, brauchen Forschende Tiermodelle, die die allerersten Stadien dieser langsamen Zerstörung abbilden. Diese Studie setzt sich erneut mit einem klassischen Forschungsmodell auseinander – der nicht‑adipösen diabetischen (NOD) Maus –, um zu prüfen, ob gängige Kriterien, mit denen Mäuse als „diabetisch“ eingestuft werden, ein entscheidendes frühes Schadensfenster übersehen, das dem beim Menschen ähnlicher aussieht. 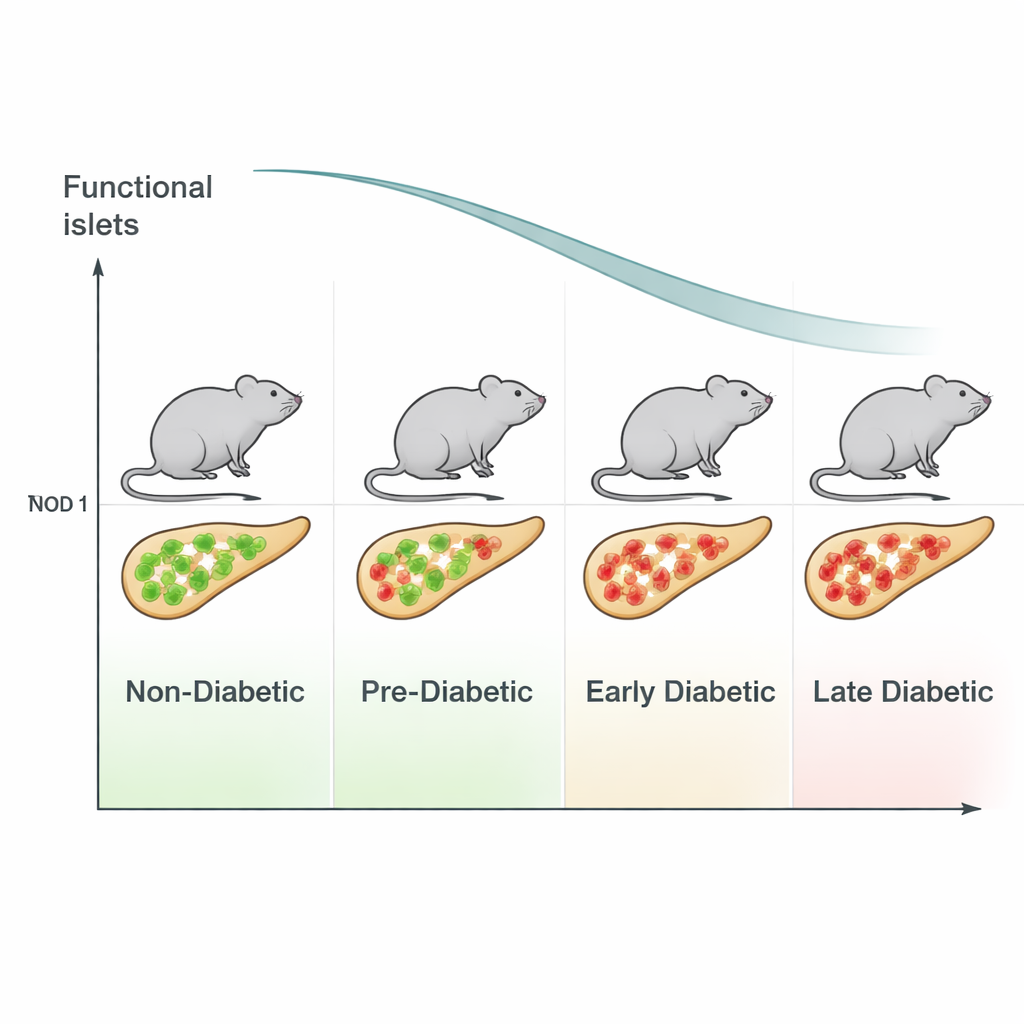
Ins Innere der Bauchspeicheldrüse blicken, bevor Diabetes offensichtlich wird
Die Forschenden konzentrierten sich auf NOD‑Mäuse, deren Blutzuckerwerte noch unter der üblichen Diabetes‑Grenze von 200 Milligramm pro Deziliter (mg/dL) lagen. Dieser Bereich – 80 bis 200 mg/dL – ist der Ort, an dem subtile Veränderungen lange vor voller Ausprägung der Krankheit stattfinden könnten. Sie untersuchten das Pankreas von 38 weiblichen NOD‑Mäusen unterschiedlichen Alters sowie von gesunden Kontrollmäusen und Mäusen mit sehr fortgeschrittenem Diabetes. Mithilfe fortschrittlicher Fluoreszenzfärbungen und automatisierter Bildanalyse kartierten sie Tausende von Langerhans‑Inseln, den kleinen Clustern endokriner Zellen, zu denen auch die insulinproduzierenden Beta‑Zellen gehören. So konnten sie zählen, welche Zellen vorhanden waren und wie viele Immunzellen jede Insel infiltriert hatten.
Fünf Stadien des Insel‑Schadens
Durch die Kombination detaillierter Bilder mit computerbasierten Regeln sortierte das Team 3.324 Inseln in fünf Schadensstadien, von Stadium 0 (weitgehend gesund) bis Stadium 4 (stark geschädigt). In den frühen Stadien enthielten die Inseln noch viele insulinproduzierende Beta‑Zellen, und nur wenige Immunzellen lauerten in der Nähe. Mit fortschreitenden Stadien umringten und durchdrangen zunehmend T‑Zellen die Inseln, Beta‑Zellen verschwanden nahezu, und glucagonproduzierende Alpha‑Zellen zusammen mit anderen endokrinen Zellen übernahmen die Rolle. In den am stärksten geschädigten Inseln blieben fast keine Beta‑Zellen mehr, und Immunzellen waren weitgehend verschwunden, sodass Inseln von anderen Zelltypen dominiert wurden. Gesunde Kontrollmäuse sahen größtenteils wie Stadium 0 aus, während stark diabetische Mäuse überwiegend Stadien 3 und 4 zeigten. 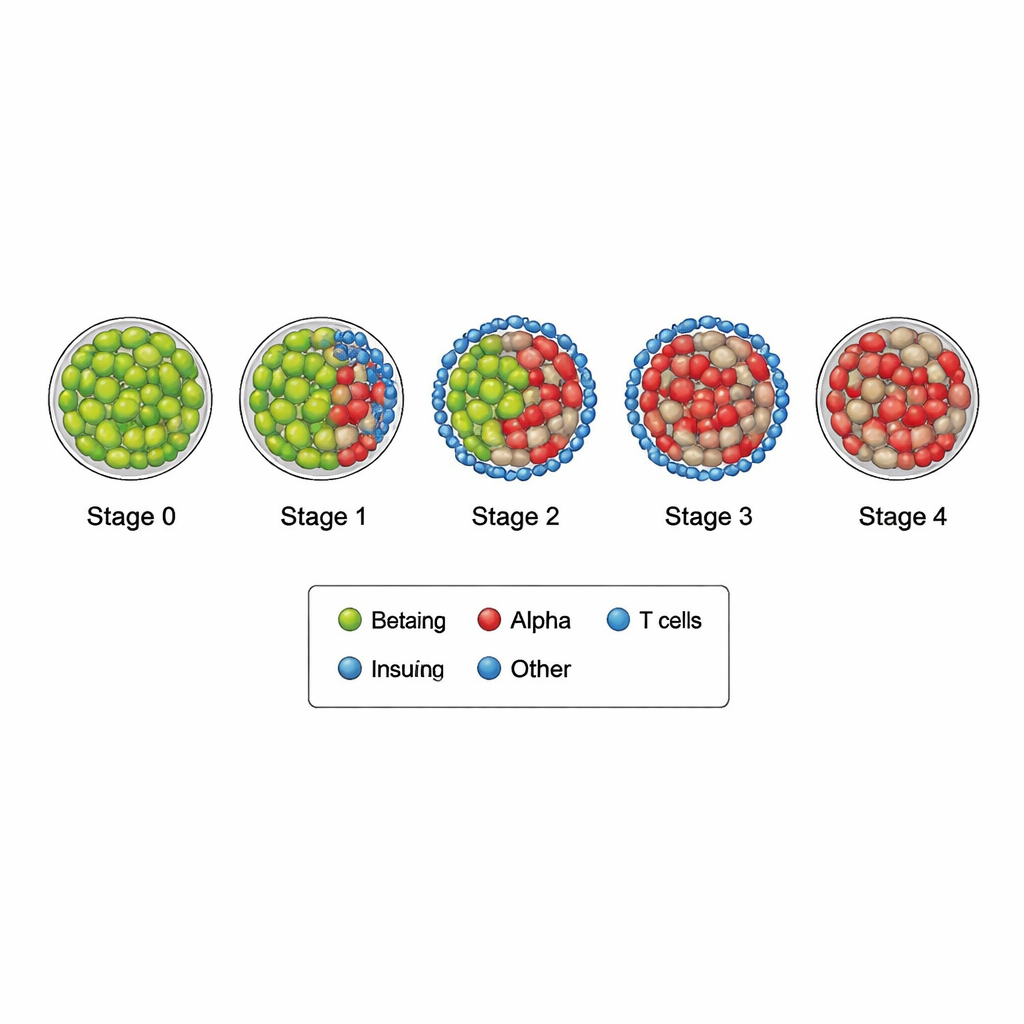
Blutzucker als frühes Warnsignal
Anschließend verknüpften die Wissenschaftler diese Insel‑Stadien mit dem durchschnittlichen Blutzucker jedes Tieres über die vorangegangenen zwei Wochen. Sie stellten fest, dass eine große Verschiebung im Insel‑Zustand bei etwa 126 mg/dL stattfand – eine vertraute Zahl, denn sie entspricht auch dem standardmäßigen Nüchtern‑Schwellenwert zur Diabetesdiagnose beim Menschen. Unter etwa 115 mg/dL befanden sich die meisten Inseln in den frühesten, gesünderen Stadien. Über etwa 135 mg/dL hatten die meisten Inseln die stärker geschädigten Stadien 3 und 4 erreicht, mit wenigen verbleibenden Beta‑Zellen. Zwischen diesen Werten lag eine Übergangszone, in der einige Mäuse bereits einen großen Anteil geschädigter Inseln aufwiesen, obwohl ihre Blutzuckerwerte noch nicht als diabetisch nach den üblichen Mäuseexperimenten gelten würden.
„Nicht‑diabetisch“, „prädiabetisch“ und „frühdiabetisch“ bei Mäusen neu definieren
Um diesen verborgenen Verlauf zu erfassen, entwickelten die Forschenden einen „Islet Score“, der das durchschnittliche Stadium aller Inseln in jeder Maus widerspiegelt. Mit diesem Score zusammen mit dem Blutzucker identifizierten sie drei sinnvolle Untergruppen bei Tieren, deren Blutzucker noch unter 200 mg/dL lag. Mäuse mit niedrigen Scores und Blutzucker unter 126 mg/dL wurden als nicht‑diabetisch bezeichnet; sie hatten überwiegend intakte Inseln. Eine kleine Gruppe mit höheren Scores, aber noch normalem Blutzucker, wurde als prädiabetisch eingestuft: Ihre Inseln waren bereits stark angegriffen, obwohl der Blutzucker akzeptabel erschien. Eine dritte, frühdiabetische Gruppe wies sowohl höhere Scores als auch Blutzucker über 126 mg/dL auf, was einen Punkt markiert, an dem das Pankreas die Blutzuckerregulation zu verlieren begann, jedoch noch vor den extremen Werten, die traditionell zur Definition von Diabetes bei NOD‑Mäusen verwendet werden.
Was das für die zukünftige Diabetesforschung bedeutet
Diese Arbeit legt nahe, dass die gängige Mäuse‑Schwelle von 200 mg/dL eine kritische frühe Phase des Beta‑Zell‑Verlusts übersieht. Indem man den praktischen Schwellenwert auf etwa 126 mg/dL senkt und das neue inselbasierte Bewertungssystem einsetzt, können Forschende das NOD‑Maus‑Modell besser an die Entwicklung von Typ‑1‑Diabetes beim Menschen anpassen. Für Nicht‑Spezialisten lautet die Kernbotschaft: Der Schaden an insulinproduzierenden Zellen kann umfangreich sein, lange bevor der Blutzucker deutlich auffällig wird. Das Erkennen und Untersuchen dieses früheren Stadiums bei Mäusen kann Forschenden helfen, Therapien zu entwerfen und zu testen, die Beta‑Zellen schützen, bevor sie weitgehend zerstört sind.
Zitation: Ehall, B., Herbsthofer, L., Obermüller, B. et al. Revisiting type 1 diabetes progression in the non-obese diabetic mouse. Sci Rep 16, 5768 (2026). https://doi.org/10.1038/s41598-026-35483-9
Schlüsselwörter: Typ‑1‑Diabetes, NOD‑Maus, Beta‑Zell‑Verlust, Inselentzündung, frühe Diagnose