Clear Sky Science · de
Globale RNA-Expressionsanalyse von Patientenproben identifizierte potenzielle diagnostische Biomarker, spezifisch für peritoneale, ovarielle und tiefe Endometriose
Warum diese Erkrankung im Alltag wichtig ist
Endometriose betrifft schätzungsweise 190 Millionen Frauen weltweit und verursacht häufig starke Beckenschmerzen, Erschöpfung und Probleme mit der Fruchtbarkeit. Dennoch warten viele Menschen fast ein Jahrzehnt auf eine eindeutige Diagnose, die meist erst durch eine Operation bestätigt wird. Diese Studie stellt eine einfache, aber kraftvolle Frage: Können wir stattdessen die molekularen „Fingerabdrücke“ des Körpers lesen, um Endometriose früher zu erkennen und sogar ihre verschiedenen Formen zu unterscheiden — möglicherweise mithilfe eines einfachen Tests in der Zukunft?
Verschiedene Gesichter derselben Krankheit
Endometriose entsteht, wenn Gewebe, das dem Gebärmutterschleimhautgewebe ähnelt, an Stellen wächst, wo es nicht hingehört, etwa am Eierstock, an der dünnen Bauchinnenhaut (Peritoneum) oder tief in den Beckenorganen. Diese Orte definieren drei Hauptsubtypen: ovarielle, peritoneale und tiefe Endometriose. Jeder kann unterschiedliche Schmerzprofile, Fruchtbarkeitsprobleme und Organschäden verursachen. Heute stützen sich Ärztinnen und Ärzte auf Symptome, bildgebende Verfahren und häufig auf eine Laparoskopie — einen Eingriff unter Narkose —, um die Diagnose zu bestätigen und den Subtyp zu bestimmen. Eine nichtinvasive Methode, diese Formen zu unterscheiden, würde vielen Frauen Jahre der Unsicherheit und Operationen ersparen.
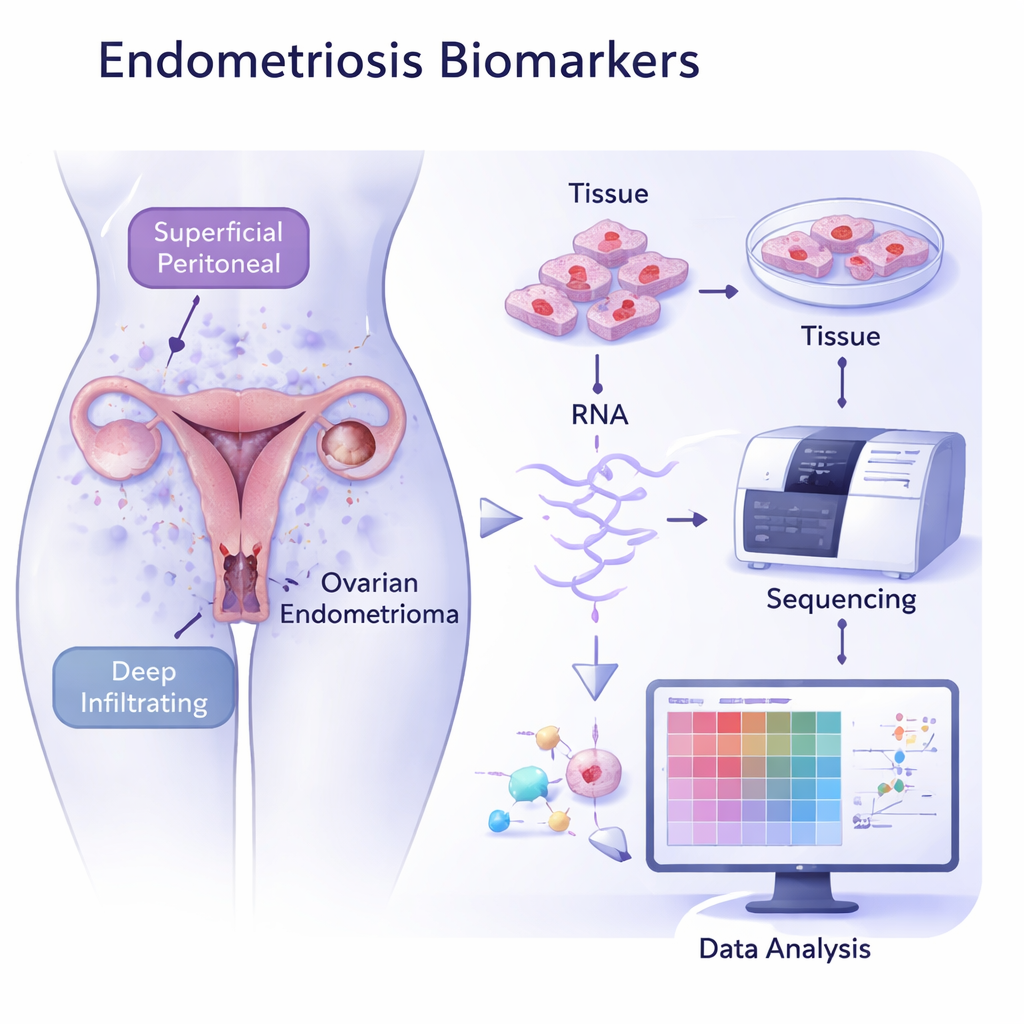
Das RNA-„Barcode“ kranker Gewebe lesen
Die Forschenden sammelten Gewebeproben von 26 Frauen mit Endometriose — aus allen drei Subtypen — und von 15 Frauen ohne die Erkrankung. Anschließend nutzten sie RNA-Sequenzierung, eine Methode, die misst, welche Gene ein- oder ausgeschaltet sind, um ein globales Bild der Aktivität in diesen Geweben zu erstellen. Beim Vergleich des erkrankten Gewebes mit der gesunden Gebärmutterschleimhaut gruppierten sich die Proben in klar unterscheidbare Cluster und zeigten unterschiedliche Genaktivitätsmuster. Ovarielle Läsionen bildeten eine enge Gruppe, während peritoneale und tiefe Läsionen zusammenhielten, was die Vorstellung stützt, dass diese Subtypen trotz gemeinsamer Merkmale unterschiedlichen biologischen Wegen folgen.
Geteilte Bahnen von Narbenbildung und Entzündung
In allen drei Subtypen fanden die Forschenden eine höhere Aktivität in Genen, die am Aufbau und Umbau des Gewebegerüsts (extrazelluläre Matrix) beteiligt sind, eine erhöhte Zellkontraktilität, wie sie bei Narbenbildung typisch ist, und starke entzündliche Signalwege. Diese Veränderungen passen zu klinischen Beobachtungen: steife, fibröse Läsionen, die Schmerzen und Verwachsungen verursachen. Die Studie entdeckte außerdem ein verändertes immunologisches Umfeld in den Läsionen. So genannte M2-Makrophagen, eine Art Immunzelle, die mit Wundheilung und Fibrose assoziiert ist, waren besonders häufig, während natürliche Killerzellen (NK-Zellen) — wichtig für die Beseitigung auffälliger Zellen — deutlich reduziert waren. Dieses Ungleichgewicht könnte dem endometriotischen Gewebe helfen, trotz Fehlplatzierung zu überleben und sich auszubreiten.
Subtypspezifische molekulare Hinweise
Über diese gemeinsamen Muster hinaus wies jeder Subtyp seine eigene molekulare Signatur auf. Bei tiefer und peritonealer Endometriose waren Gene, die an Phosphodiesterase-Signalwegen beteiligt sind — Pfade, die bereits mit anderen fibrotischen Erkrankungen in Verbindung gebracht wurden — stark erhöht. Bei ovarieller Endometriose fielen Gene im Zusammenhang mit Immunpräsentation und Hormonproduktion auf, was darauf hindeutet, dass der Eierstock ein eigenes biochemisches Umfeld bietet. Die Forschenden untersuchten auch nicht-kodierende RNAs, Moleküle, die keine Proteine herstellen, aber die Genaktivität regulieren können. Sie identifizierten mehrere, die insgesamt oder spezifisch in bestimmten Subtypen deutlich erhöht waren, was auf neue regulatorische Akteure und mögliche Biomarker hindeutet, die in Blut oder anderen Körperflüssigkeiten nachweisbar sein könnten.
Vielversprechende Proteinmarker für zukünftige Tests
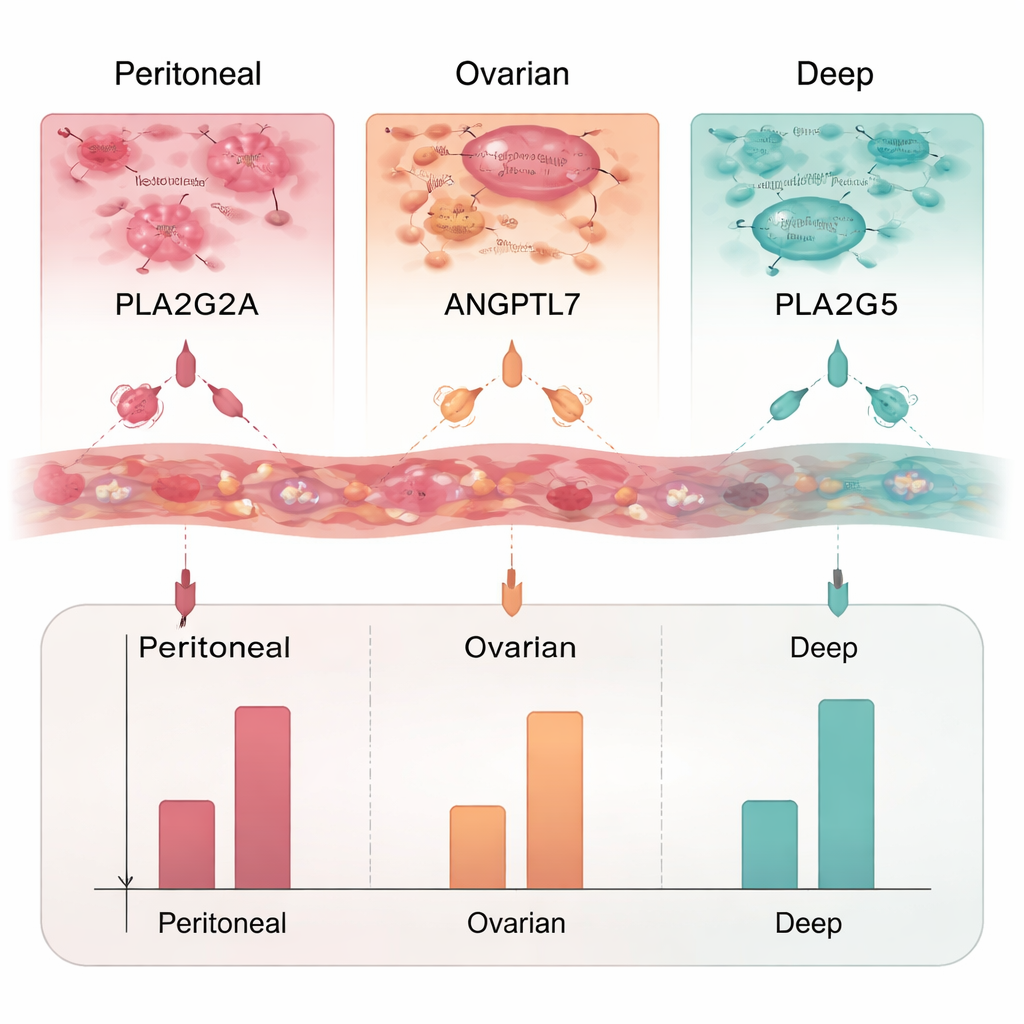
Aus der langen Liste veränderter Gene konzentrierte sich das Team auf solche, die sekretierte Proteine produzieren — ideale Kandidaten für einen späteren Bluttest. Sie wählten drei Proteine für eine genauere Untersuchung: PLA2G2A, ANGPTL7 und PLA2G5. Mittels ELISA, einer Labor‑methode zur Messung von Proteinspiegeln, fanden sie heraus, dass PLA2G2A bei allen drei Endometriose‑Typen erhöht war, besonders bei ovariellen Läsionen. ANGPTL7 war hauptsächlich bei tiefen und peritonealen Läsionen erhöht, während PLA2G5 nur bei der tiefen Endometriose anstieg. Zusammen bilden diese Proteine ein potenzielles Panel, das nicht nur auf das Vorhandensein von Endometriose hinweisen, sondern auch auf die mögliche Lokalisation der Läsionen deuten könnte.
Was das für Patientinnen bedeutet
Diese Forschung liefert noch keinen fertigen Bluttest, legt aber wichtige Grundlagen. Indem sie abbildet, wie Tausende von Genen und Immunzellen in verschiedenen Endometriose-Subtypen agieren, benennt die Studie spezifische Proteine — PLA2G2A, ANGPTL7 und PLA2G5 —, die zukünftig nichtinvasiv messbar sein könnten. Wenn solche Marker in größeren, unabhängigen Patientengruppen validiert werden, könnten Kombinationen dieser Marker den langen Weg bis zur Diagnose verkürzen, die Notwendigkeit von Operationen allein zur Bestätigung der Erkrankung reduzieren und eine gezieltere Behandlung je nach genauem Subtyp ermöglichen.
Zitation: Lisá, Z., Fanta, M., Kokavec, J. et al. Global RNA expression analysis of patient samples identified potential diagnostic biomarkers specific for peritoneal, ovarian and deep endometriosis. Sci Rep 16, 5070 (2026). https://doi.org/10.1038/s41598-026-35467-9
Schlüsselwörter: Endometriose, Biomarker, RNA-Sequenzierung, Immunzellen, Frauenhealth