Clear Sky Science · de
Zebra-Körpererkennung durch künstliche Intelligenz (ZEBRA): ein rechnergestütztes Werkzeug für die Fabry-Nephropathie
Warum winzige Nierenveränderungen wichtig sind
Die Fabry-Krankheit ist eine seltene erbliche Erkrankung, die allmählich viele Organe schädigt, besonders die Nieren. Eine frühe Behandlung kann schwere Schäden verhindern, doch die ersten Warnzeichen im Nierengewebe sind oft unauffällig und selbst für Fachleute leicht zu übersehen. Diese Studie stellt ein neues Werkzeug der künstlichen Intelligenz (KI) vor, genannt ZEBRA, das digitale Bilder von Nierenbiopsien durchsucht, um Ärzten zu helfen, solche frühen Veränderungen zuverlässiger und schneller zu erkennen.
Eine seltene Erkrankung mit leisem Beginn
Bei der Fabry-Krankheit führt ein fehlendes oder fehlerhaftes Enzym dazu, dass sich fetthaltige Moleküle in Zellen im gesamten Körper anreichern, einschließlich der winzigen Filter in den Nieren. Diese Filter enthalten spezialisierte Zellen, sogenannte Podozyten, die bei der Blutreinigung helfen. Wenn sie überladen sind, wirken ihre Zellinnenräume unter dem Mikroskop geschwollen und „schaumig“. Dieses schaumige Erscheinungsbild ist eines der wenigen frühen Hinweise auf Nierenbeteiligung, besonders bei Frauen und bei milderen, spät beginnenden Formen der Erkrankung. Ähnliche schaumige Veränderungen können jedoch auch bei anderen Erkrankungen auftreten, und die Goldstandard-Bestätigung — die Elektronenmikroskopie — ist nicht immer verfügbar. Daher kann eine Nierenbeteiligung bei Fabry übersehen werden, was Diagnose und Behandlung verzögert.
Glasobjektträger in digitale Hinweise verwandeln
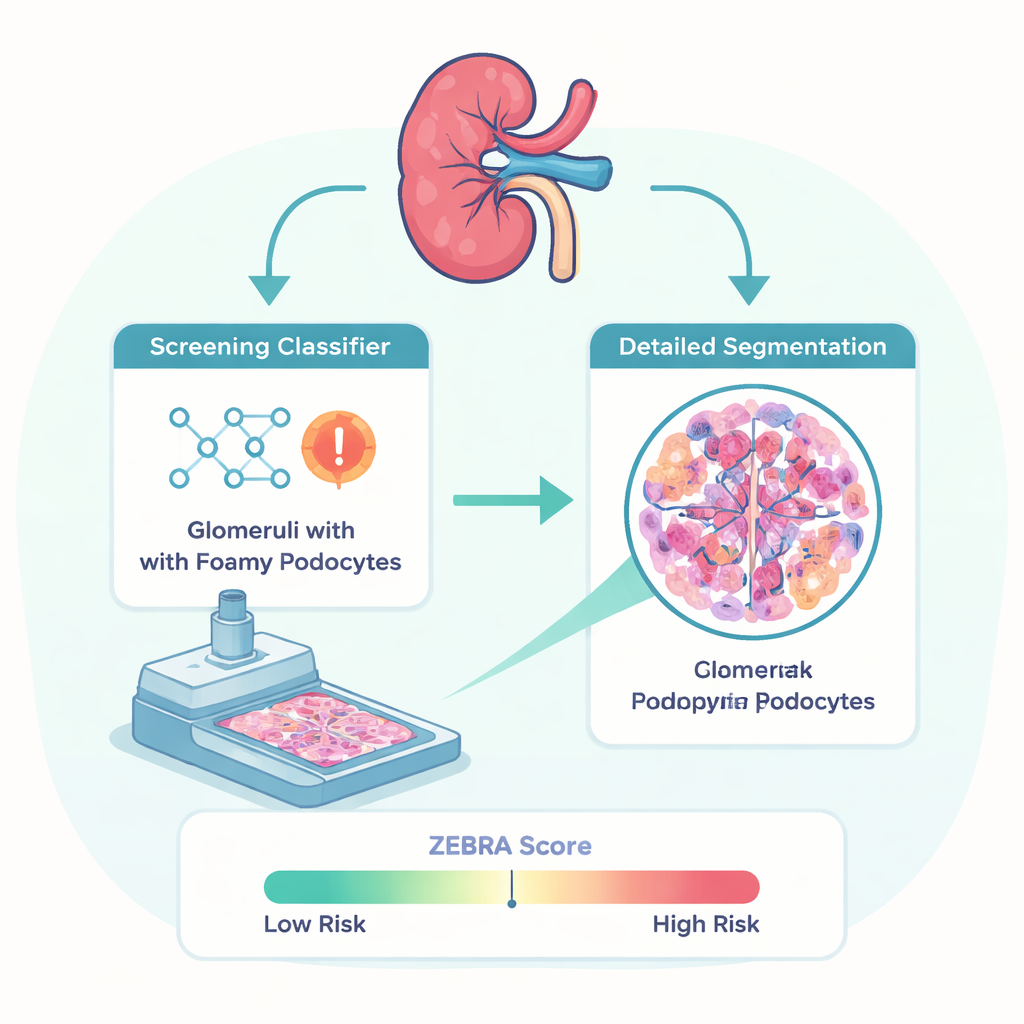
Um dieses Problem anzugehen, sammelten Forschende mehrerer italienischer Zentren Nierenbiopsien von 37 Menschen mit genetisch bestätigter Fabry-Nephropathie und 40 Patientinnen und Patienten mit anderen Nierenerkrankungen. Die Objektträger wurden eingescannt, um hochauflösende digitale Bilder zu erzeugen. Expert:innen der Nierenpathologie markierten dann sorgfältig jeden Glomerulus (die winzige Filtereinheit in der Niere) und zogen Umrisse um einzelne schaumige Podozyten. Mit diesen detaillierten Markierungen als Referenz trainierte das Team zwei Arten von KI-Modellen: ein Klassifikationsmodell, das entscheidet, ob ein Glomerulus schaumige Podozyten enthält, und ein Segmentierungsmodell, das genau nachzeichnet, wo sich diese abnormalen Zellen innerhalb jedes Glomerulus befinden.
Computern beibringen, das zu sehen, was Expert:innen sehen
Das am besten abschneidende Klassifikationsmodell, EfficientNetB2 genannt, kennzeichnete Glomeruli mit oder ohne schaumige Podozyten in etwa vier von fünf Fällen korrekt. Wichtig ist: Auf Patientenebene erkannte es in der unabhängigen Testgruppe alle Fabry-Fälle, obwohl es gelegentlich Glomeruli aus Nicht-Fabry-Erkrankungen fälschlich als verdächtig einstufte. Damit ist es besonders nützlich als hochsensitives Screening-Werkzeug, das Patholog:innen auf Fälle aufmerksam machen kann, die einer näheren Prüfung bedürfen. Das Segmentierungsmodell, basierend auf einer modernen Transformer-Architektur (SegFormerB4), war zwar weniger exakt beim Nachzeichnen der genauen Grenzen, zeigte sich aber sehr sensitiv darin, überhaupt das Vorhandensein schaumiger Podozyten zu erkennen. Zusammen bilden diese Modelle die ZEBRA-Pipeline, die als freie Software verfügbar ist und in gängige digitale Pathologieplattformen integriert werden kann.
Von Pixeln zu einem einfachen Risikoscore
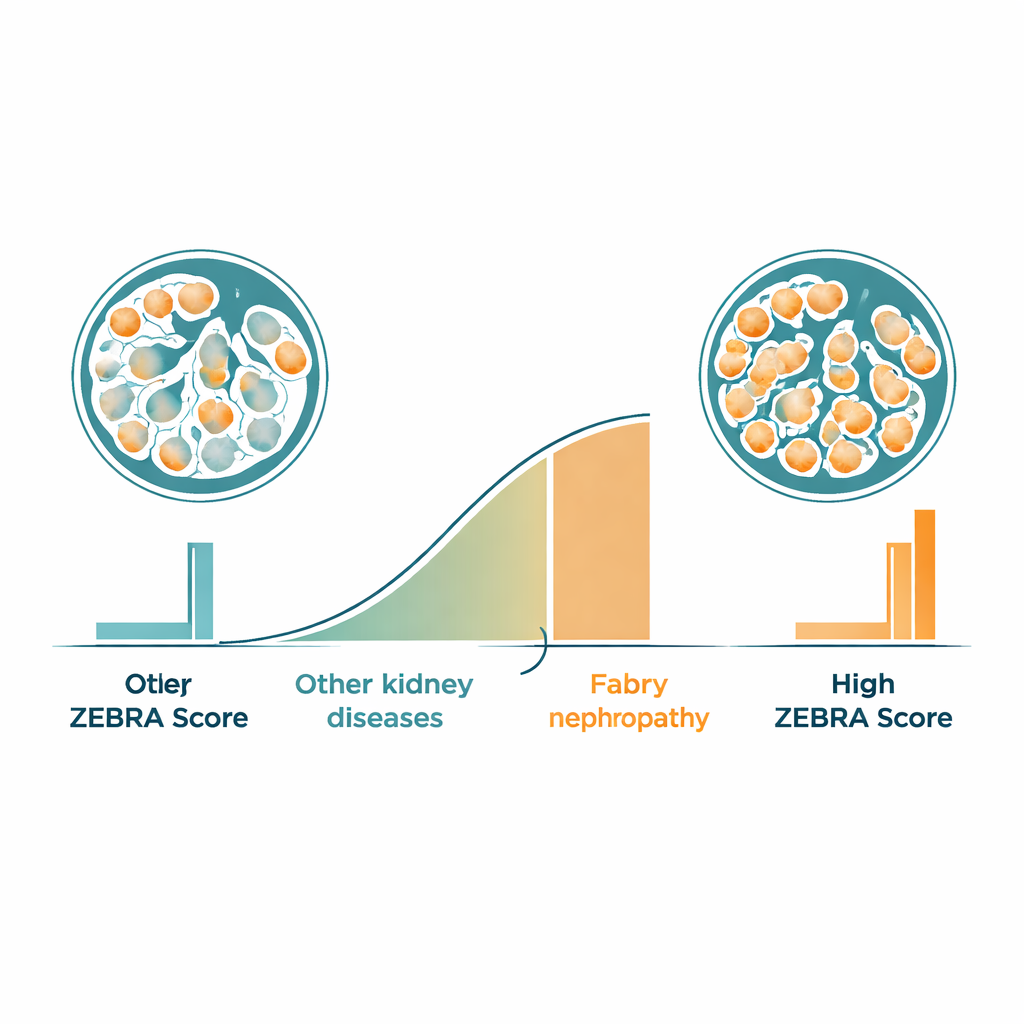
Anhand der Segmentierungsergebnisse entwickelten die Forschenden eine neue numerische Messgröße, den ZEBRA-Score. Für jeden Glomerulus berechnet die Software, welcher Bruchteil der Fläche von schaumigen Podozyten eingenommen wird, und fasst dies anschließend für jede:n Patient:in zusammen. Beim Vergleich von Menschen mit Fabry-Nephropathie und solchen mit anderen Nierenerkrankungen trennte der ZEBRA-Score die beiden Gruppen klar, mit nahezu keiner Überlappung. Ein vorgeschlagener Grenzwert konnte Fabry- von Nicht-Fabry-Fällen mit hoher Sensitivität und guter Spezifität unterscheiden. Der Score stimmte außerdem in angemessenem Maße mit manuellen Bewertungen durch Patholog:innen überein und zeigte moderate Zusammenhänge mit Nierenfunktion und Proteinverlust im Urin, selbst bei Patient:innen, deren Laborwerte noch relativ normal wirkten.
Was das für Patient:innen und Behandlungsteams bedeutet
Diese Arbeit zeigt, dass KI als zusätzliche hochaufmerksame Beobachtung auf routinemäßigen Nierenbiopsie-Objektträgern dienen kann und Patholog:innen dabei hilft, Muster zu erkennen, die sonst übersehen würden. Der ZEBRA-Score soll zwar keine genetische Testung oder fachärztliche Beurteilung ersetzen, kann aber Risikofälle markieren, weiterführende Tests anstoßen und zu konsistenterer Befundberichterstattung zwischen Kliniken beitragen. Mit größeren Studien und Langzeitbeobachtungen könnte dieses digitale Werkzeug Ärzten schließlich nicht nur helfen, die Fabry-Krankheit früher zu diagnostizieren, sondern auch zu überwachen, wie gut Behandlungen die Nieren im Zeitverlauf schützen.
Zitation: Cazzaniga, G., Carbone, M., Barretta, R. et al. Zebra bodies recognition by artificial intelligence (ZEBRA): a computational tool for Fabry nephropathy. Sci Rep 16, 5072 (2026). https://doi.org/10.1038/s41598-026-35466-w
Schlüsselwörter: Fabry-Krankheit, Nierenbiopsie, digitale Pathologie, künstliche Intelligenz, ZEBRA-Score