Clear Sky Science · de
Immunoinformatikbasierte Entwicklung und Bewertung eines Multi-Epitop-Impfstoffs gegen Vibrio fluvialis
Warum ein neuer Impfstoff für Meeresfrüchteliebhaber wichtig ist
Vibrio fluvialis ist ein weniger bekannter Verwandter der Cholera-Erreger, der in warmen Küstengewässern vorkommt und Meeresfrüchte sowie Trinkwasser kontaminieren kann. Er verursacht schwere Durchfallerkrankungen und Darminfektionen und wird mit steigenden Meerestemperaturen sowie schwindender Wirksamkeit von Antibiotika zunehmend häufiger. Für Menschen gibt es derzeit jedoch keinen Impfstoff. Diese Studie nutzt fortgeschrittene Computermethoden, um einen neuen experimentellen Impfstoff zu entwerfen, der aus sorgfältig ausgewählten kleinen Fragmenten des Bakteriums besteht, mit dem langfristigen Ziel, Personen zu schützen, die über Nahrung, Wasser oder klimabedingte Überschwemmungen exponiert sind.

Aus einer versteckten Bedrohung wird ein klares Ziel
Vibrio fluvialis wurde oft mit anderen Vibrio-Arten verwechselt, weshalb seine Rolle bei lebensmittelbedingten Erkrankungen wahrscheinlich unterschätzt wurde. Ausbrüche standen im Zusammenhang mit kontaminierten Meeresfrüchten und verschmutztem Wasser, und kürzliche Stürme und Überschwemmungen haben diese Bakterien ins Landesinnere getragen, wodurch Menschen weit entfernt von der Küste erkrankten. Viele Patienten benötigen Krankenhausbehandlung, und eine besorgniserregende Zahl von Stämmen ist inzwischen gegen mehrere Antibiotika resistent. Da die Oberfläche des Mikroorganismus der verwandter Bakterien ähnelt, können Ärzte Infektionen falsch diagnostizieren und die richtige Behandlung verzögern. All dies schafft einen starken Bedarf an Prävention statt alleiniger Abhängigkeit von Medikamenten.
Entwurf eines Impfstoffs im Computer
Anstatt ganze Bakterien im Labor zu züchten, wandten sich die Forscher der „Immunoinformatik“ zu — der Nutzung von Software, um vorherzusagen, welche kleinen Teile von Vibrio fluvialis am wahrscheinlichsten vom menschlichen Immunsystem erkannt und angegriffen werden. Sie konzentrierten sich auf zwei Membranproteine, die an der Oberfläche des Bakteriums sitzen und für dessen Überleben und Pathogenität wichtig sind. Aus diesen Proteinen extrahierte das Team zehn kurze Abschnitte, sogenannte Epitope, die sowohl von T-Zellen als auch von B-Zellen erkannt werden können, den Hauptakteuren unserer Immunabwehr. Diese Stücke verbanden sie anschließend zu einer einzigen 246‑Aminosäuren-Kette, fügten kurze Verbindungssegmente hinzu, damit das Immunsystem jedes Stück richtig verarbeiten kann, sowie ein Adjuvansfragment zur Verstärkung der Gesamtreaktion.
Prüfung von Wirksamkeit, Sicherheit und weltweiter Reichweite
Sobald der virtuelle Impfstoff konstruiert war, führte das Team eine Reihe von Tests vollständig in silico durch, also am Computer statt an Tieren oder Menschen. Programme sagten voraus, dass das kombinierte Konstrukt für das Immunsystem gut „sichtbar“ sein, aber wahrscheinlich keine Allergien oder Toxizität auslösen würde. Die gewählten Epitope stimmten mit häufigen Varianten der Immun-Gene weltweit überein, was darauf hindeutet, dass etwa 99,97 Prozent der Weltbevölkerung ansprechbar sein sollten, einschließlich Personen in stark betroffenen Regionen wie Süd- und Ostasien. Das Impfstoffprotein erschien außerdem stabil, hydrophil genug, um sich gut zu lösen, und geeignet für eine effiziente Produktion in Standard-Laborbakterien, was eine spätere Herstellung praktikabler macht.
Wie der Impfstoff Schutz auslösen könnte
Die Forscher prüften anschließend, ob das entworfene Protein plausibel mit einem echten Immunsensor interagieren würde. Mithilfe moderner Strukturvorhersagewerkzeuge bauten sie ein dreidimensionales Modell des Impfstoffs und simulierten dann, wie es an den Toll-like-Rezeptor 2 (TLR2) andocken könnte, ein Molekül auf Immunzellen, das bakterielle Komponenten erkennt. Computergestützte Docking-Studien deuteten auf eine enge Passung zwischen dem Impfstoff und TLR2 hin, gestützt durch zahlreiche stabilisierende molekulare Kontakte. Lange, detaillierte Bewegungssimulationen über 100 Nanosekunden zeigten, dass das Impfstoff-Rezeptor-Paar über die Zeit stabil und kompakt blieb. Zusätzliche Simulationen des Immunsystems sagten starke Antikörper- und T-Zell-Antworten sowie die Bildung von Gedächtniszellen voraus, die prinzipiell einen dauerhaften Schutz gegen Vibrio fluvialis bieten könnten.
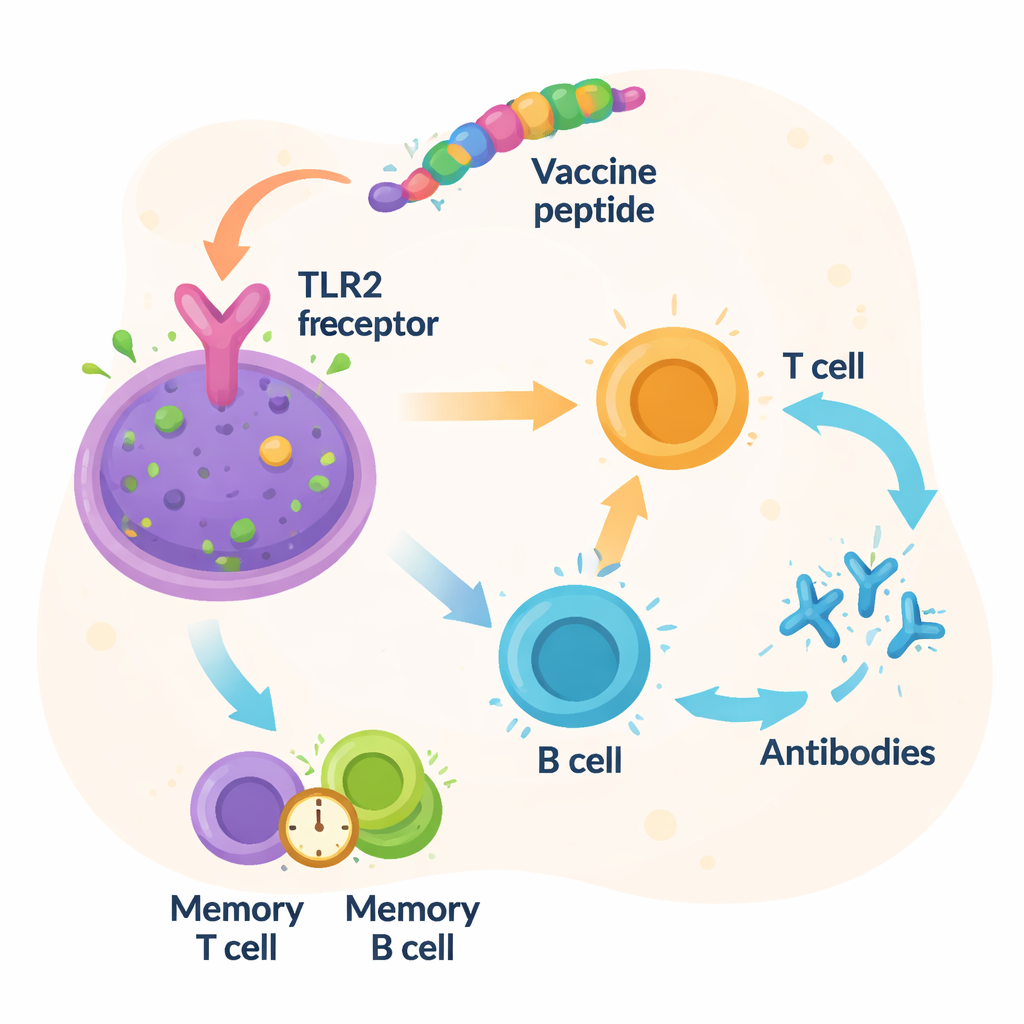
Vom digitalen Plan zum Schutz in der Praxis
Alltäglich gesprochen bietet diese Arbeit einen digitalen „Bauplan“ für einen zukünftigen Vibrio fluvialis-Impfstoff, der nur aus den wichtigsten Fragmenten des Bakteriums besteht, so angeordnet, dass er weitreichend wirksam und potenziell sicherer als Ganzzellimpfstoffe ist. Die Studie zeigt, dass dieses Konstrukt von den meisten menschlichen Immunsystemen erkannt werden sollte, gut an einen wichtigen Immunsensor bindet und mit Standardmethoden herstellbar ist. Allerdings stammen all diese Ergebnisse aus Computermodellen. Die nächsten Schritte erfordern die Herstellung des Impfstoffs im Labor, Tests in Zellen und Tieren und schließlich in klinischen Studien am Menschen, um zu bestätigen, dass er tatsächlich vor Infektionen schützt, ohne Schaden zu verursachen. Wenn diese Tests gelingen, könnten solche Multi-Epitop-Impfstoffe kraftvolle neue Werkzeuge gegen lebensmittelbedingte Bakterien in einer wärmer werdenden und dichter besiedelten Welt werden.
Zitation: Naveed, M., Husnain, M., Aziz, T. et al. Immunoinformatics-based design and evaluation of a multi-epitope vaccine against Vibrio fluvialis. Sci Rep 16, 4100 (2026). https://doi.org/10.1038/s41598-026-35434-4
Schlüsselwörter: Vibrio fluvialis, Multi-Epitop-Impfstoff, lebensmittelbedingte Infektion, Immunoinformatik, Antibiotikaresistenz