Clear Sky Science · de
Entwicklung eines globalen Screeningsystems zur Detektion von Protein–Protein-Interaktionen mittels Lumineszenzkomplementierung in Spalthefe
Das verborgene Leben der Proteine zum Leuchten bringen
Jeder Herzschlag, jeder Gedanke und jeder Atemzug in unserem Körper beruht darauf, dass Proteine in den Zellen zusammenarbeiten. Diese winzigen Partnerschaften, Protein–Protein-Interaktionen genannt, steuern alles von der Genablesung bis zur Stressantwort der Zelle. Viele dieser Verbindungen sind jedoch flüchtig oder empfindlich, weshalb sie mit vorhandenen Methoden schwer nachzuweisen sind. Diese Studie beschreibt ein neues, hochempfindliches "lichtbasiertes" Screening-System in einem einfachen Modellorganismus, der Spalthefe, das gleichzeitig Tausende solcher verborgenen Proteinverbindungen aufdecken kann.
Warum Proteinpartnerschaften so schwer zu erkennen sind
Proteine arbeiten selten allein. Sie binden wechselnde Partner, manchmal nur für einen kurzen Augenblick, und ihr Verhalten kann durch chemische Modifikationen oder durch ihren Ort in der Zelle verändert werden. Traditionelle Methoden zur Untersuchung dieser Interaktionen entfernen Proteine oft aus ihrem natürlichen Umfeld oder beruhen auf genetischen Tricks, die nicht jede Paarung erfassen. Daher sind die bestehenden Karten darüber, wer mit wem in der Zelle interagiert, unvollständig. Die Autoren haben sich vorgenommen, dieses Bild zu verbessern, indem sie ein flexibleres, empfindlicheres System entwickelten, das nahezu jedes Protein der Spalthefe in lebenden Zellen untersuchen kann.
Berührung in Licht verwandeln
Kern der neuen Methode ist ein geteiltes Enzym, das Licht erzeugt. Ein Teil, LgBiT genannt, wird an ein "Köder"-Protein gekoppelt, das die Forschenden untersuchen wollen. Der andere Teil, SmBiT, ist an viele mögliche "Beute"-Partner gekoppelt, jeweils in einem Hefestamm. Für sich genommen interagieren diese beiden Enzymfragmente kaum. Wenn sich Köder und Beute jedoch innerhalb der Zelle binden, fügen sich die Fragmente zusammen und bilden ein funktionsfähiges Enzym, das in Gegenwart eines chemischen Substrats leuchtet. Durch Messung der Lichtintensität jedes Hefestamms kann das Team feststellen, welche Proteine tatsächlich in der Zelle aufeinandertreffen und wie stark ihre Wechselwirkung ist. Um Partner nicht zu übersehen, weil das Tag die normale Funktion blockiert, wird das Köderprotein in zwei Versionen hergestellt, mit LgBiT jeweils am N‑ oder C‑Termin, was die Wahrscheinlichkeit erhöht, dass mindestens eine Orientierung funktioniert. 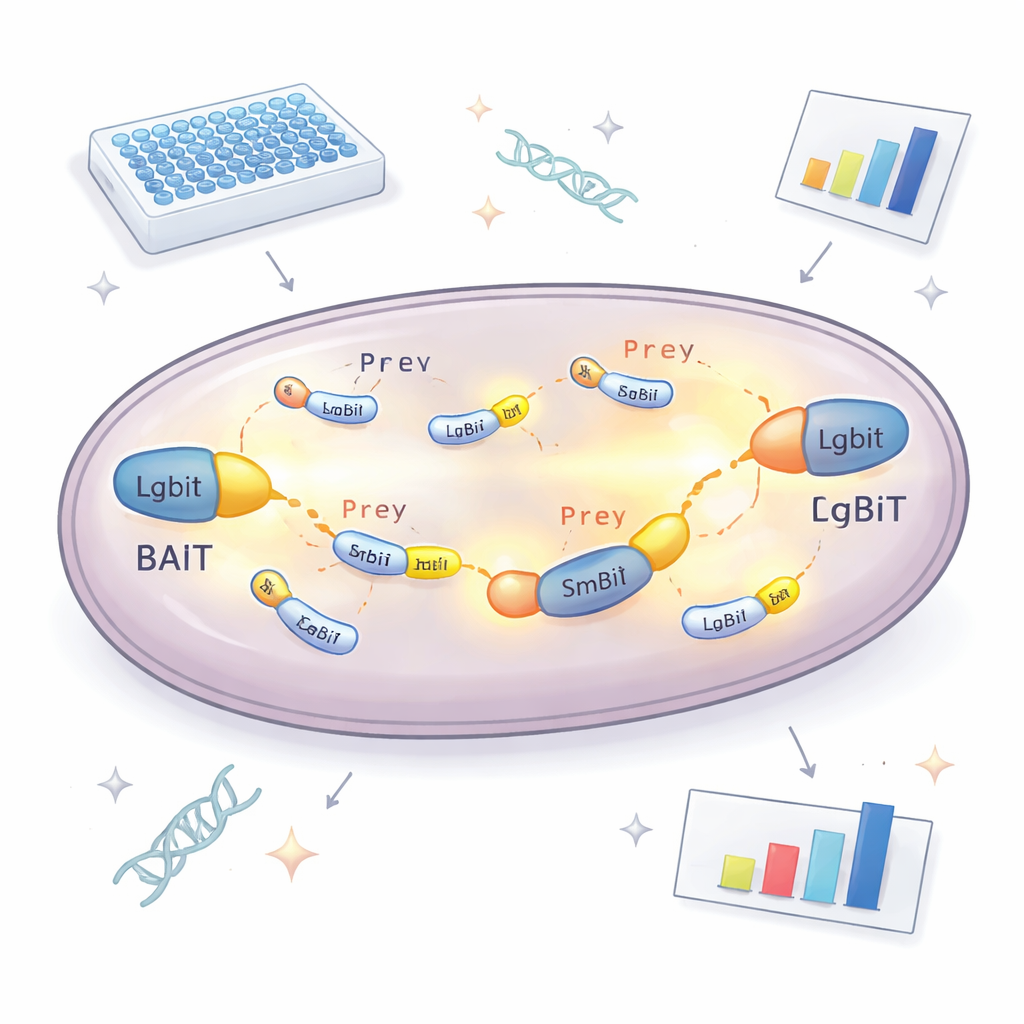
Konstruktion einer Hefebibliothek und eines Stammen-Systems
Der Aufbau dieser Plattform erforderte mehr als nur ein cleveres Enzym. Die Forschenden mussten außerdem Tausende von Beuteproteinen kontrolliert in die Hefe in Ein-Kopie-Manier einbringen. Sie entwarfen einen speziellen DNA-Vektor für Beuteproteine, der an einer definierten Stelle im Hefegenom integriert wird und einen roten Fluoreszenzmarker trägt. Die Helligkeit dieses roten Signals spiegelt wider, wie viele Kopien eingefügt wurden, sodass das Team leicht Kolonien mit genau einer Kopie auswählen kann — eine Voraussetzung für verlässliche Vergleiche. Außerdem erzeugten sie dedizierte Köder-Vektoren, die LgBiT am Anfang oder Ende des Köderproteins platzieren, getrennt durch flexible Linker, damit das Protein weiterhin korrekt falten und sich bewegen kann. Sorgfältig konstruierte Hefestämme wurden dann aufgebaut, um gleichzeitig zwei Köderkonstrukte und ein Beutekonstrukt aufzunehmen; Nährstoffmarker gewährleisteten, dass nur korrekt kombinierte Zellen überleben.
Wie das System sich bewährt
Um zu prüfen, ob ihr Design die Detektion tatsächlich verbesserte, untersuchten die Wissenschaftler zunächst Proteine mit gut bekannten Partnern. Sie bestätigten, dass die Signalstärke stark davon abhängt, wo das lichtemittierende Tag angebracht ist: Manche Interaktionen traten nur auf, wenn LgBiT an einem Ende des Köders saß, nicht am anderen. Die gleichzeitige Expression beider Versionen steigerte das Lichtsignal, was zeigt, dass die Doppel-Köder-Strategie schwache oder orientationsabhängige Interaktionen leichter nachweisbar macht. Das System detektierte auch Kontakte, an denen membrangebundene Proteine beteiligt sind — eine Klasse, die für traditionelle Hefe-Zwei-Hybrid-Methoden berüchtigt schwierig ist. Mit dieser Validierung skalierten die Forschenden auf einen genomweiten Screen hoch und verwendeten ein transkriptionsbezogenes Protein namens Tfs1 als Köder. Beim Screening von mehr als 4.600 Beuteproteinen identifizierten sie 31 starke Kandidaten, darunter mehrere bereits bekannte Partner und viele neue, zum Teil außerhalb des Zellkerns lokalisiert, zum Beispiel in Mitochondrien oder an der Zelloberfläche. 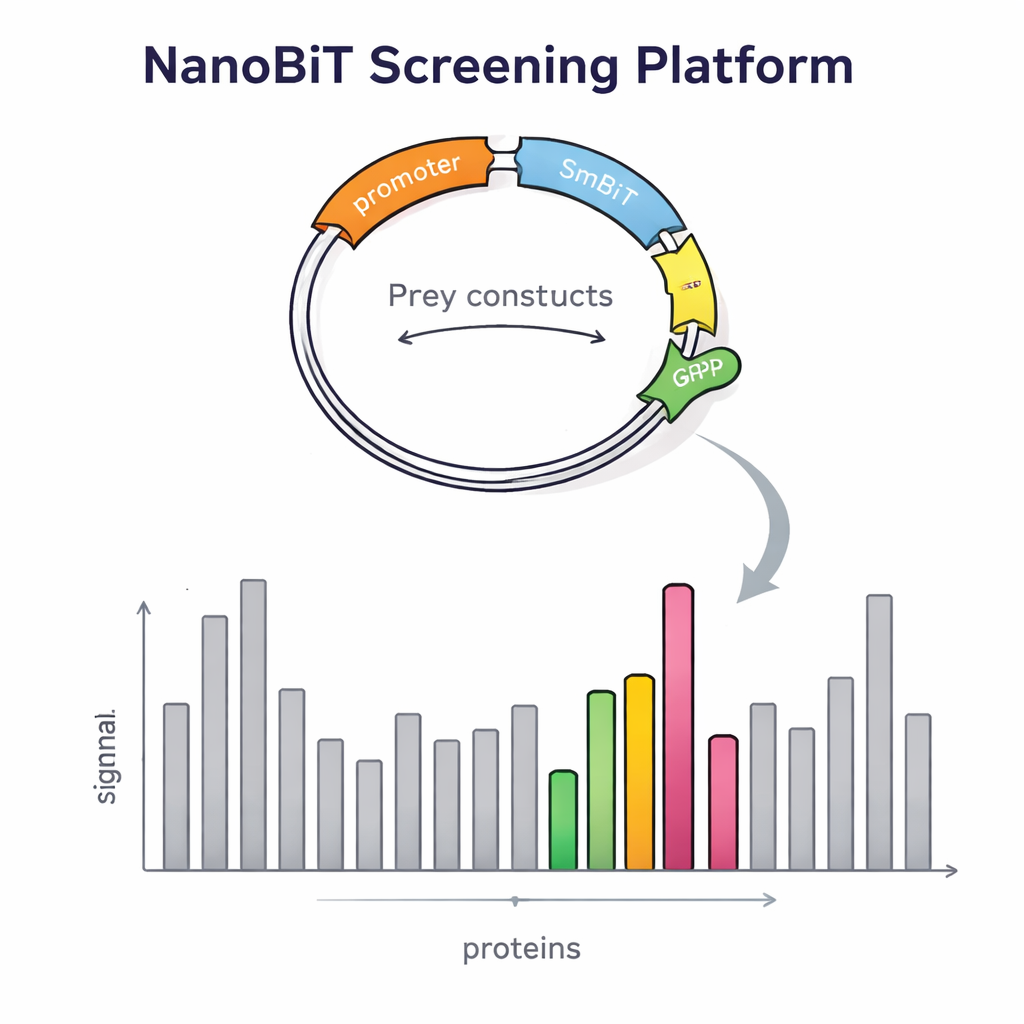
Bedeutung für Biologie und Wirkstoffforschung
Für Nicht-Spezialisten ist die Kernbotschaft, dass die Autoren ein empfindlicheres "Interaktions-Radar" innerhalb von Hefezellen aufgebaut haben. Indem flüchtige Proteinkontakte in messbare Lichtblitze übersetzt und die Genetik so angeordnet wurde, dass drei markierte Proteine zusammen exprimiert werden können, deckt ihr System sowohl bekannte als auch zuvor unsichtbare Proteinpartner auf. Zwar sind weitere Kontrollen mit anderen Techniken nötig, um jede neue Paarung zu bestätigen, doch diese Plattform schließt wichtige Lücken in unseren Karten zellulärer Netzwerke. Da die Stämme zudem so konstruiert wurden, dass sie empfindlicher auf kleine Moleküle reagieren, kann dasselbe System angepasst werden, um nach Wirkstoffen zu suchen, die schädliche Proteinpartnerschaften stören oder nützliche stabilisieren — ein leistungsfähiges neues Werkzeug für die Grundlagenforschung und die frühe Wirkstoffentdeckung.
Zitation: Azadeh, F., Hashimoto, A., Nishimura, S. et al. Development of a global screening system for detecting protein–protein interactions by luminescence complementation in fission yeast. Sci Rep 16, 5034 (2026). https://doi.org/10.1038/s41598-026-35430-8
Schlüsselwörter: Proteininteraktionen, Spalthefe, Lumineszenz-Assay, Hochdurchsatz-Screening, Werkzeuge zur Wirkstoffforschung