Clear Sky Science · de
Signal Recognition Particle‑abhängiges Secretom beim Menschen
Wie Zellen entscheiden, welche Proteine die Zelle verlassen
Unsere Zellen schicken fortlaufend Proteine aus, die Hormone, Antikörper und das Gerüst zwischen Geweben bilden. Nicht jedes Protein ist jedoch zum Verlassen der Zelle bestimmt. Diese Studie stellt eine grundlegende, bisher unbeantwortete Frage: Wie entscheiden menschliche Zellen, welche Proteine auf einen wichtigen Helfer namens Signal Recognition Particle (SRP) angewiesen sind, um das interne Versandzentrum der Zelle zu erreichen, und welche auch ohne dieses System dorthin gelangen können? Indem die Autorinnen und Autoren diese Entscheidung gleichzeitig für Tausende von Proteinen kartieren, zeigen sie, wer vom SRP abhängig ist, wer nicht, und was passiert, wenn dieses System versagt — ein Thema, das für viele Erkrankungen relevant ist, die mit fehlgeleiteten oder fehlenden sekretorischen Proteinen verbunden sind.
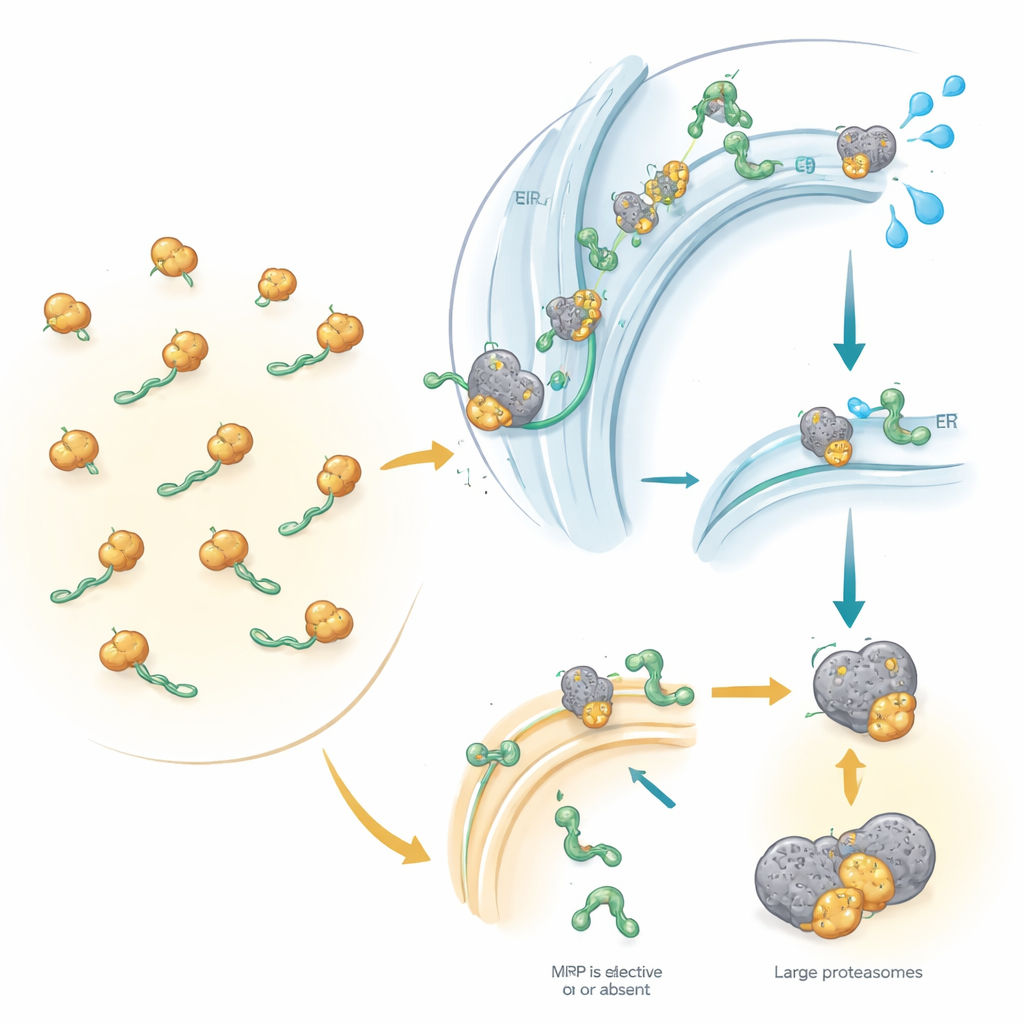
Das Versanddock der Zelle und sein Hauptlotse
Ungefähr eines von drei menschlichen Proteinen ist entweder für die Zelloberfläche, zelluläre Membranen oder die Freisetzung außerhalb der Zelle bestimmt. Um den richtigen Bestimmungsort zu erreichen, müssen die meisten dieser Proteine zuerst in ein Netzwerk interner Membranen eintreten, das endoplasmatische Retikulum — das Versanddock der Zelle. Das SRP fungiert als Lotse: Es erkennt ein kleines „Adressschild“ am Anfang neu entstehender Proteine und stoppt vorübergehend deren Synthese. Diese Pause gibt dem Ribosom — der Proteinfabrikation — Zeit, am endoplasmatischen Retikulum anzudocken, wo die Produktion wiederaufgenommen wird und das wachsende Protein in oder durch die Membran eingefädelt wird. Einige Proteine nutzen jedoch alternative Wege, die kein SRP erfordern, insbesondere sehr kleine Proteine oder solche, die am C‑Ende verankert sind. Bislang wussten Wissenschaftlerinnen und Wissenschaftler nicht in großem Maßstab, welche menschlichen Proteine tatsächlich auf SRP angewiesen sind und welche es umgehen können.
SRP herunterfahren, um zu sehen, was kaputtgeht
Um dies zu untersuchen, reduzierten die Forschenden gezielt die Menge einer essentiellen SRP‑Komponente, SRP54, in menschlichen HeLa‑Zellen. Anschließend nutzten sie eine empfindliche Methode, die Massenspektrometrie, um über 6.000 Proteine innerhalb der Zellen und nahezu 2.000 Proteine im umgebenden Medium — dem sogenannten conditioned medium — zu messen. Der Vergleich zwischen Zellen mit normaler SRP54‑Menge und solchen mit reduziertem SRP54 erlaubte es, zu erkennen, welche Proteine weniger vorhanden waren, welche zunahmen und welche unverändert blieben. Ein starker Rückgang des Proteinspiegels — besonders sowohl innerhalb der Zelle als auch im Medium — wurde als Hinweis darauf gewertet, dass dieses Protein SRP für seine korrekte Synthese und Sortierung benötigt.
Wer ist auf SRP angewiesen und wer kommt ohne aus
Die Analyse zeigte, dass die Mehrheit der normalerweise ins Medium sezernierten Proteine deutlich auf SRP angewiesen ist. Bei Reduktion von SRP54 fielen die meisten dieser sekretorischen Proteine stark ab, insbesondere diejenigen mit einem klassischen Signalsequenz‑„Adressschild“. Viele Membranproteine innerhalb der Zelle nahmen ebenfalls ab und wurden damit als SRP‑Klienten identifiziert. Eine kleinere Gruppe von Proteinen mit ähnlichen Adressschildern blieb weitgehend unbeeinflusst und ist damit SRP‑unabhängig; diese nutzen wahrscheinlich alternative Routen zum endoplasmatischen Retikulum. Die Forschenden entdeckten außerdem, dass spezifische Merkmale der Signalsequenz — etwa eine positiv geladene Region am Anfang — bei SRP‑abhängigen Proteinen häufiger vorkommen, was auf feine Regeln hindeutet, die SRP bei der Auswahl seiner Fracht nutzt. Gleichzeitig stiegen manche Proteine an, die an der Markierung beschädigter Proteine für den Abbau und an mitochondrialen Funktionen beteiligt sind, was darauf hindeutet, dass Zellen Backup‑Mechanismen und Energieproduktion hochfahren, wenn ihr Hauptlotse gestört ist.
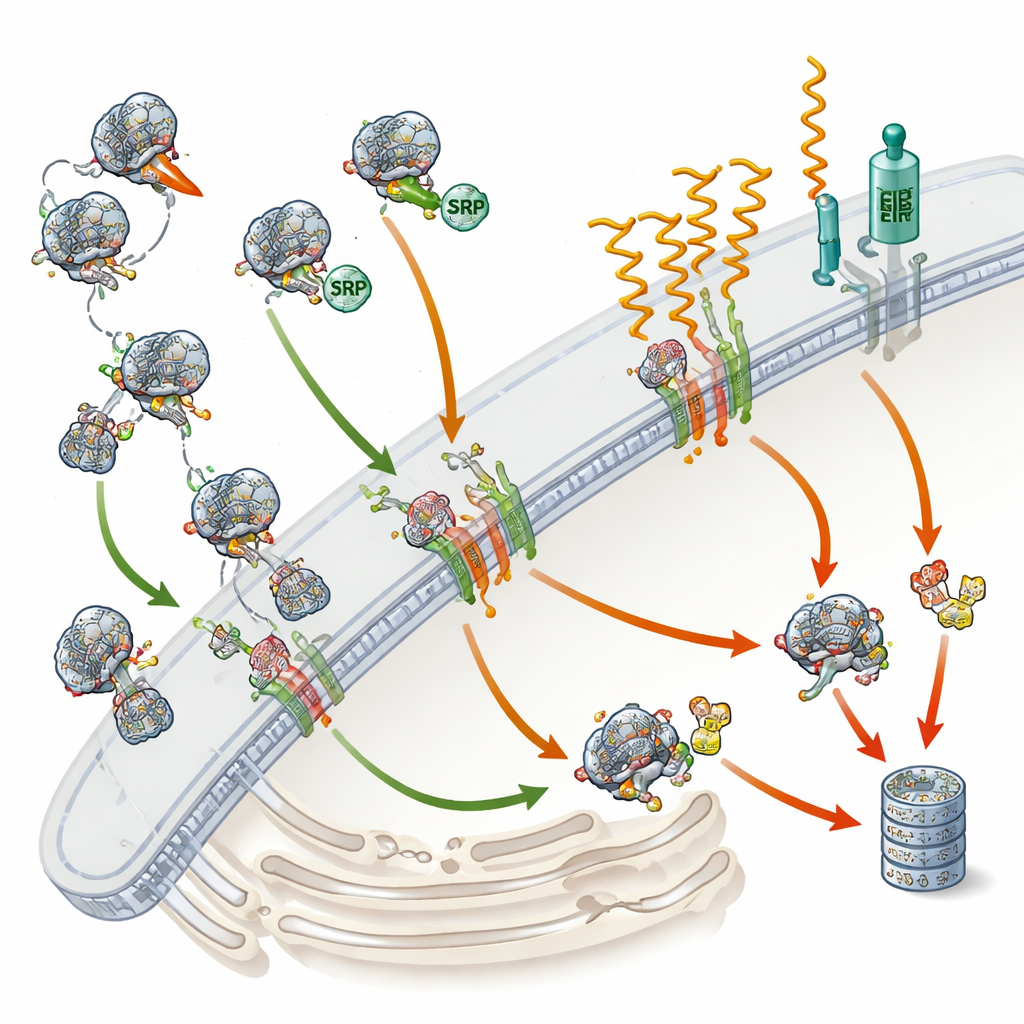
Qualitätskontrolle, wenn das Targeting schiefgeht
Die Studie ging über das bloße Zählen von Proteinen hinaus: Sie verglich diese Veränderungen mit Verschiebungen in der messenger‑RNA, den Blaupausen für die Proteinsynthese. Viele SRP‑abhängige Proteine verloren nicht nur das Protein selbst, sondern auch ihre RNA‑Vorlagen, was auf einen Qualitätskontrollweg namens RAPP hindeutet. Wenn SRP nicht korrekt an ein entstehendes sekretorisches oder membranlokalisiertes Protein binden kann, scheint dieser Weg den Abbau der entsprechenden RNA auszulösen und so die weitere Produktion eines fehlgeleiteten Proteins zu verhindern. Gleichzeitig werden unvollständig synthetisierte Proteine, die das endoplasmatische Retikulum nicht erreichen, wahrscheinlich mit kleinen molekularen Markern versehen und zu zellulären „Schreddern“ — den Proteasomen — geleitet. Interessanterweise wurden klassische Stresswege des endoplasmatischen Retikulums nicht stark aktiviert, was darauf schließen lässt, dass defektes SRP eine andere Art von zellulärer Stressantwort hervorruft.
Was das für Gesundheit und Krankheit bedeutet
Indem erstmals in menschlichen Zellen kartiert wurde, welche sekretorischen und membranständigen Proteine SRP‑abhängig bzw. SRP‑unabhängig sind, liefert diese Arbeit eine Referenzkarte der Versandregeln der Zelle. Die Ergebnisse zeigen, dass die meisten exportierten Proteine tatsächlich auf SRP angewiesen sind und dass Zellen bei Versagen von SRP sowohl Proteine als auch deren Blaupausen abbauen und alternative Bewältigungsmechanismen aktivieren. Da viele krankheitsverursachende Mutationen die Signalsequenzen sekretorischer Proteine betreffen, kann das Verständnis, wie SRP seine Klienten erkennt und wie RAPP fehlerhafte Exemplare entfernt, erklären, warum bestimmte Mutationen zu Hormonmängeln, Immunstörungen oder Neurodegeneration führen — und möglicherweise langfristig neue Ansätze liefern, um die Protein‑Sortierung im Menschen gezielt zu beeinflussen.
Zitation: Miller, S.C., Tikhonova, E.B., Rodríguez-Almonacid, C.C. et al. Signal recognition particle-dependent secretome in humans. Sci Rep 16, 8760 (2026). https://doi.org/10.1038/s41598-026-35427-3
Schlüsselwörter: Proteinsekretion, Signal Recognition Particle, Secretom, Protein‑Qualitätskontrolle, Endoplasmatisches Retikulum