Clear Sky Science · de
Sequenzielle Platin- und PARP‑Hemmung erhöht die Wirksamkeit der PD1‑Immuntherapie bei murinem, BRCA2‑mutiertem Pankreaskarzinom
Warum diese Forschung für Patienten wichtig ist
Pankreaskrebs zählt zu den tödlichsten Krebsarten, und selbst wenn Ärzte eine verwundbare Stelle im Tumor kennen – etwa eine Mutation im BRCA2‑Gen – halten die heutigen Behandlungen die Krankheit selten lange unter Kontrolle. Diese Studie verwendet ein realitätsnahes Mausmodell, um eine praktische Frage zu beantworten, die viele Patienten und Onkologen heute beschäftigt: Kann das Hinzufügen moderner Immuntherapie nach intensiver Chemotherapie und einem PARP‑Inhibitor das Überleben spürbar verlängern, und warum kommen Tumoren so oft zurück?
Ein hartnäckiger Krebs mit genetischer Schwachstelle
Das duktale Adenokarzinom des Pankreas ist berüchtigt schwer zu behandeln, mit einer Fünfjahresüberlebensrate, die noch im einstelligen Prozentbereich liegt. Ein kleiner Teil der Patienten trägt erbliche oder tumorspezifische Defekte in BRCA2, einem Gen, das für die Reparatur gebrochener DNA nötig ist. Diese Tumoren sind ungewöhnlich empfindlich gegenüber DNA‑schädigenden Medikamenten wie platinbasierten Chemotherapien und gegenüber PARP‑Inhibitoren, die die Fähigkeit der Krebszellen zur DNA‑Reparatur zusätzlich beeinträchtigen. Die aktuelle Standardbehandlung für fortgeschrittenen, BRCA‑mutierten Pankreaskrebs sind mehrere Monate Platin‑Chemotherapie gefolgt von einer Erhaltungsbehandlung mit einem PARP‑Inhibitor. Doch in der wichtigen POLO‑Studie verlängerte diese Strategie nicht das Gesamtüberleben, was die Notwendigkeit unterstreicht, Resistenzen zu verstehen und bessere Erhaltungsansätze zu entwickeln.
Ein realitätsnäheres Mausmodell entwickeln
Viele gängige Labor‑Modelle entfernen die immunologischen und stromalen Komponenten, die echte Tumoren beim Menschen umgeben. Um dem entgegenzuwirken, erzeugten die Autoren Mäuse, die BRCA2‑defiziente Pankreastumoren in einem vollständig funktionierenden Immunsystem entwickeln. Aus diesen spontanen Tumoren leiteten sie klonale Zelllinien ab, die in genetisch passenden Mäusen implantiert werden konnten. Diese Brca2‑mutierten Tumoren sahen menschlichem Pankreaskrebs sehr ähnlich und verhielten sich auch so: sie waren dicht fibrotisch, schlossen weitgehend T‑Zellen aus und zeigten hohe Werte spontaner DNA‑Schäden. Entscheidend war, dass die Tumoren hochsensitiv gegenüber einer gängigen Platin‑Kombination (Gemcitabin plus Cisplatin) waren, während die Behandlung mit einem PARP‑Inhibitor allein in Tieren nur mäßige und kurzlebige Effekte zeigte, obwohl dieselben Zellen in der Zellkultur stark ansprechbar waren. 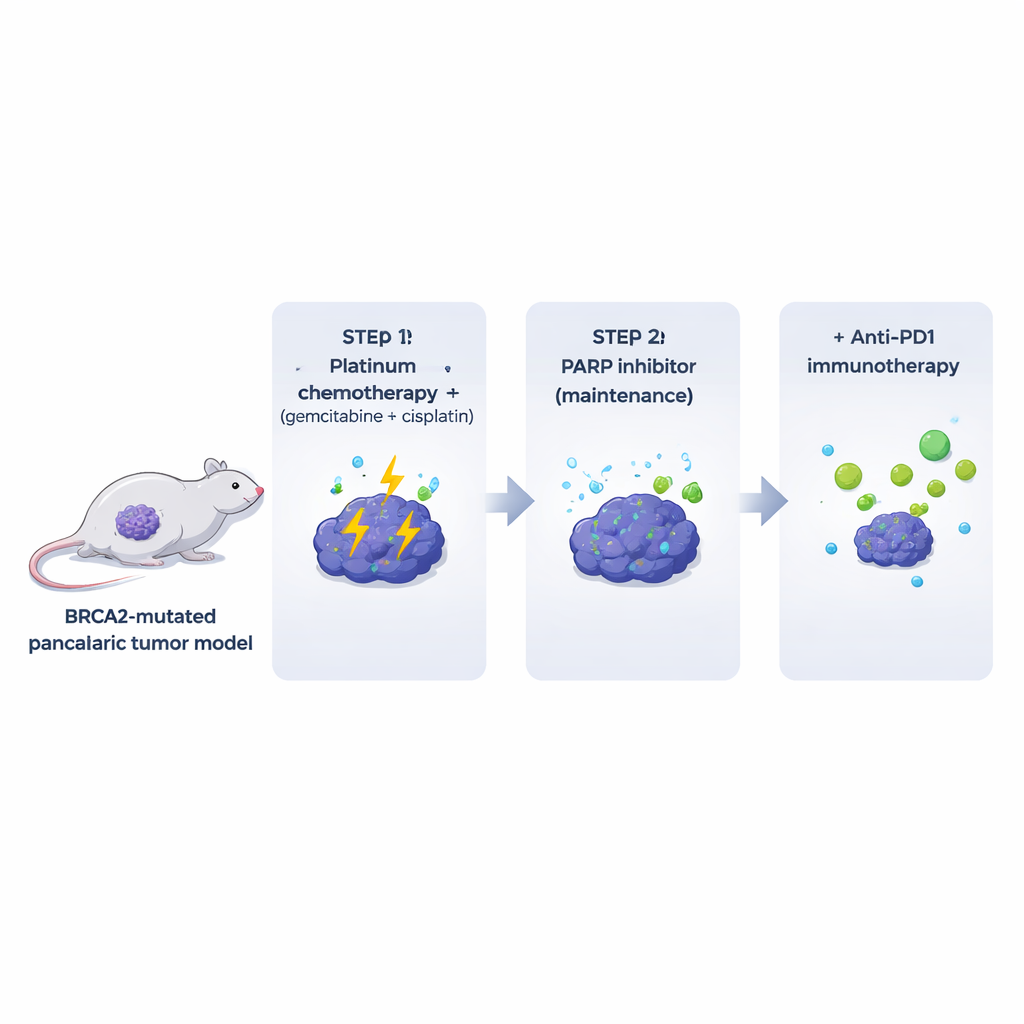
Chemotherapie verändert das Tumorumfeld
Das Team untersuchte dann, was zehn Tage nach einer Platin‑Chemotherapie im Tumor passiert. Die Tumoren waren zwar geschrumpft, jedoch nicht vollständig eliminiert. Genexpressionsanalysen zeigten eine auffällige Verschiebung hin zu immunbezogener Aktivität: Signalwege, die mit T‑Zell‑Aktivierung und adaptiver Immunität verknüpft sind, wurden hochreguliert. Mehr T‑Zellen fanden sich in den behandelten Tumoren, und viele dieser T‑Zellen trugen Erschöpfungsmarker – Hinweise darauf, dass sie aktiviert worden waren, aber zunehmend unwirksam wurden. Ähnliche Muster mit einer erhöhten T‑Zell‑Präsenz wurden auch bei menschlichen Pankreastumoren mit BRCA‑ oder verwandten PALB2‑Mutationen nach präoperativer platinbasierter Chemotherapie beobachtet. Gleichzeitig erhöhten die Tumorzellen ihre PD‑L1‑Spiegel, ein Oberflächenprotein, das T‑Zellen durch Bindung an den PD‑1‑Rezeptor abschalten kann, was darauf hindeutet, dass die Tumoren sich gegen diesen neuen Immunstress verteidigten.
Warum PARP allein nicht ausreicht – und wo Resistenzen entstehen
Analog zur Patientenversorgung erhielten die Mäuse zunächst eine Behandlung mit Gemcitabin und Cisplatin, gefolgt von einer Erhaltungstherapie mit dem PARP‑Inhibitor Olaparib. Diese Abfolge verbesserte die Tumorkontrolle und das Überleben im Vergleich zur Chemotherapie allein und bestätigte, dass vorausgegangene Chemotherapie Tumoren gegenüber PARP‑Hemmung empfindlicher machen kann. Dennoch wurden keine Mäuse geheilt: Unter PARP‑Erhaltung wuchsen die Tumoren schließlich wieder. Resistente Tumoren zeigten ein stärker differenziertes Erscheinungsbild und deutlich erhöhte Werte des Entwicklungsregulators CDX2. Das deutet darauf hin, dass in diesem Modell die Resistenz nicht einfach durch die Wiederherstellung des ursprünglichen DNA‑Reparaturdefekts entsteht, sondern mit einer Verschiebung in der zellulären Identität des Tumors verbunden sein kann. CDX2 könnte potenziell als Biomarker für entstehende Resistenz bei Patienten dienen.
Immuntherapie entfesseln mit der richtigen Abfolge
Immun‑Checkpoint‑Medikamente wie Anti‑PD1‑Antikörper haben die Behandlung mehrerer Krebsarten transformiert, doch der Pankreaskrebs bleibt weitgehend unempfänglich. Konsistent damit konnte Anti‑PD1 (mit oder ohne einen weiteren Checkpoint‑Antikörper, Anti‑CTLA4) weder bei unbehandelten BRCA2‑mutierten Tumoren helfen noch viel bewirken, wenn es einfach zur PARP‑Therapie hinzugefügt wurde. Das Bild änderte sich jedoch, wenn die gesamte Abfolge angewendet wurde: zuerst Platin‑Chemotherapie, dann PARP‑Hemmung plus Anti‑PD1 als Erhaltung. In diesem Setting schrumpften die Tumoren stärker und die Mäuse lebten länger als bei Chemotherapie plus PARP‑Inhibitor oder Anti‑PD1 allein. Das Hinzufügen von Anti‑CTLA4 zur PARP‑Erhaltung brachte keine vergleichbaren Vorteile, was darauf hindeutet, dass das chemotherapie‑vorbereitete Tumorumfeld speziell dafür empfänglich ist, auf eine PD‑1‑Blockade zu reagieren. 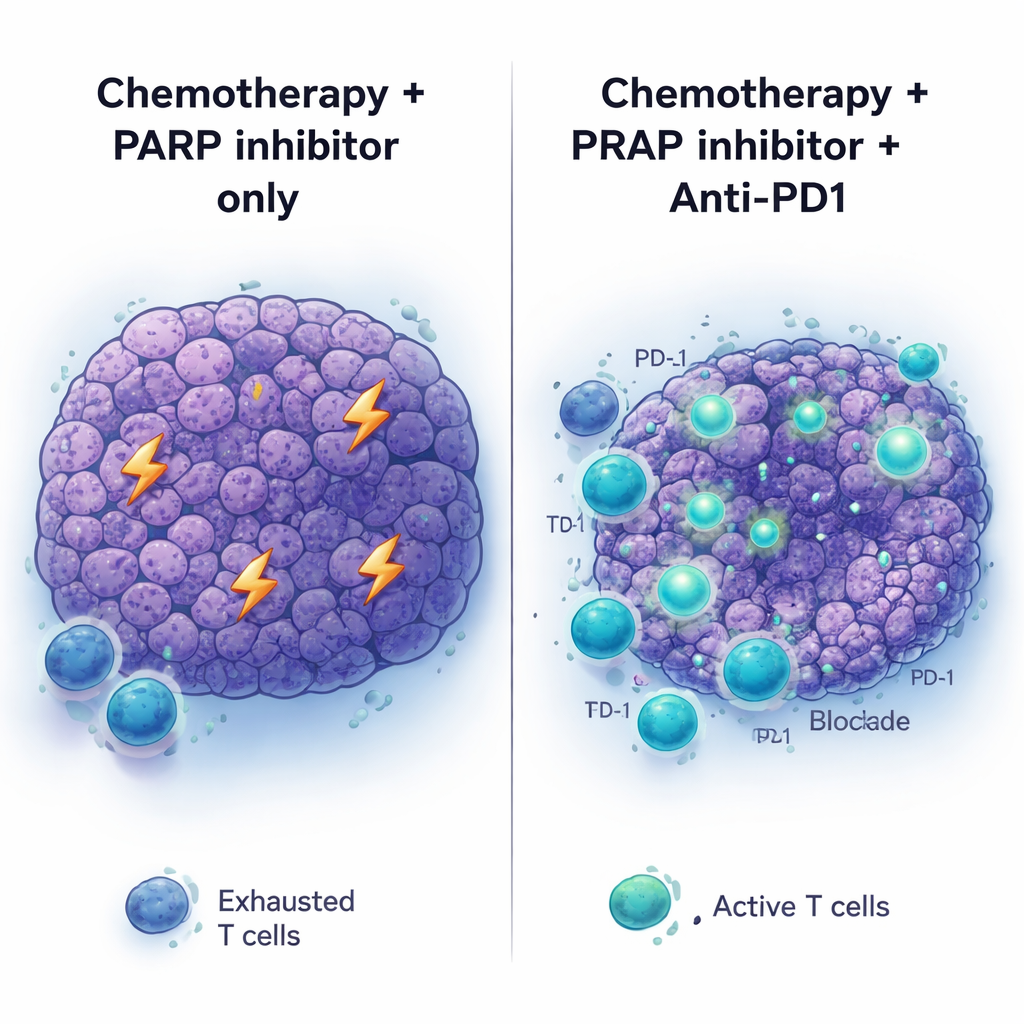
Was das für die zukünftige Versorgung bedeuten könnte
Zusammengefasst legt die Studie nahe, dass bei BRCA‑mutiertem Pankreaskrebs die Reihenfolge und Kombination der Therapien stark ins Gewicht fallen. Stark DNA‑schädigende Chemotherapie greift Tumorzellen nicht nur direkt an, sondern löst auch eine Immunantwort aus, selbst wenn diese anfänglich durch Erschöpfung und PD‑L1‑Verteidigung abgeschwächt ist. PARP‑Inhibitoren können den Nutzen verlängern, sind allein jedoch kaum kurativ und können Tumoren in einen resistenten, CDX2‑hohen Zustand treiben. Durch das Schichten von Anti‑PD1‑Immuntherapie auf die PARP‑Erhaltung nach Platin‑Chemotherapie könnte es möglich sein, dieses kurzzeitig entzündete, erschöpfte Immunmilieu in einen wirksameren und langlebigeren antitumoralen Angriff umzuwandeln. Laufende klinische Studien, die PARP‑Inhibitoren mit Immuntherapie bei BRCA‑assoziiertem Pankreaskrebs kombinieren, werden entscheidend sein, um zu klären, ob diese sorgfältig getimte Strategie in längere, bessere Leben für Patienten übertragbar ist.
Zitation: McVey, J.C., Wattenberg, M.M., Coho, H. et al. Sequential platinum and PARP Inhibition enhances PD1 immunotherapy efficacy in murine Brca2 mutated pancreatic cancer. Sci Rep 16, 6808 (2026). https://doi.org/10.1038/s41598-026-35423-7
Schlüsselwörter: Pankreaskrebs, BRCA2‑Mutation, Platin-Chemotherapie, PARP‑Inhibitor, PD‑1‑Immuntherapie