Clear Sky Science · de
Störung der intrazellulären Eisenhomöostase durch mitochondriale Dysfunktion im Zusammenhang mit der Unterdrückung der ATP13A2-Expression
Warum Eisen innerhalb von Gehirnzellen wichtig ist
Morbus Parkinson ist vor allem für Zittern und steife Bewegungen bekannt, doch tief im Inneren betroffener Gehirnzellen läuft ein anderes Drama ab: Eisen, ein lebensnotwendiges Metall, sammelt sich an Orten an, an denen es nichts zu suchen hat. In dieser Studie wird eine einfache, aber wichtige Frage gestellt: Wie kommt es zu dieser Eisenanhäufung, und wie könnte sie die winzigen Kraftwerke und Recyclingzentren der Nervenzellen schädigen? Die Beantwortung liefert Hinweise darauf, warum bestimmte Hirnregionen bei Parkinson und verwandten Erkrankungen degenerieren, und weist auf neue Behandlungsansätze hin, die über das Ersetzen von Dopamin hinausgehen.
Ein genauerer Blick auf einen seltenen genetischen Hinweis
Die Forscher konzentrieren sich auf eine seltene erbliche Form von Parkinson, PARK9 genannt, die durch Defekte im Gen ATP13A2 verursacht wird. Dieses Gen kodiert ein Protein, das in den Lysosomen sitzt – den Abbau- und Recyclingkompartimenten der Zelle. Menschen mit ATP13A2-Mutationen können zudem eine Erkrankung entwickeln, die durch Eisenablagerungen im Gehirn gekennzeichnet ist. Diese Verbindung machte ATP13A2 zu einem idealen Ansatzpunkt, um zu untersuchen, wie das Eisenungleichgewicht entsteht. Mithilfe einer humanen, neuronähnlichen Zelllinie, die das Parkinson-Protein Alpha‑Synuclein überexprimiert, setzten die Forschenden kleine RNA-Fragmente ein, um ATP13A2 herunterzuregulieren, und verfolgten dann, wie sich Eisenhaushalt, Energieproduktion und Zellgesundheit veränderten.
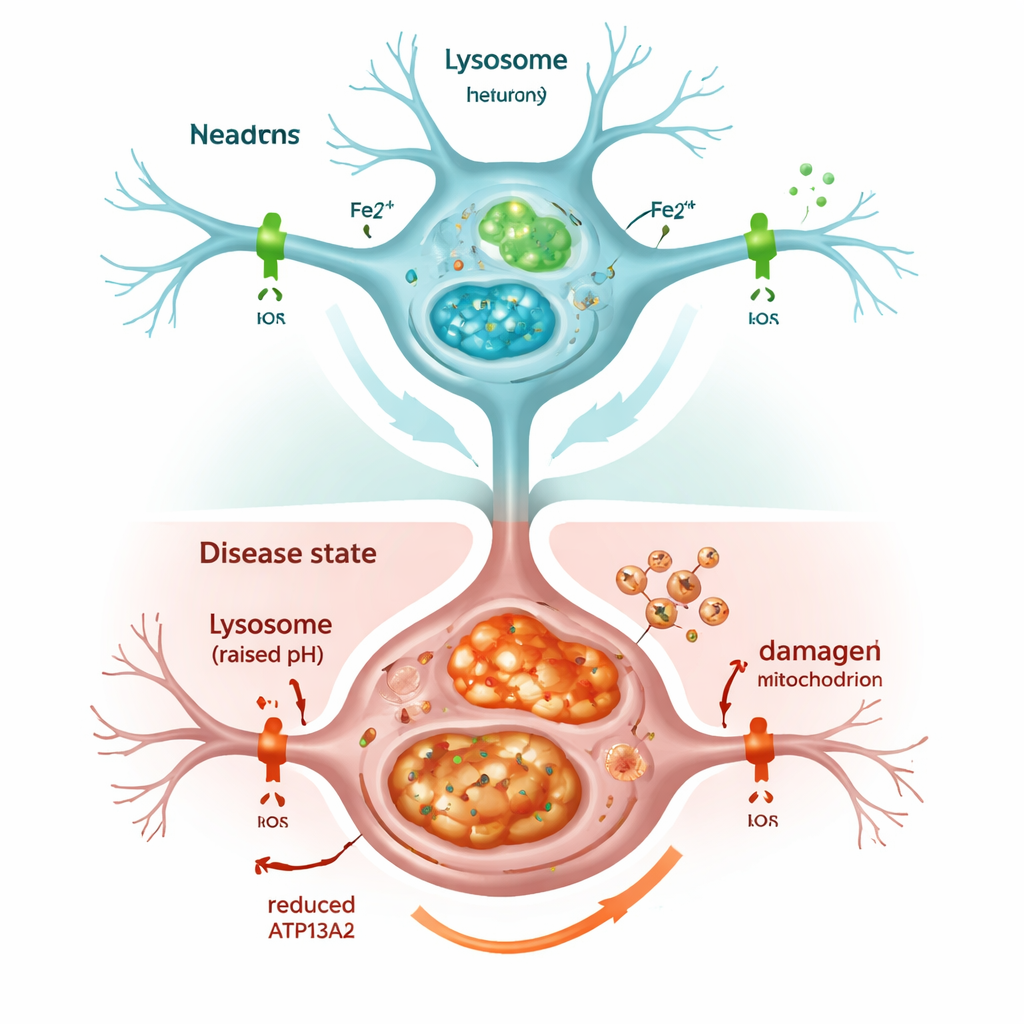
Wenn das Recycling der Zelle stockt
Die Abschaltung von ATP13A2 schwächte schnell die Lysosomen. Ihre innere Säure-Umgebung, die für den Abbau unerwünschter Substanzen wichtig ist, nahm ab, und Marker des Zellreinigungsprozesses, der Autophagie, häuften sich anstatt abgebaut zu werden. Infolgedessen akkumulierte Alpha‑Synuclein, was dem entspricht, was man in Parkinson-Gehirnen sieht. Die Zellen wiesen außerdem insgesamt mehr Eisen auf und insbesondere mehr der chemisch aktiven Form Fe2+ in sowohl Lysosomen als auch Mitochondrien. Die Zelle reagierte, indem sie mehr Ferritin produzierte, ein Protein, das Eisen speichert, doch das reichte nicht aus, um die Schäden zu verhindern: Die überlasteten Mitochondrien erzeugten vermehrt reaktive Sauerstoffspezies, und das Überleben der Zellen nahm ab. Die Behandlung der Zellen mit einem eisenbindenden Wirkstoff, ähnlich denen, die klinisch verwendet werden, verringerte diesen oxidativen Stress und verbesserte teilweise die Zellvitalität, was unterstreicht, dass überschüssiges Eisen selbst ein treibender Faktor der Schädigung ist.
Eisensensoren hören nicht mehr auf das Metall
Normalerweise besitzen Zellen ein Rückkopplungssystem, das registriert, wenn Eisen ansteigt, und daraufhin die Eisenaufnahme drosselt. Ein Protein namens IRP2 erkennt Eisen, zum Teil über ein hämbedingtes Signal aus den Mitochondrien, und reguliert so die Produktion von eisentransportierenden Proteinen an der Zelloberfläche. In den ATP13A2-defizienten Zellen versagte diese Schutzfunktion. Transporter, die Eisen in die Zelle bringen, blieben hochreguliert, obwohl das Eisen bereits erhöht war. Die IRP2-Proteinspiegel änderten sich kaum, und zusätzliches externes Eisen löste nicht seinen normalen Abbau aus. Das Team verfolgte dieses Versagen bis zu den Mitochondrien: Geschädigte Mitochondrien atmeten weniger effizient, zeigten Anzeichen fehlerhafter Qualitätskontrolle (Mitophagie) und, entscheidend, verloren die Fähigkeit, Häm zu synthetisieren, das eisenhaltige Molekül, das IRP2 bei der Eisenerkennung hilft. Ohne ausreichendes Häm erhielt IRP2 keine "zu viel Eisen"-Nachricht und erlaubte einen fortgesetzten Eisenzufluss.
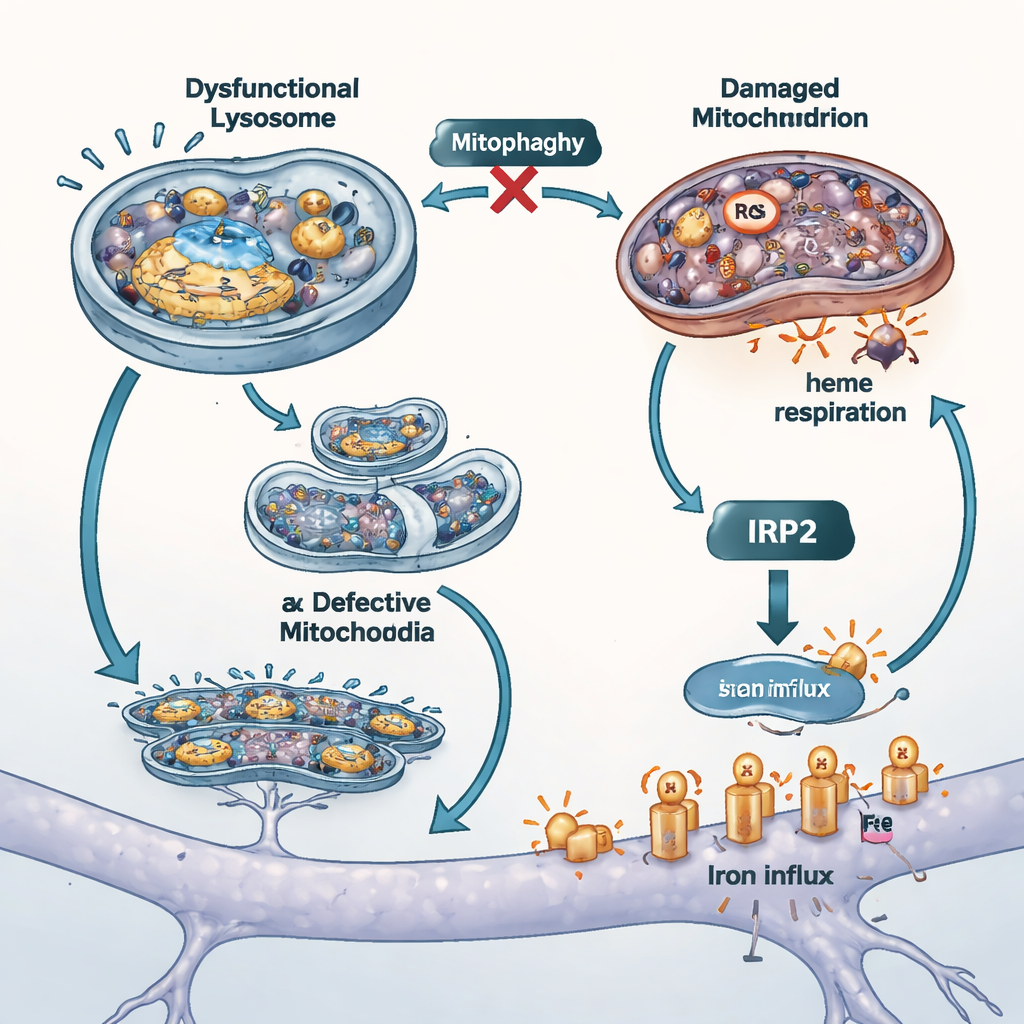
Den Eisenhahn zudrehen und andere Modelle prüfen
Um zu prüfen, wie stark dieser ungehemmte Eiseneintritt zur Zellverletzung beitrug, blockierten die Wissenschaftler zwei Hauptwege der Eisenaufnahme. Sie verwendeten transferrinfreies Transferrin, um mit einem Importer zu konkurrieren, und ein kleines Medikament, um die Aktivität eines anderen Transporters namens DMT1 zu dämpfen. Beide Maßnahmen senkten das Gesamt- und freie Eisen in den Zellen, reduzierten mitochondriale oxidative Belastung und verbesserten das Überleben, was nahelegt, dass Oberflächen-Eisenkanäle wichtige Verstärker der Schädigung sind, wenn ATP13A2 verloren geht. Die Forschenden wiederholten außerdem zentrale Experimente in Zellen, denen ein anderes Parkinson-assoziiertes Gen, PINK1, fehlte, das für gestörte Mitophagie bekannt ist. Diese Zellen zeigten dieselbe Kombination aus Eisenansammlung und geschwächter Hämsynthese und stützen die Idee, dass mitochondriale Qualitätskontrolle und Eisenbalance in verschiedenen Formen der Erkrankung eng verknüpft sind.
Was das für Parkinson und künftige Therapien bedeutet
Kurz gesagt skizziert die Studie einen Teufelskreis. Wenn ATP13A2 unterdrückt ist, versagen Lysosomen darin, beschädigte Komponenten zu beseitigen, einschließlich fehlerhafter Mitochondrien. Diese geschwächten Mitochondrien produzieren dann weniger Energie und weniger Häm, wodurch das Eisensensorsystem der Zelle abgeschwächt wird. Eisen strömt weiterhin über Oberflächen-Transporter ein, sammelt sich in empfindlichen Kompartimenten und treibt toxische Reaktionen an, die die Mitochondrien weiter schädigen. Im Laufe der Zeit könnte diese Schleife erklären, warum bestimmte Neurone bei Parkinson und verwandten eisenbelasteten Hirnerkrankungen absterben. Die Ergebnisse legen nahe, dass künftige Therapien nicht nur überschüssiges Eisen entfernen sollten, sondern auch die richtige Lysosomenfunktion, mitochondriale Qualitätskontrolle und Hämsynthese wiederherstellen könnten – also das Problem an der Quelle bekämpfen, statt das Metall nachträglich nur zu beseitigen.
Zitation: Murakami, T., Ohuchi, K., Kiuchi, M. et al. Disruption of intracellular iron homeostasis through mitochondrial dysfunction associated with suppression of ATP 13A2 expression. Sci Rep 16, 5007 (2026). https://doi.org/10.1038/s41598-026-35368-x
Schlüsselwörter: Morbus Parkinson, Gehirneisen, Mitochondrien, Lysosomen, Hämsynthese