Clear Sky Science · de
Untersuchung der funktionellen Hot‑Spot‑Reste eines Enzyms durch Echtzeit‑Überwachung der enzymatischen Reaktion mittels NMR und rechnerischer Ansätze
Warum das für künftige Virostatika wichtig ist
Favipiravir ist eine Tablette, die bereits gegen Influenza eingesetzt und für COVID‑19 getestet wurde, aber in der Form, die wir schlucken, bekämpft sie Viren nicht direkt. Unsere Zellen müssen sie zuerst in ein aktives, virusblockierendes Molekül umwandeln. Diese Studie zerlegt, nahezu Atom für Atom, wie ein menschliches Enzym einen entscheidenden Aktivierungsschritt durchführt und welche winzigen Bereiche des Enzyms als „Hot‑Spots“ fungieren, die bestimmen, wie schnell und wie gut das Medikament aktiviert wird. Das Verständnis dieser Details könnte das Design der nächsten Generation von Virostatika leiten, die sowohl wirksamer als auch vorhersagbarer im Patienten sind.
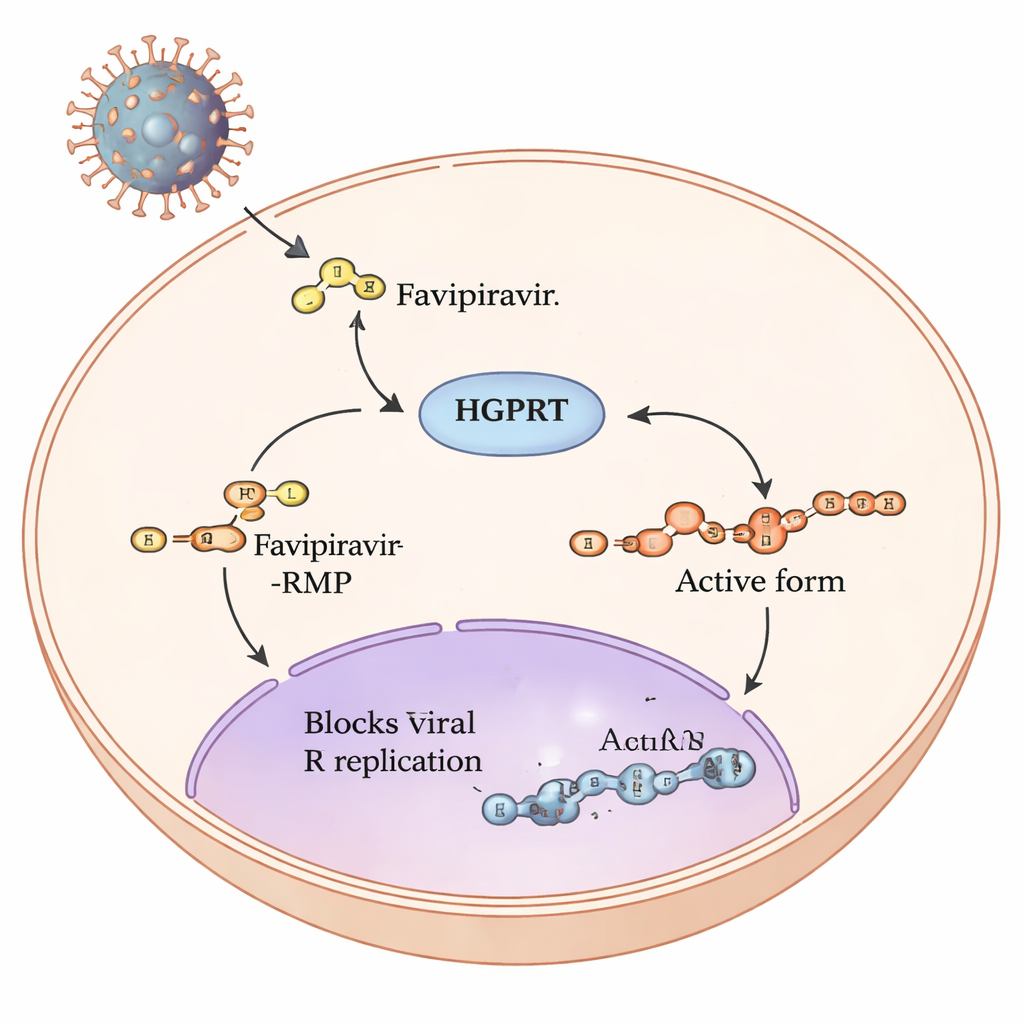
Die Reise eines Prodrugs in unseren Zellen
Favipiravir ist ein sogenanntes Prodrug: Sobald es in menschliche Zellen gelangt, wird es in mehreren chemischen Schritten so umgebaut, dass es die Kopiermaschine von RNA‑Viren wie Influenza und SARS‑CoV‑2 blockieren kann. Der erste und langsamste Schritt dieses Weges wird von einem menschlichen Enzym namens Hypoxanthin‑Guanin‑Phosphoribosyltransferase, kurz HGPRT, katalysiert. HGPRT fügt Favipiravir eine kleine Zucker‑Phosphat‑Gruppe hinzu und erzeugt Favipiravir‑RMP. Erst nach diesem Schritt können andere Enzyme die vollständig aktive Triphosphat‑Form bauen, die direkt die virale RNA‑Polymerase stört. Da dieser erste HGPRT‑getriebene Schritt wie ein Engpass wirkt, der bestimmt, wie viel aktives Medikament entsteht, wollten die Autoren herausfinden, welche Teile von HGPRT am wichtigsten für die Verarbeitung von Favipiravir sind.
Chemie in Echtzeit mit NMR beobachten
Einzigartig an Favipiravir ist ein Fluor‑Atom, das sich in einem Magnetfeld wie ein winziger Funksender verhält. Das Team nutzte dies, indem es Fluor‑19‑Kernspinresonanz (NMR) verwendete, um in Echtzeit zu beobachten, wie viel Favipiravir und wie viel Favipiravir‑RMP zu verschiedenen Zeitpunkten in einer Reaktionslösung vorhanden waren. Weil nur das Medikament Fluor trägt, sind die NMR‑Signale sauber und leicht zu verfolgen. Durch wiederholte Aufnahme von Spektren über 12 Stunden konnten die Forschenden das Verschwinden des Ausgangsstoffes und das Anwachsen des modifizierten Produkts verfolgen und daraus übliche kinetische Größen wie die Reaktionsgeschwindigkeit und die scheinbare Bindungsstärke des Enzyms ableiten.
Schlüsselpositionen im Enzym feinjustieren
Frühere Röntgenschnappschüsse von HGPRT gebunden an Favipiravir‑RMP hatten einige Aminosäuren vorgeschlagen, die das Medikament in einer Tasche umschließen. Die neue Arbeit prüft drei dieser Positionen, indem präzise Einbuchstabenänderungen im Protein erzeugt und jedes Mutantenenzym mit dem natürlichen verglichen wurde. Eine Veränderung, bezeichnet T138A, machte das Enzym überraschenderweise etwa vier- bis sechsmal schneller bei der Umwandlung von Favipiravir, obwohl dabei eine chemische Gruppe entfernt wurde, von der man annahm, sie trage zur Halterung des Medikaments bei. Eine zweite Änderung, K140M, verlangsamte die Reaktion moderat und schwächte die scheinbare Bindung leicht. Eine dritte Änderung, D193N, hob die Fähigkeit des Enzyms, Favipiravir‑RMP zu erzeugen, vollständig auf, obwohl das veränderte Protein noch hergestellt werden konnte und das Produkt binden zeigte. Zusammengenommen zeigen diese Ergebnisse, dass nicht alle Kontaktstellen gleichwertig sind: Einige wirken als subtile Geschwindigkeitsregulatoren, andere als unverzichtbare Schalter.
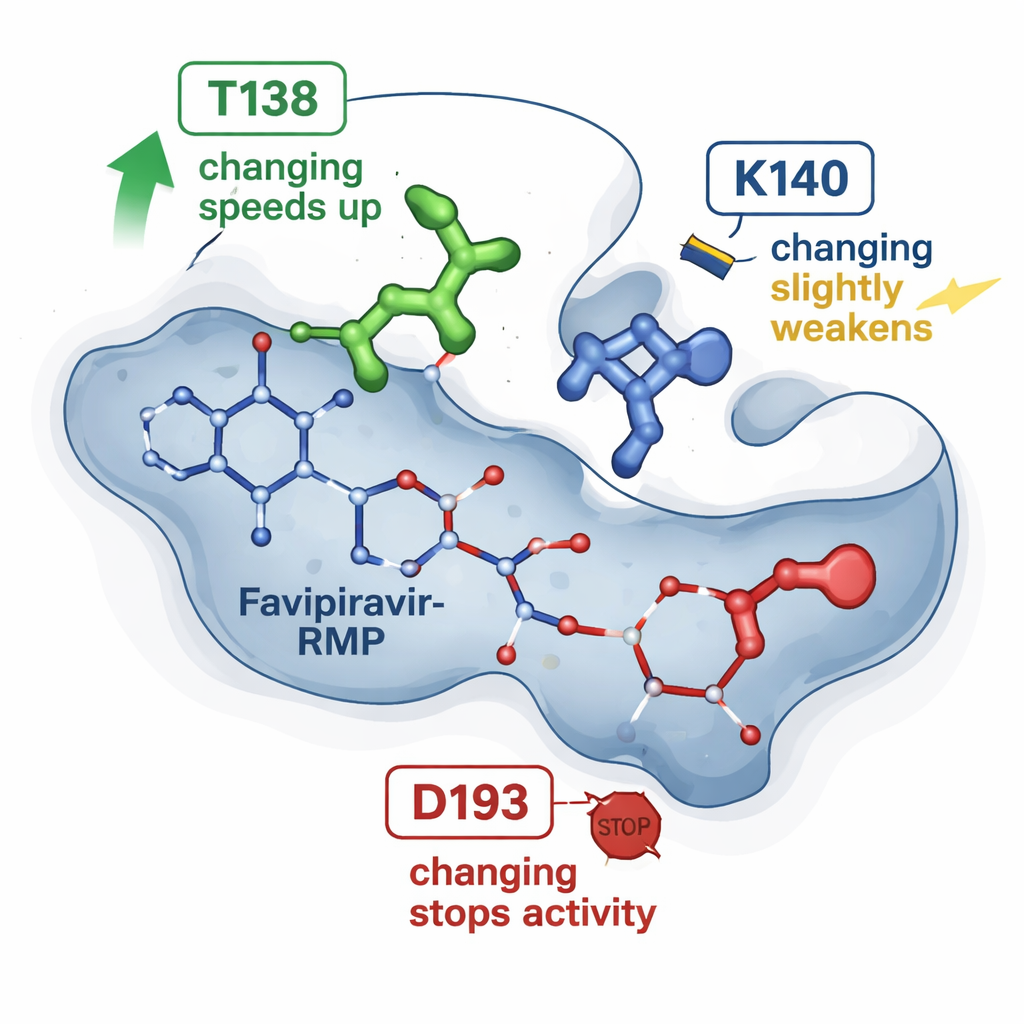
Die beweglichen Teile am Computer simulieren
Um über statische Strukturen hinauszublicken, wandten sich die Forschenden molekularen Simulationen zu. Ausgehend von der bekannten dreidimensionalen Struktur von HGPRT mit Favipiravir‑RMP nutzten sie etablierte rechnerische Werkzeuge, um abzuschätzen, wie stark das Medikament in jedem Mutanten bindet, und führten viele kurze Molekulardynamik‑Simulationen durch. Diese Simulationen verfolgen, wie die Atome über zehn‑ bis hundert Nanosekunden wackeln und interagieren. Die Berechnungen stimmten mit den NMR‑abgeleiteten Trends überein: Die T138A‑Variante schien Favipiravir‑RMP günstiger zu halten, zeigte aber auch Episoden, in denen das Medikament sich einem „Flucht“‑Pfad näherte, geführt von einem anderen Rest (K140), der die Phosphatgruppe kurzzeitig verankert, bevor sie freigesetzt wird. Im Gegensatz dazu hielt die D193N‑Variante das Produkt zwar noch, scheiterte aber offenbar an einem früheren katalytischen Schritt, der ein Magnesiumion erfordert, was erklärt, warum sie trotz stabiler Bindung die Aktivität verlor.
Eine Landkarte für intelligenteres antivirales Design
Durch die Kombination von Echtzeit‑NMR‑Messungen mit detaillierten Computermodellen kartiert diese Studie die funktionellen Hot‑Spots in HGPRT, die darüber entscheiden, wie effizient Favipiravir aktiviert wird. Für Nicht‑Spezialisten lautet die Erkenntnis: Unsere eigenen Enzyme können stark beeinflussen, wie viel aktives antivirales Medikament sich in Zellen anreichert, und eine Anpassung sowohl der Form des Medikaments als auch der Tasche des Enzyms kann dieses Ergebnis dramatisch verändern. Die hybride Strategie der Autoren bietet eine allgemeine Blaupause, um zu untersuchen, wie andere Wirkstoffe mit ihren Zielproteinen interagieren, und könnte die Entwicklung neuer antiviraler Verbindungen beschleunigen, die besser auf die Aktivierungsmaschinerie des Körpers abgestimmt sind.
Zitation: Sugiki, T., Yoshida, T., Tsukamoto, M. et al. Investigation of the functional hot-spot residues of an enzyme by real-time monitoring of the enzymatic reaction using NMR and computational approaches. Sci Rep 16, 5896 (2026). https://doi.org/10.1038/s41598-026-35354-3
Schlüsselwörter: Favipiravir, Aktivierung antiviraler Mittel, HGPRT‑Enzym, NMR‑Spektroskopie, Arzneimittel‑Design