Clear Sky Science · de
Informierte räumlich sensible Muster für multiplexe Immunfluoreszenzdaten
Warum die Nachbarschaft von Tumorzellen wichtig ist
Pankreaskrebs gehört zu den tödlichsten Krebsarten, zum Teil weil seine Tumoren in einer komplexen „Nachbarschaft“ aus Immun- und Stütz-Zellen leben, die den Krebs entweder bekämpfen oder ihm helfen, sich zu verstecken. Diese Studie stellt eine neue Methode vor, um die räumliche Anordnung dieser Zellen in Mikroskopbildern zu lesen, und zeigt, wie sich das Verhalten des Immunsystems bei aggressivem Pankreasduktaladenokarzinom (PDAC) im Vergleich zu seinem präkanzerösen Gegenstück, dem intraduktalen papillären muzinösen Neoplasma (IPMN), unterscheidet. Das Verständnis dieser verborgenen Muster könnte auf bessere Diagnosen und klügere, gezieltere Behandlungen hinweisen.
Gewebe als Karten sehen, nicht nur als Bilder
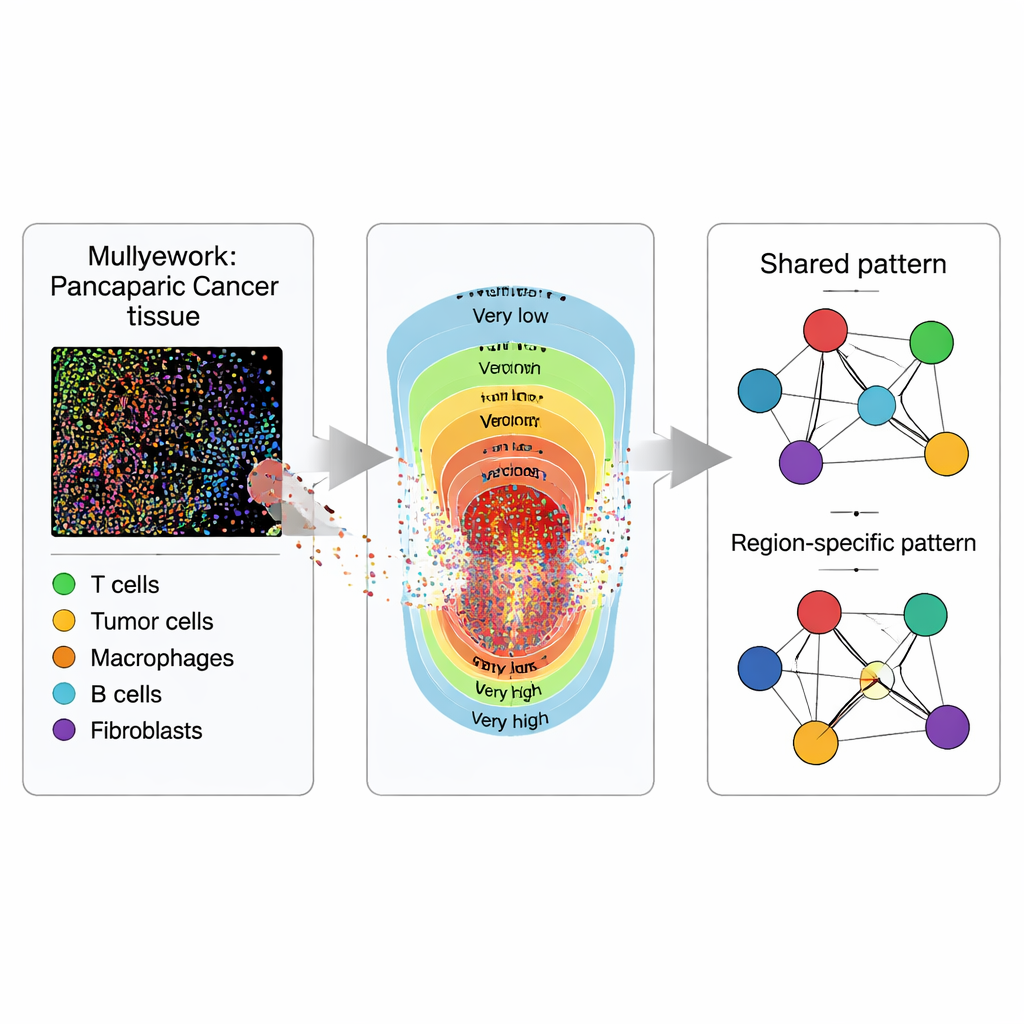
Anstatt einen Tumorschnitt als flaches Bild zu behandeln, sehen die Forschenden ihn wie eine Karte voller Punkte. Mit multiplexer Immunfluoreszenz-Imaging färben sie Gewebeproben von 119 PDAC- und 53 IPMN-Patienten so, dass verschiedene Zelltypen in unterschiedlichen Farben leuchten. Spezialisierte Software verwandelt jede sichtbare Zelle in einen Punkt mit Koordinaten und einer Beschriftung: Tumor-(epithel-)zellen, mehrere Typen von T‑Zellen, die angreifen oder Immunantworten regulieren können, und antigenpräsentierende Zellen, die Tumorfragmente den T‑Zellen zeigen. Die Kernfrage ist nicht nur, wie viele von jedem Zelltyp vorhanden sind, sondern wo sie zueinander im Gewebe liegen.
Den Tumor in Zonen aufteilen
Um abzubilden, wie Tumoren vom Zentrum nach außen variieren, teilt jede Gewebeprobe das Team in fünf Zonen ein, basierend darauf, wie dicht die Tumorzellen gepackt sind, von „sehr niedrig“ bis „sehr hoch“ Tumorintensität. Diese Zonen repräsentieren einen Gradienten von Tumorbelastung und zellulärer Dichte, den Pathologen häufig unter dem Mikroskop sehen, aber selten quantifizieren. Innerhalb jeder Zone schätzt das Team geglättete „Intensitätskarten“ für jeden Zelltyp, wodurch verstreute Punkte in kontinuierliche Heatmaps verwandelt werden, die zeigen, wo sich jeder Zelltyp zu sammeln pflegt. Diese Zonierung erlaubt Vergleiche nicht nur der generellen Zell‑Interaktionen, sondern auch, wie sich diese Interaktionen von dünn besiedelten zu dicht besiedelten Tumorregionen verschieben.
Zellnachbarschaften in Netzwerke verwandeln
Als Nächstes übersetzen die Forschenden die räumlichen Muster in Netzwerke, in denen jeder Zelltyp ein Knoten ist und Verbindungen darstellen, wie stark zwei Zelltypen dazu neigen, zusammen aufzutreten, nachdem für alle anderen berücksichtigt wurde. Mithilfe eines bayesianischen Statistik‑Rahmens, den sie ISPat (Informed Spatially aware Patterns) nennen, trennen sie Merkmale, die über alle Zonen hinweg geteilt werden, von solchen, die zonenspezifisch sind. ISPat kann auch vorhandenes biologisches Vorwissen einbeziehen, was die Schätzung in komplexen Daten stabilisiert. Simulationsversuche zeigen, dass ISPat bekannte Muster zuverlässig rekonstruieren kann und dies deutlich schneller als traditionelle Methoden tut, wodurch es für größere Bildgebungsstudien praktikabel wird.
Zwei Krankheiten, zwei Immunarchitekturen
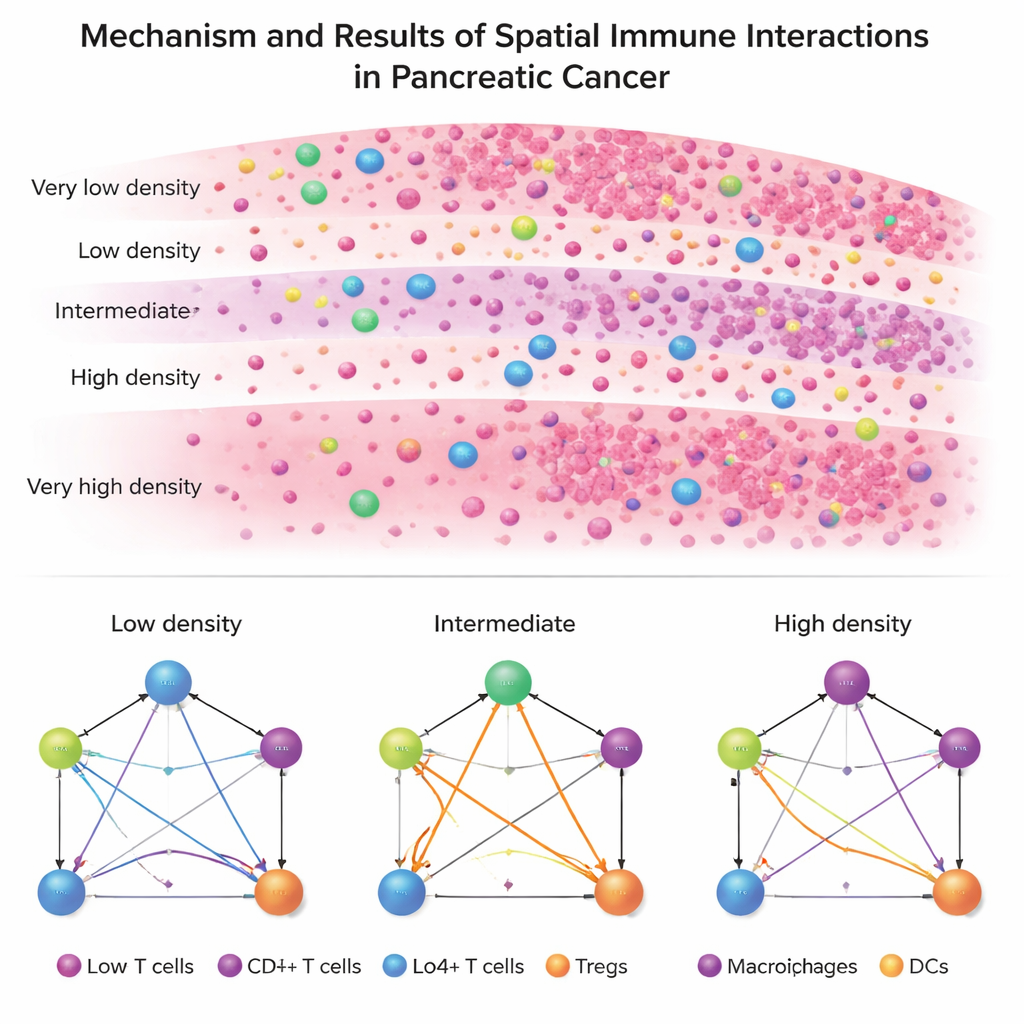
Wenden sie ISPat auf echte Patientendaten an, tritt ein markanter Gegensatz zwischen PDAC und IPMN zutage. PDAC zeigt eine starre, einheitliche Immunarchitektur: in fast allen Zonen behalten Tumorzellen, Helfer‑T‑Zellen, Killer-(zytotoxische)‑T‑Zellen, regulatorische T‑Zellen und antigenpräsentierende Zellen nahezu dasselbe Beziehungs‑Muster bei. Das deutet auf eine stabile, fest verankerte immunsuppressive Umgebung hin, die schwer zu durchbrechen ist. Im Gegensatz dazu zeigt IPMN weit mehr Variation von Zone zu Zone, insbesondere darin, wie regulatorische T‑Zellen mit anderen Immunzellen verbunden sind. Bei IPMN zeigen Zonen mittlerer Dichte — weder vollständig mit Tumorzellen gefüllt noch nahezu tumorfrei — die dramatischsten Umgestaltungen der Immuninteraktionen.
Hotspots für Immunflucht und Therapie
Bei genauerer Betrachtung identifiziert die Studie bestimmte Zellpaar‑Interaktionen, die zwischen PDAC und IPMN konsistent unterschiedlich sind, insbesondere in jenen Zonen mittlerer Dichte. Viele davon betreffen regulatorische T‑Zellen, die Immunangriffe dämpfen können, sowie antigenpräsentierende Zellen und Killer‑T‑Zellen, die Anti‑Tumor‑Antworten auslösen und ausführen. Bemerkenswerterweise divergieren Interaktionen, die Antigenpräsentation und direkte Tumorzerstörung antreiben, ebenso wie solche, die Immunsuppression durchsetzen, am stärksten in diesen Übergangsbereichen und nicht in den extremsten Tumorregionen. Dieses Muster legt nahe, dass das entscheidende Schlachtfeld für die Immunkontrolle in den Übergangszonen liegt, in denen Tumor und Immunsystem noch aktiv verhandeln.
Was das für Patientinnen und Patienten bedeutet
Für Nicht‑Spezialisten lautet die Schlussfolgerung: Wo Zellen im Tumor sitzen, ist genauso wichtig wie welche Zellen dort sind. PDAC scheint eine stabile, unterdrückende Immun"landschaft" zu verankern, während die Immunlandschaft von IPMN flexibler und regionsabhängiger bleibt. Diese räumlichen Fingerabdrücke könnten zu Biomarkern werden, um gefährliche Tumoren von präkanzerösen Läsionen zu unterscheiden und vorherzusagen, welche Patientinnen und Patienten von bestimmten Immuntherapien profitieren könnten. Der ISPat‑Rahmen bietet ein allgemeines Werkzeug, um solche räumlichen Codes in vielen Erkrankungen zu lesen und unterstützt eine Zukunft, in der Krebsbehandlung nicht nur von Genetik und Zelltypen geleitet wird, sondern von der feingliedrigen Geografie der Zellen im Tumor jedes einzelnen Patienten.
Zitation: Bhadury, S., Peruzzi, M., Acharyya, S. et al. Informed spatially aware patterns for multiplexed immunofluorescence data. Sci Rep 16, 5015 (2026). https://doi.org/10.1038/s41598-026-35341-8
Schlüsselwörter: Pankreaskrebs, Tumormikroumgebung, räumliche Bildgebung, Immuninteraktionen, präzisionsonkologie